

分析 (1)根據元素周期表的信息以及離子形成過程來分析;
(2)根據元素在人體內的存在形式以及鐵元素與人體健康的關系來分析;
(3)根據反應原理找出反應物、生成物、反應條件,根據化學方程式的書寫方法、步驟進行書寫;
(4)根據二氧化碳的性質來分析;
(5)根據鐵的化學性質來分析;
(6)根據尾氣中含有一氧化碳來分析;
(7)由混合物的質量和固體減少的質量根據四氧化三鐵和一氧化碳反應的化學方程式可知固體減少的質量就是四氧化三鐵中氧元素的質量,根據氧元素的質量從而求出四氧化三鐵的質量進而求出混合物中鐵的質量分數.
解答 解:(1)鐵的原子序數為26,相對原子質量為55.85;,故填:26;55.85;
在原子中原子序數=質子數=核外電子數,故鐵原子有26個電子,形成亞鐵離子時失去了2個電子,故亞鐵離子還有24個電子但是質子數不變,故填:24;26;
(2)元素在人體內主要是以化合物的形式存在的,缺鐵易患貧血,故填:化合物;c;
(3)一氧化碳還原氧化鐵,主要是利用CO的還原性,在高溫下和氧化鐵反應生成鐵和二氧化碳,反應的化學方程式為Fe2O3+3CO$\frac{\underline{\;高溫\;}}{\;}$2Fe+3CO2.故填:Fe2O3+3CO$\frac{\underline{\;高溫\;}}{\;}$2Fe+3CO2;
(4)產生的二氧化碳與氫氧化鈣反應生成了碳酸鈣白色沉淀和水,故填:渾濁;
(5)鐵能與稀硫酸反應生成硫酸亞鐵和氫氣,此現象說明黑色固體中含有鐵,但不一定全部是鐵.故填:Fe+H2SO4=FeSO4+H2↑;c;
(6)尾氣中含有有毒的一氧化碳氣體,不能直接排放到空氣中,需將其點燃處理,故填:D;
(7)解:設四氧化三鐵的質量為x,由四氧化三鐵和一氧化碳反應的化學方程式可知固體減少的質量就是四氧化三鐵中氧元素的質量可知:
Fe3O4+4CO$\frac{\underline{\;高溫\;}}{\;}$3Fe+4CO2 減少的質量
232 232-168=64
x 10g-7.6g=2.4g
$\frac{232}{64}=\frac{x}{2.4g}$
x=8.7g
則混合物中鐵的質量分數為:$\frac{10g-8.7g}{10g}×100%$=13%
答:10g黑色粉末中單質鐵的質量分數為13%.
點評 本題主要考查有關化學方程式的計算,難度較大.解答本題的關鍵是找到物質間的差量,運用差量法來求解.


科目:初中化學 來源: 題型:選擇題
| A物質的分類 | B物質鑒別 |
| ①鐵、氧氣都屬于單質 ②氧化物中一定含有氧元素 ③混合物一定含有多種元素 | ①硬水和軟水--肥皂水 ②一氧化碳與二氧化碳--澄清石灰水 ③空氣與氮氣--帶火星的木條 |
| C“低碳經濟”的措施 | D用“化學”眼光分析 |
| ①改造或淘汰高能耗、高污染產業 ②研制和開發新能源替代傳統能源 ③減少使用一次性塑料方便袋 | ①用細沙滅火可以降低可燃物的著火點 ②濕衣服晾干是因為分子之間有間隔 ③明礬凈水是因為明礬溶于水生成膠狀物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
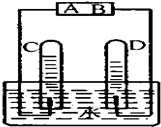 如圖是電解水的簡易裝置
如圖是電解水的簡易裝置查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | CaCl2 KNO3 Na2CO3 KCl | B. | NaCl BaCl2 Na2CO3 HCl | ||
| C. | Na2SO4 Ba(OH)2 Na2CO3 NaNO3 | D. | HNO3 Na2CO3 MgCl2 Ba(OH)2 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題

 ”和“
”和“ ”分別表示不同的原子).
”分別表示不同的原子).
 ”微粒.
”微粒.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com