
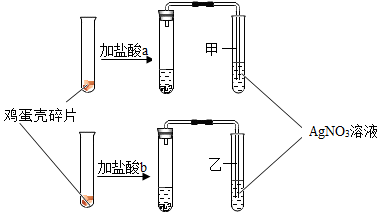
分析 【討論交流】根據碳酸鈣和鹽酸反應生成氯化鈣、水和二氧化碳寫出有氣泡生成的化學方程式;
【做出猜想】根據雞蛋殼的主要成分是碳酸鈣進行分析;
【實驗驗證】根據氯離子和銀離子反應會生成氯化銀沉淀進行分析;
【實驗結論】根據濃鹽酸具有揮發性進行分析;
【反思應用】(1)根據實驗室制備CO2時,最好選擇稀鹽酸進行分析;
(2)根據影響反應速率的因素進行分析.
解答 解:【討論交流】碳酸鈣和鹽酸反應生成氯化鈣、水和二氧化碳,化學方程式為:CaCO3+2HCl═CaCl2+CO2↑+H2O;
【做出猜想】雞蛋殼的主要成分是碳酸鈣,所以依據所學化學知識和生活常識,認為小紅的猜想是不合理的;
【實驗驗證】氯離子和銀離子反應會生成氯化銀沉淀,所以白色沉淀的化學式是AgCl;
【實驗結論】濃鹽酸具有揮發性,所以上述實驗說明鹽酸a中溶質的質量分數一定大于鹽酸b中的溶質的質量分數,同時也說明了雞蛋殼中含有CO32-的可能性;
【反思應用】(1)由于濃鹽酸易揮發出氯化氫氣體,所以實驗室制備CO2時,最好選擇稀鹽酸;
(2)實驗中發現,與相同溶質質量分數的鹽酸反應時,雞蛋殼碎片比大塊雞蛋殼更劇烈,說明增大反應物接觸面積可以加快反應速率.
故答案為:(1)CaCO3+2HCl═CaCl2+CO2↑+H2O;
【做出猜想】小紅;
【實驗驗證】AgCl;
【實驗結論】大于;
【反思應用】(1)稀鹽酸;(2)接觸面積.
點評 在解此類題時,首先分析題中考查的問題,然后結合學過的知識和題中的提示進行解答.


 浙大優學小學年級銜接捷徑浙江大學出版社系列答案
浙大優學小學年級銜接捷徑浙江大學出版社系列答案科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
濃度 反應條件 | 30%的過氧化氫 | 15%的過氧化氫 | 10%的過氧化氫 | 5%的過氧化氫溶液 |
| 無催化劑、不加熱 | 幾乎不反應 | 幾乎不反應 | 幾乎不反應 | 幾乎不反應 |
| 無催化劑、加熱 | 360 | 480 | 540 | 720 |
| 二氧化錳作催化劑、加熱 | 10 | 25 | 60 | 120 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題

查看答案和解析>>
科目:初中化學 來源: 題型:計算題
查看答案和解析>>
科目:初中化學 來源: 題型:推斷題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com