
| 探究過程 | K2CO3) | (NH4)2SO4 | 結論及化學方程式 |
| (1)分別取碳酸鉀和硫酸銨固體,加入足量水溶解,取溶液分別滴入紫色石蕊溶液,觀察溶液顏色變化 | 變藍 | 變紅 | 碳酸鉀溶液顯堿性 硫酸銨溶液顯酸性 |
| (2)另取兩種溶液分別加入足量 稀鹽酸,觀察現象 | 產生氣泡 | 無明顯現象 | 產生氣泡的化學方程式 2HCl+K2CO3=2=KCl+CO2↑+H2O |
| (3)再取兩種溶液分別加入Ba(OH)2溶液,觀察現象 | 產生白色沉淀 | 有白色沉淀生成,同時以刺激性氣味氣體產生 | (NH4)2SO4與Ba(OH)2反應方程式 NH4)2SO4+Ba(OH)2═BaSO4↓+2H2O+2NH3↑ |
分析 【實驗探究】:①根據碳酸鉀與純堿具有相似的化學性質,呈堿性,使石蕊試液變藍,硫酸銨呈酸性使石蕊試液變紅;
②根據碳酸鉀與鹽酸反應生成氯化鉀、水和二氧化碳解答;
③根據氫氧化鋇和硫酸銨反應生成硫酸鋇、氨氣和水解答;
【交流共享】:②銨態氮肥和顯堿性物質混合能生成氨氣,從而降低肥效;
(4)根據質量守恒定律,反應前后減少的質量為二氧化碳的質量,利用二氧化碳純堿樣品中碳酸鈉的質量.
解答 解:【實驗探究】:①碳酸鉀與純堿具有相似的化學性質,所以碳酸鉀溶液呈堿性,使石蕊試液變藍,硫酸銨使石蕊試液變紅,說明呈酸性,
②取兩種溶液分別加入足量稀鹽酸,碳酸鉀與鹽酸反應生成氯化鉀、水和二氧化碳,反應的化學方程式為2HCl+K2CO3=2=KCl+CO2↑+H2O;
③氫氧化鋇和硫酸銨反應生成硫酸鋇、氨氣和水,硫酸鋇是不溶于水的白色物質,氨氣有刺激性氣味,
故填:產生白色沉淀、有刺激性氣味的氣體生成,(NH4)2SO4與 Ba(OH)2反應方程式為:NH4)2SO4+Ba(OH)2═BaSO4↓+2H2O+2NH3↑;
【討論與反思】:②銨態氮肥和顯堿性物質混合能生成氨氣,從而降低肥效,
(4)生成二氧化碳的質量為11g+50g-56.6g=4.4g
設樣品中碳酸鈉的質量為x,
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 4.4g
$\frac{106}{x}=\frac{44}{4.4g}$
解得,x=10.6g
碳酸鈉的質量分數=$\frac{10.6g}{11g}$×100%≈96.4%
答案:
| 探究過程 | K2CO3) | (NH4)2SO4 | 結論及化學方程式 |
| (1)分別取碳酸鉀和硫酸銨固體,加入足量水溶解,取溶液分別滴入紫色石蕊溶液,觀察溶液顏色變化 | 變藍 | 變紅 | 碳酸鉀溶液顯 堿性 硫酸銨溶液顯酸性 |
| (2)另取兩種溶液分別加入足量 稀鹽酸,觀察現象 | 產生氣泡 | 無明顯現象 | 產生氣泡的化學方程式 2HCl+K2CO3=2=KCl+CO2↑+H2O |
| (3)再取兩種溶液分別加入Ba(OH)2溶液,觀察現象 | 產生白色沉淀 | 有白色沉淀生成,同時以刺激性氣味氣體產生 | (NH4)2SO4與Ba(OH)2反應方程式 NH4)2SO4+Ba(OH)2═BaSO4↓+2H2O+2NH3↑ |
點評 本題主要考查氮肥、鉀肥的判斷和使用時的注意事項,難度稍大,須熟練運用酸堿鹽的性質進行解答;


 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:實驗探究題
| 實驗步驟 | 實驗現象 | 實驗結論 |
| ①取樣品加入過量氫氧化鈉溶液,振蕩 | 溶液顏色褪去,無藍色沉淀生成 | 猜想1錯誤 |
| ②向①溶液中加入過量的稀鹽酸,振蕩 | 溶液顏色為藍色 | 猜想2正確 |
| 實驗步驟 | 實驗現象 | 實驗結論 |
| 取樣,向樣品中加鐵片 | 產生大量氣泡且無紅色固體析出 | 猜想1錯誤 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
| 實驗步驟 | 實驗現象 | 實驗結論 |
| 步驟1:用潔凈干燥的玻璃棒蘸取溶液,粘在pH試紙上,與標準比色卡對照 | 試紙變色,溶液pH<7 | 溶液中有HCl |
| 步驟2:取少量反應后溶液于試管中,滴加碳酸鈉溶液振蕩 | 先產生氣泡,后產生沉淀 | 溶液中有CaCl2 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
 ”和“
”和“ ”分別表示氮原子和氧原子,如圖2是氮氣與氧氣在放電條件下發生反應的微觀模擬圖,請回答下列問題:
”分別表示氮原子和氧原子,如圖2是氮氣與氧氣在放電條件下發生反應的微觀模擬圖,請回答下列問題: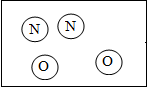 ,你的理論依據是反應前后原子種類、個數不變.
,你的理論依據是反應前后原子種類、個數不變.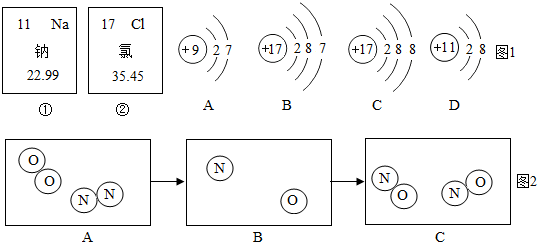
查看答案和解析>>
科目:初中化學 來源: 題型:推斷題
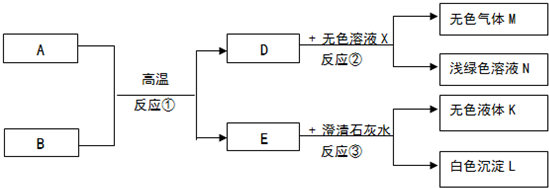
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 氧分子:O2 | B. | 鎂離子:$\stackrel{+2}{Mg}$ | C. | 2個氫原子:H2 | D. | 氧化鋁:AlO |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com