
| 實驗方案 | 實驗步驟 | 實驗現象 | 實驗結論 |
| 方案一 | 取樣,滴入適量的氯化鋇溶液 | 出現白色沉淀 | 硫酸過量 |
| 方案二 | 取樣,滴入幾滴紫色石蕊溶液 | 溶液顏色為紫色 | 酸堿恰好完全反應 |
| 方案三 | 取樣,滴入幾滴無色酚酞溶液 | 溶液變紅 | 氫氧化鈉過量,溶質為氫氧化鈉和硫酸鈉 |
分析 【實驗原理】反應物是氫氧化鈉和硫酸,生成物是硫酸鈉和水,用觀察法配平,寫出方程式;
【實驗評價】:
方案一:驗證硫酸根離子的存在,必須排除隱含在溶液中的硫酸根離子的存在;
方案二:根據紫色石蕊遇酸變紅,遇堿變藍,遇中性不變色,所以若觀察到溶液為紫色解答;
方案三:根據滴入幾滴無色酚酞溶液,酚酞變紅,只能說明溶液呈堿性,氫氧化鈉過量,溶質為氫氧化鈉和硫酸鈉解答;
①根據氫氧化鈉和硫酸恰好完全反應時,生成硫酸鈉和水,硫酸鈉和氯化鋇溶液也產生白色沉淀解答;
②根據紫色石蕊遇酸變紅進行解答.
解答 解:【實驗原理】氫氧化鈉和硫酸反應生成硫酸鈉和水,化學方程式是:2NaOH+H2SO4=Na2SO4+2H2O;
【實驗探究】方案二:取樣,滴入幾滴紫色石蕊溶液,紫色石蕊遇酸變紅,遇堿變藍,遇中性不變色,所以若觀察到溶液為紫色,則說明酸堿恰好完全反應;
方案三:取樣,滴入幾滴無色酚酞溶液,酚酞變紅,只能說明溶液呈堿性,氫氧化鈉過量,溶質為氫氧化鈉和硫酸鈉;
①硫酸根離子和鋇離子反應會生成硫酸鋇沉淀,所以方案一中,向溶液中滴加氯化鋇溶液,即使稀硫酸不過量,也會出現白色沉淀,因為溶液中有生成的硫酸鈉,存在硫酸根離子;
②紫色石蕊遇酸變紅色,所以實驗方案為:取樣,滴入幾滴紫色石蕊溶液,液變紅,溶液呈酸性,說明硫酸過量.
故答案為:【實驗原理】2NaOH+H2SO4=Na2SO4+2H2O;
【實驗探究】
| 實驗方案 | 實驗步驟 | 實驗現象 | 實驗結論 |
| 方案一 | 取樣,滴入適量的氯化鋇溶液 | 出現白色沉淀 | 硫酸過量 |
| 方案二 | 取樣,滴入幾滴紫色石蕊溶液 | 溶液顏色為紫色 | 酸堿恰好完全反應 |
| 方案三 | 取樣,滴入幾滴無色酚酞溶液 | 溶液變紅 | 氫氧化鈉過量,溶質為 氫氧化鈉和硫酸鈉 |
點評 本題主要是考查學生的綜合分析能力,不但要求學生具備有關化合物的基礎知識,而且要有實驗操作的經歷和分析、解決化學實驗問題的能力.


科目:初中化學 來源: 題型:選擇題
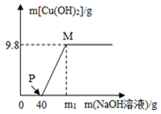 含CuCl2和HCl的100g混合溶液中,逐滴加入溶質質量分數為10%的NaOH溶液,參加反應的NaOH溶液質量與生成沉淀質量關系如圖,則下列說法不正確的是( )
含CuCl2和HCl的100g混合溶液中,逐滴加入溶質質量分數為10%的NaOH溶液,參加反應的NaOH溶液質量與生成沉淀質量關系如圖,則下列說法不正確的是( )| A. | m1的數值為80 | |
| B. | P點溶液中的溶質是氯化鈉和氯化銅 | |
| C. | M點溶液中的溶質是氯化鈉 | |
| D. | 整個反應過程中,溶液中氯離子個數不變 |
查看答案和解析>>
科目:初中化學 來源: 題型:推斷題
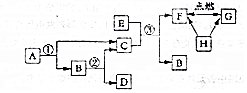 A-H是初中化學常見的物質,它們的相互轉化關系如圖所示.已知A、B組成元素相同且都是由兩種元素組成的,F、G、H三種物質含有同種非金屬元素,其中H是單質,G是易與血液中血紅蛋白結合的有毒氣體,請回答下列問題.(有些轉換關系,反應條件等略去).
A-H是初中化學常見的物質,它們的相互轉化關系如圖所示.已知A、B組成元素相同且都是由兩種元素組成的,F、G、H三種物質含有同種非金屬元素,其中H是單質,G是易與血液中血紅蛋白結合的有毒氣體,請回答下列問題.(有些轉換關系,反應條件等略去).查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
| 實驗編號 | 硫酸的質量分數 (均取20mL) | 鋅的形狀 (均取1g) | 氫氣的體積(mL) (均收集3分鐘) |
| ① | 20% | 鋅粒 | 31.7 |
| ② | 20% | 鋅片 | 50.9 |
| ③ | 30% | 鋅粒 | 61.7 |
| ④ | 30% | 鋅片 | 79.9 |
| 時段(均為1分鐘) | 第1分鐘 | 第2分鐘 | 第3分鐘 | 第4分鐘 | 第5分鐘 | 第6分鐘 |
| H2的體積 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |
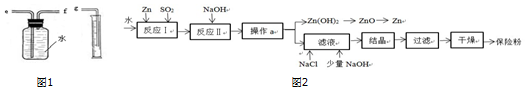
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 100 g水中溶解了10 g食鹽 | |
| B. | 100 g食鹽溶液中溶解了10 g食鹽 | |
| C. | 將10 g食鹽溶解于90 g水中所得的溶液 | |
| D. | 將食鹽、食鹽水按1:10的質量比配成的溶液 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com