
 某化學興趣小組為測定一種石灰石樣品中碳酸鈣的質量分數,進行如下實驗:
某化學興趣小組為測定一種石灰石樣品中碳酸鈣的質量分數,進行如下實驗:分析 (1)根據生成二氧化碳的質量與反應時間的關系圖,樣品充分反應后,二氧化碳質量不再隨反應時間延長而增加,此時所得二氧化碳質量為4.4g;由生成二氧化碳的質量,根據反應的化學方程式,可計算出樣品中碳酸鈣的質量,進而可計算出樣品中的碳酸鈣的質量分數;
(2)根據生成二氧化碳的質量與反應時間的關系圖中等質量的粉末狀石灰石與塊狀石灰石完全反應所消耗時間的關系,推斷影響該化學反應速率的因索.
(3)根據碳酸鈣的質量求出氧化鈣的質量即可.
解答 解:根據關系圖可知,樣品充分反應后,生成二氧化碳的質量為4.4g
設樣品中碳酸鈣的質量為x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
$\frac{100}{x}=\frac{44}{4.4g}$
x=10.0g
樣品中碳酸鈣的質量分數為$\frac{10.0g}{12.5g}$×100%=80%.
故填:4.4;80%;
(2)由生成二氧化碳的質量與反應時間的關系圖,可知等質量的粉末狀的碳酸鈣樣品反應的速度更快一些,則反應物間的接觸面積影響化學反應的速度;故填:反應物之間的接觸面積大小;
(3)解:設制得CaO的質量為x
CaCO3$\frac{\underline{\;高溫\;}}{\;}$CaO+CO2
100 56
125t×80% x
$\frac{100}{125t×80%}=\frac{56}{x}$
解得x=56t
則含有雜質的生石灰質量:56t+125t(1-80%)=81t
答:可制得含有雜質的生石灰質量為81t.
點評 本題難度不大,掌握根據化學方程式的計算即可正確解答本題,細致地分析生成二氧化碳的質量與反應時間的關系圖,確定生成二氧化碳氣體的質量是正確解答本題的關鍵


科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| 物質 | 雜質 | 除去雜質的方法 | |
| A | FeCl2溶液 | CuCl2 | 加入足量的鐵粉、過濾 |
| B | CO2氣體 | CO | 用點燃的方法徐去 |
| C | 鐵粉 | 銅粉 | 加過量HCl溶液、過濾 |
| D | Cu | C | 通入O2加熱點燃 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
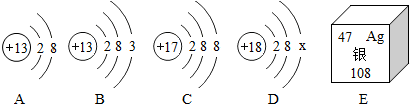
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
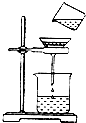 如圖是小明同學將渾濁的河水樣品倒入燒杯中,先加入明礬粉末攪拌溶解,靜置一會兒,進行過濾的操作.
如圖是小明同學將渾濁的河水樣品倒入燒杯中,先加入明礬粉末攪拌溶解,靜置一會兒,進行過濾的操作.查看答案和解析>>
科目:初中化學 來源: 題型:解答題
| 實驗過程 | 實驗現象 | 實驗結論 |
| 向盛有少量Fe2O3的試管中加入NaCl溶液,振蕩 | 固體不溶解 | Cl-不能使Fe2O3溶解,H2O不能使Fe2O3溶解,使氧化鐵溶解的是氫離子 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
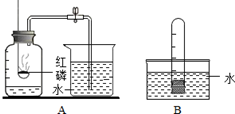 某校化學興趣小組就空氣中氧氣的含量進行實驗探究.
某校化學興趣小組就空氣中氧氣的含量進行實驗探究.查看答案和解析>>
科目:初中化學 來源: 題型:解答題
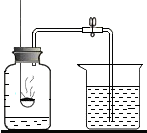
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com