
 酸、堿、鹽是有廣泛用途的重要化合物.某化學活動小組的同學圍繞這幾類化合物進行了一系列的探究活動.
酸、堿、鹽是有廣泛用途的重要化合物.某化學活動小組的同學圍繞這幾類化合物進行了一系列的探究活動.| 實驗目的 | 實驗操作 | 現象 | 結論或化學方程式 |
除去碳酸鈉 | 取少量該固體樣品溶于水配成溶液,滴加適量的氯化鋇溶液,充分反應后過濾 | 有白色沉淀生成 | 有關反應的化學方程式為Na2CO3+BaCl2=BaCO3↓+2NaCl |
| 檢驗是否含有氫氧化鈉 | 在濾液中滴加酚酞溶液 | 溶液變紅 | 該樣品中含有氫氧化鈉 |
分析 (1)根據溶液稀釋前后溶質的質量不變來求算出需要加入水的質量,根據濃硫酸的密度和水的密度比較及濃硫酸溶解放出大量的熱來分析不能將水注入濃硫酸的原因;利用碳酸鹽的性質,檢驗碳酸鈉的存在,證明氫氧化鈉變質;
(2)選擇合適的試液檢驗氫氧化鈉是否存在;碳酸鈉能與氯化鋇反應形成白色沉淀,可以判斷出反應產生現象,然后利用氫氧化鈉能使酚酞變紅的性質,再向反應后溶液中滴加酚酞試液,觀察溶液顏色,以確定溶液的組成,從而判斷氫氧化鈉變質情況
解答 解:(1)根據溶液稀釋前后溶質的質量不變,設需加入水的質量為x,則:
10g×98%=(10g+x)×20%
解得:x=39g,
由于濃硫酸的密度比水的大,并且濃硫酸在溶解的時候要放出大量的熱,放出的熱足以使水沸騰,而引起酸液的迸濺,所以為了防止酸液迸濺引起危險,而應該將濃硫酸慢慢注入水中,并不斷攪拌;
故填:39;濃硫酸的密度比水的大,并且濃硫酸在溶解的時候要放出大量的熱,放出的熱足以使水沸騰,而引起酸液的迸濺,所以為了防止酸液迸濺引起危險,而應該將濃硫酸慢慢注入水中,并不斷攪拌;
(2)①碳酸鹽可以與酸反應放出能使澄清石灰水變渾濁的二氧化碳氣體;所以無色溶液可能是:鹽酸;故填:鹽酸;
②氯化鋇溶液與碳酸鈉溶液反應生成碳酸鋇沉淀和氯化鈉,所以根據題中的實驗結論可以知道能觀察到的現象為:有白色沉淀生成,有關反應的化學方程式為:Na2CO3+BaCl2=BaCO3↓+2NaCl,而氯化鈉、氯化鋇溶液都呈中性;故在反應后的溶液中滴入酚酞,溶液變紅色,則一定是氫氧化鈉溶液使酚酞變紅,所以氫氧化鈉沒有完全變質;
故填:
| 實驗目的 | 實驗操作 | 現象 | 結論或化學方程式 |
| 除去碳酸鈉 | 取少量該固體樣品溶于水配成溶液,滴加適量的 氯化鋇溶液,充分反應后過濾 | 有白色沉淀生成 | 有關反應的化學方程式為 Na2CO3+BaCl2=BaCO3↓+2NaCl |
| 檢驗是否含有氫氧化鈉 | 在濾液中滴加酚酞溶液 | 溶液變紅 | 該樣品中含有氫氧化鈉 |
點評 檢驗氫氧化鈉與碳酸鈉的混合物時,可先把碳酸鈉變成沉淀并且不生成影響氫氧化鈉檢驗的堿性物質,然后使用酚酞檢驗氫氧化鈉.


科目:初中化學 來源: 題型:選擇題
| A. | 催化劑都能加快化學反應速率 | |
| B. | 含氧元素的化合物都是氧化物 | |
| C. | 物質發生化學變化時都伴隨著能量的變化 | |
| D. | 只有燃燒的化學反應才能放出熱量 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
 下表是a、b二種物質在不同溫度時的溶解度,請根據表中數據回答:
下表是a、b二種物質在不同溫度時的溶解度,請根據表中數據回答:| 溫度/℃ | 0 | 20 | 30 | 40 | 60 | |
| 溶解度/g | 物質a | 13.3 | 31.6 | 45.8 | 63.9 | 110 |
| 物質b | 21.4 | 9.84 | 7.24 | 5.63 | 3.87 | |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
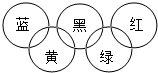 奧運會會標是五環旗,假定奧運五環旗中的一環表示一種物質,相連環物質間一定條件下能發生常見反應,不相連環物質間不能發生反應,且四種反應中必須包含化合反應、置換反應及復分解反應,適合的一組是( )
奧運會會標是五環旗,假定奧運五環旗中的一環表示一種物質,相連環物質間一定條件下能發生常見反應,不相連環物質間不能發生反應,且四種反應中必須包含化合反應、置換反應及復分解反應,適合的一組是( )| 藍 | 黃 | 黑 | 綠 | 紅 | |
| A | SiO2 | NaOH溶液 | CuSO4溶液 | Ag | O2 |
| B | O2 | Fe | 稀H2SO4 | NaOH溶液 | CO2 |
| C | O2 | NH3 | 稀H2SO4 | NaOH溶液 | Al(OH)3 |
| D | Mg | Al | CO2 | Fe2O3 | KOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
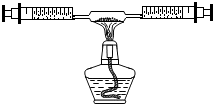 某課外活動小組在學習了書本“空氣中氧氣含量的測定”實驗,知道P2O5不能隨便排放在空氣中,否則會對空氣造成污染,所以對該實驗進行了改進:
某課外活動小組在學習了書本“空氣中氧氣含量的測定”實驗,知道P2O5不能隨便排放在空氣中,否則會對空氣造成污染,所以對該實驗進行了改進:查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com