
分析 根據反應物、生成物、鳳于九天及其質量守恒定律可以書寫反應的化學方程式;
化合物中元素化合價代數和為零.
解答 解:(1)實驗室用過氧化氫溶液制取氧氣的化學方程式為:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)燈泡里放極少量紅磷延長使用壽命,是因為紅磷能和氧氣反應生成五氧化二磷,反應的化學方程式為:4P+5O2$\frac{\underline{\;點燃\;}}{\;}$2P2O5.
故填:4P+5O2$\frac{\underline{\;點燃\;}}{\;}$2P2O5.
(3)實驗室用白色固體氯酸鉀和黑色固體二氧化錳混合加熱制取氧氣的化學方程式為:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,該反應的基本類型是分解反應.
故填:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;分解反應.
(4)氫氧化鈉和硫酸銅反應生成氫氧化銅沉淀和硫酸鈉,反應的化學方程式為:2NaOH+CuSO4═Na2SO4+Cu(OH)2↓.
故填:2NaOH+CuSO4═Na2SO4+Cu(OH)2↓.
(5)硝酸銨[NH4NO3]在撞擊時迅速分解產生一氧化氮[N2O]氣體和水,反應的化學方程式為:NH4NO3$\frac{\underline{\;撞擊\;}}{\;}$N2O+2H2O,該反應中氮元素的化合價分別為(從前向后)-3、+5、+1.
故填:NH4NO3$\frac{\underline{\;撞擊\;}}{\;}$N2O+2H2O,-3、+5、+1.
(6)加熱高錳酸鉀制取氧氣的化學方程式為:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
故填:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(7)氫氣還原氧化銅的化學方程式為:CuO+H2$\frac{\underline{\;高溫\;}}{\;}$Cu+H2O.
故填:CuO+H2$\frac{\underline{\;高溫\;}}{\;}$Cu+H2O.
(8)鐵釘放入藍色硫酸銅溶液中時,反應的化學方程式為:Fe+CuSO4═FeSO4+Cu,過程中能夠觀察到:溶液顏色變成淺綠色,鐵釘表面附著了一層紅色物質.
故填:Fe+CuSO4═FeSO4+Cu,溶液顏色變成淺綠色,鐵釘表面附著了一層紅色物質.
點評 書寫化學方程式要注意四步:一是反應物和生成物的化學式要正確;二是要遵循質量守恒定律,即配平;三是要有必要的條件;四是看是否需要“↑”或“↓”.


 小學課時特訓系列答案
小學課時特訓系列答案科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
 西瓜可清熱解暑、除煩止渴,如圖列出了西瓜的營養成分.
西瓜可清熱解暑、除煩止渴,如圖列出了西瓜的營養成分.查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 50g | B. | 10g | C. | 15g | D. | 20g |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
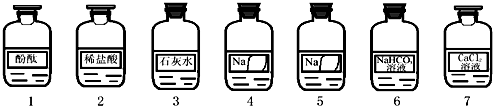
| 實驗操作 | 實驗現象 | 實驗結論 |
| ①取少量4號溶液于試管中,加入足量CaCl2溶液②向上層清液中滴加無色酚酞試液 | ①有白色沉淀生成②溶液由無色變成紅色 | 4號溶液是部分變質的NaOH溶液. |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com