
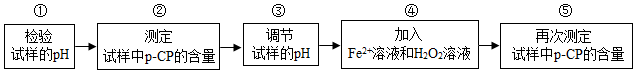
| 實驗編號 | 溫度/℃ | pH | 測得p-CP的含量隨時間變化的關系圖 |
| a | 25 | 10 | 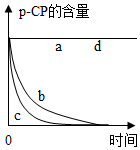 |
| b | 25 | 3 | |
| c | 40 | 3 | |
| d | 40 | 10 |
分析 (1)根據pH大于7溶液顯堿性,欲使試樣的pH小于7,應加入酸性物質解答;
(2)根據反應原理寫出反應的化學方程式解答;
(3)根據通入氧氣,測得p-CP含量沒有變化解答;
(4)對比實驗的基本思想是控制變量法,可以在溫度相同時,變化濃度,或者在濃度相等時,變化溫度;
(5)根據實驗bc的數據來回答;
(6)根據實驗數據內容進行分析;
(7)根據實驗數據內容進行分析.
解答 解;
(1)pH大于7溶液顯堿性,欲使試樣的pH小于7,應加入酸性物質,NaOH溶液顯堿性,稀HCl 呈酸性,NaCl溶液和水呈中性,故選b;
(2)步驟④有多個反應發生,其中產生氧氣的化學方程式為:2H2O2═2H2O+O2↑.
(3)取樣,加入MnO2和H2O2溶液,測得p-CP含量沒有變化(或取樣,通入氧氣,測得p-CP含量沒有變化),說明試樣中p-CP含量的減少與產生氧氣的反應無關;
(4)對比實驗的基本思想是控制變量法,為探究pH對Fe2+、H2O2處理p-CP的反應快慢影響,可比較實驗a和b或c或d.從兩組實驗對比中得到的結論是
pH越小,Fe2+、H2O2處理p-CP的反應速率越快;
(5)比較實驗b和c,可以得到的結論是溫度越高,Fe2+、H2O2處理p-CP的反應速率越快;
(6)實驗a和d說明pH=10時,Fe2+、H2O2處理p-CP的反應不發生;
(7)根據實驗數據內容可以看出,將所取樣品迅速加入到一定量的NaOH溶液中,使pH為10,就可使樣品中的降解反應立即停止下來.
答案:(化學方程式(3分),第(3)小題(2分),余每空1分)
(1)b;
(2)2H2O2═2H2O+O2↑;
(3)取樣,加入MnO2和H2O2溶液,測得p-CP含量沒有變化(或取樣,通入氧氣,測得p-CP含量沒有變化);
(4)ab;cd;pH越小,Fe2+、H2O2處理p-CP的反應速率越快;
(5)溫度越高,Fe2+、H2O2處理p-CP的反應速率越快;
(6)pH=10時,Fe2+、H2O2處理p-CP的反應不發生;
(7)往樣品中加入氫氧化鈉使溶液的pH等于10(或快速降溫).
點評 本題考查學生化學平衡狀態以及化學反應速率知識,要求學生具有分析和解決問題的能力,難度較大.


 優加精卷系列答案
優加精卷系列答案科目:初中化學 來源: 題型:選擇題
| A. | 原子是最小的粒子,不可再分 | B. | 離子不能直接構成物質 | ||
| C. | “花香四溢”是因為分子在不斷運動 | D. | 空氣是由空氣分子構成的 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 氧化汞受熱分解 HgO2 $\frac{\underline{\;\;△\;\;}}{\;}$Hg+O2↑ | |
| B. | 紅磷在氧氣中燃燒 P+O2$\frac{\underline{\;點燃\;}}{\;}$P2O5 | |
| C. | 鐵絲在氧氣中燃燒 3Fe+2O2 $\frac{\underline{\;點燃\;}}{\;}$Fe3O4 | |
| D. | 電解水 2H2O═2H2↑+O2↑ |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
 同學們正在化學實驗室完成“實驗活動6--酸、堿的化學性質”
同學們正在化學實驗室完成“實驗活動6--酸、堿的化學性質”查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
科目:初中化學 來源: 題型:填空題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com