
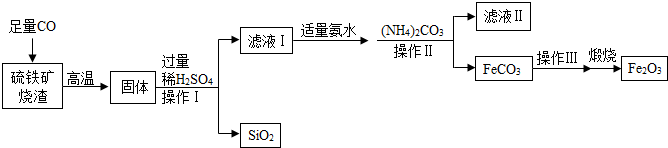
分析 根據已有的物質的性質進行分析解答,過濾是分離不溶性固體和液體的方法,根據過濾用到的玻璃儀器進行解答;一氧化碳能將氧化鐵還原為鐵,將氧化亞鐵還原為鐵,故硫鐵礦高溫通入一氧化碳得到的固體中主要含有的是鐵,稀硫酸能與鐵反應生成硫酸亞鐵和氫氣,氨水呈堿性,能夠與酸反應;根據反應物和生成物確定反應的化學方程式,據此解答.
解答 解:(1)據圖可以看出,經過操作Ⅰ、操作Ⅱ得到的是濾液和固體,故是過濾操作,用到的玻璃儀器有玻璃棒、燒杯、漏斗.
(2)一氧化碳與氧化鐵在高溫的條件下生成鐵和二氧化碳,配平即可,故其化學方程式為:3CO+Fe2O3$\frac{\underline{\;高溫\;}}{\;}$2Fe+3CO2.
(3)一氧化碳能將氧化鐵還原為鐵,將氧化亞鐵還原為鐵,硫鐵礦高溫通入一氧化碳得到的固體中主要含有的是鐵,稀硫酸能與鐵反應生成硫酸亞鐵和氫氣,故含有亞鐵離子,則濾液Ⅰ中主要的陽離子是亞鐵離子和氫離子,故濾液Ⅰ的顏色是淺綠色,該溶液的pH<7.
(3)由于硫酸過量,溶液呈酸性,氨水呈堿性,加適量氨水能將溶液調節為中性,故若在濾液Ⅰ中不先加入氨水,而是直接加入(NH4)2CO3,會反應生成二氧化碳,則開始出現的現象是有氣泡生成.
(4)碳酸銨能與硫酸亞鐵反應生成碳酸亞鐵和硫酸銨,故濾液Ⅱ中可回收的產品是硫酸銨,故其化學式為:(NH4)2SO4.
(6)為了提高得到的Fe2O3的純度,操作Ⅲ應該是洗滌干燥.
故答案為:
(1)漏斗.(2)3CO+Fe2O3$\frac{\underline{\;高溫\;}}{\;}$2Fe+3CO2.(3)淺綠色,<;
(4)有氣泡生成.(5)NH4)2SO4.(6)洗滌干燥
點評 本題考查的是常見的物質制備和分離的知識,完成此題,可以依據已有的知識進行,要熟練掌握有關物質的化學性質,以便靈活應用.


科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
| 物質 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| 溶解度 | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
| 實驗步驟 | 實驗現象 | 實驗結論 |
| ①取少量濾液于試管中,滴加稀鹽酸 | 產生無色無味氣體 | 說明濾液中含有的物質是NaHCO3 |
| ②另取少量濾液于試管中,滴加足量稀HNO3后,再滴加AgNO3溶液 | 產生白色沉淀 | 證明濾液中含有NaCl |
| 第一組 | 第二組 | 第三組 | 第四組 | |
| CaCl2溶液的質量(克) | 100 | 200 | 300 | 400 |
| 產生沉淀的質量(克) | 8 | 16 | 20 | 20 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| 選項 | 實驗操作 | 現象 | 結論 |
| A | 向氫氧化鈉固體中加入水 | 氫氧化鈉固體消失 | 氫氧化鈉與水發生了化學反應 |
| B | 向含有硝酸銀、硝酸銅、硝酸鋅的混合溶液中加入一定量的鐵粉,充分反應后過濾,向濾渣中滴加稀鹽酸 | 有氣泡產生 | 濾液中一定含有Zn2+、Fe3+、可能有Cu2+ |
| C | 向溶質的質量分數為5%的過氧化氫溶液中加入少量氧化銅 | 有大量氣泡產生 | 氧化銅起催化作用 |
| D | 向鹽酸和氫氧化鈣反應后的溶液中滴加酚酞 | 無明顯現象 | 說明鹽酸和氫氧化鈣恰好反應 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
| 方案 | 實驗操作 | 實驗現象 | 實驗結論 |
| 方案一 | 往溶液中加鋅或CaCO3 | 有氣泡產生 | 溶液中有HCl |
| 方案二 | 往溶液中滴加AgNO3溶液 | 產生白色沉淀 | 溶液中有HCl |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 用甲醛溶液浸泡海鮮品 | B. | 用工業鹽腌制咸魚臘肉 | ||
| C. | 牛奶經發酵后得到酸奶 | D. | 用聚氯乙烯塑料袋包裝食品 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題

| 反應前(g) | 反應后(g) | |
| B | 100 | 105.4 |
| C | 150 | 163.2 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 氫氧化鈉、燒堿、NaOH | B. | 碳酸氫鈉、小蘇打、NaHCO3 | ||
| C. | 氧化鈣、石灰石、CaO | D. | 汞、水銀、Hg |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com