
 某化學興趣小組為了測定某石灰石樣品中碳酸鈣的質量分數,取用15g石灰石樣品,把100.0g稀鹽酸平均分4次加入樣品中(樣品中的雜質既不與鹽酸反應,也不溶解于水),每次充分反應后實驗數據如下,請計算:
某化學興趣小組為了測定某石灰石樣品中碳酸鈣的質量分數,取用15g石灰石樣品,把100.0g稀鹽酸平均分4次加入樣品中(樣品中的雜質既不與鹽酸反應,也不溶解于水),每次充分反應后實驗數據如下,請計算:| 實驗次數 | 1 | 2 | 3 | 4 |
| 稀鹽酸的累計加入量/g | 25.0 | 50.0 | 75.0 | 100.0 |
| 產生CO2的總質量/g | 2.2 | 4.4 | 5.5 | M |
分析 (1)根據第二次和第一次比較,鹽酸和二氧化碳都是第一次的2倍,但是第三次,鹽酸是第一次的三倍,而二氧化碳不是第一次的三倍,說明第三次碳酸鈣已經完全反應,所以M的值是5.5克;
(2)根據二氧化碳的質量可以計算參加反應的碳酸鈣的質量,然后計算質量分數;
(3)根據生成二氧化碳的質量是逐漸增加的,然后計算恰好完全反應的鹽酸的質量,然后進行作圖.
解答 解:(1)通過第二次和第一次比較,鹽酸和二氧化碳都是第一次的2倍,但是第三次,鹽酸是第一次的三倍,而二氧化碳不是第一次的三倍,說明第三次碳酸鈣已經完全反應,所以M的值是5.5克;
(2)設參加反應的碳酸鈣質量為x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 5.5g
$\frac{100}{x}$=$\frac{73}{y}$=$\frac{44}{5.5g}$
x=12.5g
所以碳酸鈣的質量分數為:$\frac{12.5g}{15g}$×100%=83.3%;
(3)稀鹽酸的質量分數為y
CaCO3+2HCl═CaCl2+H2O+CO2↑
73 44
y×25g 2.2g
$\frac{73}{y×25g}$=$\frac{44}{2.2g}$
y=0.146=14.6%
所以參加反應的鹽酸質量為z
CaCO3+2HCl═CaCl2+H2O+CO2↑
73 44
z×14.6% 5.5g
$\frac{73}{z×14.6%}$=$\frac{44}{5.5g}$
z=62.5g
所以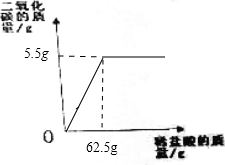
故答案為:(1)5.5;
(2)83.3%;
(3)
點評 綜合分析數據,找出加放稀鹽酸生成氣體之間的質量關系為本題的解題關鍵.根據數據利用質量守恒定律求出四次實驗分別產生的二氧化碳的質量,進行分析計算出恰好完全反應時實際發生反應的稀鹽酸的質量.


 名校課堂系列答案
名校課堂系列答案科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 屬于氧化物 | |
| B. | 一個分子中共有48個原子 | |
| C. | 興奮劑中氫元素的質量分數最大 | |
| D. | 是由碳、氫、氧三種元素組成的混合物 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 鋁是人類最早利用的金屬材料 | B. | 銅是目前世界年產量最高的金屬 | ||
| C. | 金屬在通常情況下都是固體 | D. | 日常使用的金屬材料大多數是合金 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com