
分析 已知“甲、乙、丙3種常見物質,由氫、氧、氯、鈣、鐵5種元素中的2~3種組成”,則:
(1)根據“甲俗稱熟石灰”,寫出化學式;
(2)根據“乙溶液有刺激性氣味,與固體丙反應后溶液變黃”,推測乙為稀鹽酸,丙為氧化鐵,進行書寫化學方程式;
(3)根據碳酸鈉的溶液為堿性;氫氧化鈣與碳酸鈉溶液反應生成碳酸鈣沉淀和氫氧化鈉;氫氧化鈉與稀鹽酸反應生成氯化鈉和水,碳酸鈣與稀鹽酸反應生成氯化鈣和水和二氧化碳,因為“加入過量的乙溶液”,進行分析.
解答 解:已知“甲、乙、丙3種常見物質,由氫、氧、氯、鈣、鐵5種元素中的2~3種組成”,則:
(1)因為甲俗稱熟石灰,為氫氧化鈣,則其化學式為Ca(OH)2.
(2)根據“乙溶液有刺激性氣味,與固體丙反應后溶液變黃”,推測乙為稀鹽酸,丙為氧化鐵,則該反應的化學方程式Fe2O3+6HCl═2FeCl3+3H2O.
(3)根據“試管中盛有某紅色溶液,滴加甲溶液,溶液變渾濁;再加入過量的乙溶液,觀察到產
生無色氣泡,溶液又變澄清,且由紅色變為無色”,則推測:
①因為碳酸鈉的溶液為堿性,故試管內最初盛放溶液的溶質是碳酸鈉和酚酞.
②因為氫氧化鈣與碳酸鈉溶液反應生成碳酸鈣沉淀和氫氧化鈉,故用化學方程式表示溶液變渾濁的原因為Ca(OH)2+Na2CO3═2NaOH+CaCO3↓.
③因為氫氧化鈉與稀鹽酸反應生成氯化鈉和水,碳酸鈣與稀鹽酸反應生成氯化鈣和水和二氧化碳,因為“加入過量的乙溶液”,故最終所得溶液中溶質的組成為HCl、NaCl、CaCl2.
故答案為:
(1)Ca(OH)2;(2)Fe2O3+6HCl═2FeCl3+3H2O;
(3)①碳酸鈉和酚酞;②Ca(OH)2+Na2CO3═2NaOH+CaCO3↓;③HCl、NaCl、CaCl2.
點評 本題的推斷由組成物質的元素做為限定條件,因此,熟悉常見物質的組成、性質及變化規律對該題中所涉及物質的推斷就至關重要了.


科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
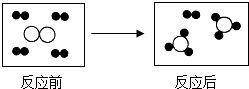
| A. | 反應后生成兩種物質 | |
| B. | 參加反應各物質的分子個數比為1:4 | |
| C. | 反應前后原子的種類沒有改變 | |
| D. | 該反應的基本類型是置換反應 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
| 溫度/℃ | 10 | 20 | 30 | 40 | |
| 溶解度 g/100gH2O | 氯化鈉 | 35.8 | 36.0 | 36.3 | 36.6 |
| 碳酸鈉 | 12.2 | 21.8 | 39.7 | 53.2 | |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com