
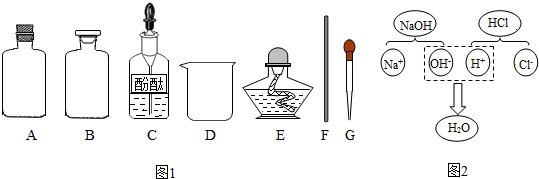
| 實驗方案 | 實驗步驟 | 現 象 | 結 論 |
| ① | 取樣,加入適量的AgNO3溶液 | 出現白色沉淀 | 稀鹽酸過量 |
| ② | 取樣,加入幾滴紫色石蕊試液 | 溶液變紅 | 稀鹽酸過量 |
| ③ | 取樣,加入少量鐵粉 | 黑色固體溶解,產生氣泡,溶液變淺綠色 | 稀鹽酸過量 |
分析 【方案1】根據對溶液稀釋也可以改變溶液的pH值進行分析;
【方案2】根據氫氧化鈉具有腐蝕性,瓶塞應該選用橡膠塞進行分析;
【思考拓展】(1)根據氫氧化鈉固體溶于水放熱,氫氧化鈉會與硫酸銅反應生成藍色的氫氧化銅沉淀進行分析;
(2)根據鐵會與鹽酸反應生成氯化亞鐵和氫氣進行分析;
根據氯離子和銀離子反應都會生成氯化銀沉淀進行分析;
根據碳酸鹽或活潑金屬會與酸反應生成氣體,金屬氧化物也會與酸反應生成鹽和水進行分析;
(3)根據酸堿中和反應的實質是氫離子和氫氧根離子反應生成水進行分析.
解答 解:【方案1】對溶液稀釋也可以改變溶液的pH值,堿性溶液稀釋堿性減弱,pH值也會減小,所以他們的結論不正確,理由是:氫氧化鈉溶液中加水稀釋pH也會減小;
【方案2】氫氧化鈉具有腐蝕性,會與二氧化硅生成硅酸鈉,使瓶塞和瓶口粘在一起,所以瓶塞應該選用橡膠塞,故選:A;
【思考拓展】(1)氫氧化鈉固體溶于水放熱,氫氧化鈉會與硫酸銅反應生成藍色的氫氧化銅沉淀,所以檢驗白色固體不是氫氧化鈉的方法是:取少量水將其溶解,沒有熱量現象或取少量水將其溶解加入CuSO4溶液,無藍色沉淀;
(2)鐵會與鹽酸反應生成氯化亞鐵和氫氣,所以實驗現象是:黑色固體溶解,產生氣泡,溶液變淺綠色,化學方程式為:Fe+2HCl=FeCl2+H2↑;
氯離子和銀離子反應都會生成氯化銀沉淀,所以上述設計方案中,不正確的是①,理由是:反應生成的NaCl也能與AgNO3反應生成白色沉淀,不能證明溶液中含有鹽酸;
碳酸鹽或活潑金屬會與酸反應生成氣體,所以確定稀鹽酸是否過量,選用的試劑是:Na2CO3溶液或鋅等;
(3)鐵離子、銅離子在溶液中會顯示一定的顏色,所以Cu(OH)2與鹽酸反應就有明顯的實驗現象;
酸堿中和反應的實質是氫離子和氫氧根離子反應生成水.
故答案為:【探究Ⅰ】
【方案1】不正確,理由:滴加的鹽酸中含水,加入后使NaOH溶液變稀,同樣會使溶液堿性減弱,pH減小;【方案2】①A;
【思考拓展】(1)取②中溶液,向其中滴加硫酸銅溶液,無藍色沉淀;
(2)黑色固體溶解,產生氣泡,溶液變淺綠色;Fe+2HCl=FeCl2+H2↑;
①,氯化鈉溶液中也含Cl-,與硝酸銀溶液反應也會生成白色沉淀;加入鋅或碳酸鈉溶液;
【探究Ⅱ】H+、OH-.
點評 合理設計實驗,科學地進行實驗、分析實驗,是得出正確實驗結論的前提,因此要學會設計實驗、進行實驗、分析實驗,為學好化學知識奠定基礎.


科目:初中化學 來源: 題型:選擇題
 ”表示氧原子,下列模型能表示“超臨界水”分子的是( )
”表示氧原子,下列模型能表示“超臨界水”分子的是( )| A. | 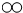 | B. |  | C. |  | D. | 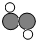 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| 物 質 | X | Y | Z | W |
| 反應前的質量/g | 10 | m | 8 | 7 |
| 反應后的質量/g | 2 | 3 | 30 | 25 |
| A. | 若W為水,則X或Y必定為酸或堿 | |
| B. | 若X為化合物,Y為單質,則該反應一定為置換反應 | |
| C. | m的數值為32 | |
| D. | 參加反應的X與Y的質量比為1:4 |
查看答案和解析>>
科目:初中化學 來源: 題型:推斷題

查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
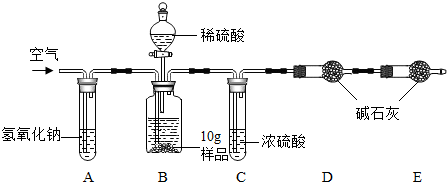
查看答案和解析>>
科目:初中化學 來源: 題型:推斷題
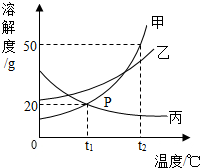 甲、乙、丙三種不含結晶水的固體物質的溶解度曲線如圖所示,請回答下列問題:
甲、乙、丙三種不含結晶水的固體物質的溶解度曲線如圖所示,請回答下列問題:查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com