
| 反 應 物 | 化 學 方 程 式 | |
| 1 | 氫氧化鈣與鹽酸反應 | Ca(OH)2+2HCl=CaCl2+2H2O |
| 2 | 氫氧化鈉與稀硫酸反應 | 2NaOH+H2SO4=Na2SO4+2H2O |
| 3 | 用胃舒平(氫氧化鋁)中和過多的胃酸 | Al(OH)3+3HCl=AlCl3+3H2O |
| 4 | 用熟石灰中和含有硫酸的污水 | Ca(OH)2+H2SO4=CaSO4+2H2O |
| 5 | 碳酸氫鈉與稀鹽酸反應 | NaHCO3+HCl=NaCl+H2O+CO2↑ |
| 6 | 用稀鹽酸除鐵銹 | 6HCl+Fe2O3=2FeCl3+3H2O |
| 7 | 用稀硫酸除鐵銹 | 3H2SO4+Fe2O3=Fe2(SO4)3+3H2O |
| 8 | 用碳酸鈉制取氫氧化鈉 | Ca(OH)2+Na2CO3=CaCO3↓+2NaOH |
| 9 | 氯化鋇與稀硫酸反應 | BaCl2+H2SO4=BaSO4↓+2HCl |
| 10 | 氫氧化鈉與三氧化硫反應 | 2NaOH+SO3=Na2SO4+H2O |
分析 1根據氫氧化鈣和鹽酸反應生成氯化鈣和水進行分析;
2根據氫氧化鈉和硫酸反應生成硫酸鈉和水進行分析;
3根據氫氧化鋁和鹽酸反應生成氯化鋁和水進行分析;
4根據氫氧化鈣和硫酸反應生成硫酸鈣和水進行分析;
5根據碳酸氫鈉和鹽酸反應生成氯化鈉、水和二氧化碳進行分析;
6根據鹽酸和氧化鐵反應生成氯化鐵和水進行分析;
7根據硫酸和氧化鐵反應生成硫酸鐵和水進行分析;
8根據碳酸鈉和氫氧化鈣反應生成碳酸鈣沉淀和氫氧化鈉進行分析;
9根據氯化鋇和硫酸反應生成硫酸鋇沉淀和鹽酸進行分析;
10根據氫氧化鈉和三氧化硫反應生成硫酸鈉和水進行分析.
解答 解:1氫氧化鈣和鹽酸反應生成氯化鈣和水,化學方程式為:Ca(OH)2+2HCl=CaCl2+2H2O;
2氫氧化鈉和硫酸反應生成硫酸鈉和水進,化學方程式為:2NaOH+H2SO4=Na2SO4+2H2O;
3氫氧化鋁和鹽酸反應生成氯化鋁和水進,化學方程式為:Al(OH)3+3HCl=AlCl3+3H2O;
4氫氧化鈣和硫酸反應生成硫酸鈣和水,化學方程式為:Ca(OH)2+H2SO4=CaSO4+2H2O;
5碳酸氫鈉和鹽酸反應生成氯化鈉、水和二氧化碳進,化學方程式為:NaHCO3+HCl=NaCl+H2O+CO2↑;
6鹽酸和氧化鐵反應生成氯化鐵和水,化學方程式為:6HCl+Fe2O3=2FeCl3+3H2O;
7硫酸和氧化鐵反應生成硫酸鐵和水,化學方程式為:3H2SO4+Fe2O3=Fe2(SO4)3+3H2O;
8碳酸鈉和氫氧化鈣反應生成碳酸鈣沉淀和氫氧化鈉,化學方程式為:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
9氯化鋇和硫酸反應生成硫酸鋇沉淀和鹽酸,化學方程式為:BaCl2+H2SO4=BaSO4↓+2HCl;
10氫氧化鈉和三氧化硫反應生成硫酸鈉和水,化學方程式為:2NaOH+SO3=Na2SO4+H2O.
故答案為:1、Ca(OH)2+2HCl=CaCl2+2H2O;
2、2NaOH+H2SO4=Na2SO4+2H2O;
3、Al(OH)3+3HCl=AlCl3+3H2O;
4、Ca(OH)2+H2SO4=CaSO4+2H2O;
5、NaHCO3+HCl=NaCl+H2O+CO2↑;
6、6HCl+Fe2O3=2FeCl3+3H2O;
7、3H2SO4+Fe2O3=Fe2(SO4)3+3H2O;
8、Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
9、BaCl2+H2SO4=BaSO4↓+2HCl;
10、2NaOH+SO3=Na2SO4+H2O.
點評 在解此類題時,首先分析應用的原理,然后找出反應物、生成物,最后結合方程式的書寫規則書寫方程式.


科目:初中化學 來源: 題型:解答題
 鈣是維持人體正常功能所必需的元素.如圖所示為“迪巧”鈣片說明書的一部分.取5片鈣片,放入 有50g稀鹽酸的燒杯中,其中碳酸鈣跟鹽酸恰好完全反應(其它成分與鹽酸不反應).燒杯內物質質量變為57.8g.試計算:
鈣是維持人體正常功能所必需的元素.如圖所示為“迪巧”鈣片說明書的一部分.取5片鈣片,放入 有50g稀鹽酸的燒杯中,其中碳酸鈣跟鹽酸恰好完全反應(其它成分與鹽酸不反應).燒杯內物質質量變為57.8g.試計算:查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
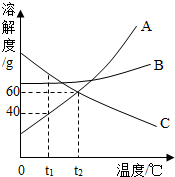 (1)如圖是A、B、C三種固體物質的溶解度曲線圖,請結合圖示回答下列問題:
(1)如圖是A、B、C三種固體物質的溶解度曲線圖,請結合圖示回答下列問題:查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
 一定質量的鎂條在氧氣中完全燃燒后生成氧化鎂.固體質量隨時間的變化關系如圖所示.下列說法不正確的是( )
一定質量的鎂條在氧氣中完全燃燒后生成氧化鎂.固體質量隨時間的變化關系如圖所示.下列說法不正確的是( )| A. | 生成MgO的質量:m2g | |
| B. | 參加反應的Mg的質量:m1 g | |
| C. | 參加反應的O2的質量:(m2-m1)g | |
| D. | 參加反應的鎂和氧氣的質量比:m1:(m2-m1)=3:1 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
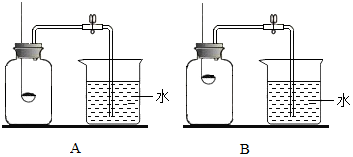
| 組 別 | 1 | 2 | 3 | 4 | 5 | 6 |
| 進入集氣瓶中水的體積(mL) | 20 | 21 | 19 | 20 | 22 | 18 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com