
| 編 號 | 第1次 | 第2次 | 第3次 |
| 所取固體樣品的質量/g | 7 | 5 | 5 |
| 加入氯化鈣溶液的質量/g | 50 | 50 | 75 |
| 反應后生成沉淀的質量/g | 4 | 4 | 4 |
分析 (1)第一次和第二次所取的固體質量不等,但是所取氯化鈣溶液的質量相等,但是生成的沉淀的質量相等,所以可以判斷第一次所取固體有剩余,即5g固樣品反應后能生成沉淀的質量為4g,第2次和第3次所取的固體樣品相等,但是所取的氯化鈣溶液的質量不等,但是生成的沉淀的質量相等,所以可以判斷第3次所取的氯化鈣溶液有剩余,即說明50g氯化鈣溶液反應后只能得到4g沉淀,綜上分析可以知道第二次是所給的物質恰好完全反應,所以可以根據第2次反應的數據進行解答;根據生成沉淀的質量可以計算出碳酸鈉的質量;
(2)根據生成沉淀的質量可以計算出氯化鈣的質量,進而計算出氯化鈣溶液的質量分數;
(3)根據(1)中所求碳酸鈉的質量可以計算出雜質中氯化鈉的質量,可以據此解答該題.
解答 解:(1)由題意分析李明的實驗數據可知,第一次和第二次所取的固體質量不等,但是所取氯化鈣溶液的質量相等,但是生成的沉淀的質量相等,所以可以判斷第一次所取固體有剩余,即5g固樣品反應后能生成沉淀的質量為4g,第2次和第3次所取的固體樣品相等,但是所取的氯化鈣溶液的質量不等,但是生成的沉淀的質量相等,所以可以判斷第3次所取的氯化鈣溶液有剩余,即說明50g氯化鈣溶液反應后只能得到4g沉淀,綜上分析可以知道第二次是所給的物質恰好完全反應.
設碳酸鈉的質量為x,參加反應的氯化鈣質量為y
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 111 100
x y 4g
$\frac{106}{x}=\frac{111}{y}=\frac{100}{4g}$
解得:x=4.24g,y=4.44 g
(2)加入的氯化鈣溶液的溶質質量分數為:$\frac{11.1g}{50g}×$100%=8.88%;
(3)碳酸鈉樣品中雜質氯化鈉的質量:5g-4.24g=0.76g;
碳酸鈉樣品中雜質氯化鈉的質量分數是$\frac{0.75g}{5g}$×100%=15.2%;
答案:
(1)5g碳酸鈉樣品中碳酸鈉的質量是4.24g;
(2)加入氯化鈣溶液的溶質質量分數是8.88%;
(3)碳酸鈉樣品中雜質氯化鈉的質量分數是15.2%
點評 本題是借助于數學模型,利用圖表的方式來分析和解決化學計算中的有關問題,要求學生有較強的識圖能力和數據分析能力.


科目:初中化學 來源: 題型:選擇題
| A. | CuSO4、NaOH、KNO3、NaCl | B. | K2CO3、NaOH、稀HCl、BaCl2 | ||
| C. | FeCl3、KOH、稀HCl、稀H2SO4 | D. | 稀HCl、Na2CO3、稀H2SO4、Na2SO4 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
 寒冷的冬日早晨,同學送給小科一個“暖寶寶”,小巧可愛.同學告訴他,這個“暖寶寶”不用加熱,只要打開包裝袋,一會兒就能給我們暖手.大家非常好奇,打開一試,果真如此.同學們不禁對“暖寶寶”的內部成分產生了極大的好奇,打開紙包,原來是一些“黑色粉末”,不一會兒還會冒煙,且燙手.那么,這些黑色粉末成分又會是什么呢?
寒冷的冬日早晨,同學送給小科一個“暖寶寶”,小巧可愛.同學告訴他,這個“暖寶寶”不用加熱,只要打開包裝袋,一會兒就能給我們暖手.大家非常好奇,打開一試,果真如此.同學們不禁對“暖寶寶”的內部成分產生了極大的好奇,打開紙包,原來是一些“黑色粉末”,不一會兒還會冒煙,且燙手.那么,這些黑色粉末成分又會是什么呢?查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 竹炭可用于凈化室內空氣 | |
| B. | (C6H10O5)n屬于有機高分子化合物 | |
| C. | 竹炭纖維是由碳元素、氫元素和氧元素組成的 | |
| D. | 竹炭纖維中C、H、O三種元素的質量比為6:10:5 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
 如圖所示,處于連線兩端的物質,在一定的條件下都能發生化學反應.如表中的A、B、C、D四組物質中符合條件的是( )
如圖所示,處于連線兩端的物質,在一定的條件下都能發生化學反應.如表中的A、B、C、D四組物質中符合條件的是( )| 甲 | 乙 | 丙 | 丁 | |
| A | C | O2 | H2SO4 | CuO |
| B | Fe | H2SO4 | CuCl2 | NaOH |
| C | NaOH | CO2 | KOH | CuCl2 |
| D | Na2SO4 | Ba(OH)2 | HCl | Ba(NO3)2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 濕衣服晾干是因為水分子運動到空氣中去了 | |
| B. | 保持水化學性質的最小微粒是水分子 | |
| C. | 水由液態變成氣態時水分子間間隔變大 | |
| D. | 水結冰后體積變大是水分子的體積增大造成的 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 除去NaCl中少量的Na2CO3雜質,先加入足量稀硝酸,再蒸發結晶 | |
| B. | 檢驗可燃性氣體中是否含有氫元素,在其燃燒火焰上方罩上干冷的燒杯,觀察有無水霧 | |
| C. | 實驗測定某礦石中碳酸鈣的質量分數,先加入硫酸,再比較反應前后的質量變化 | |
| D. | 實驗室制備干燥、純凈的氫氣,用鋅與濃鹽酸反應,產生的氣體經濃硫酸干燥后收集 |
查看答案和解析>>
科目:初中化學 來源: 題型:推斷題
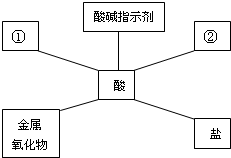
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com