

分析 (1)根據高錳酸鉀在加熱的條件下生成錳酸鉀、二氧化錳和氧氣進行分析;
(2)根據高錳酸鉀固體生成的氧氣總質量和小冰制取氧氣的質量進行計算;
(3)根據高錳酸鉀分解的化學方程式和氧氣的質量進行計算;
(4)根據二氧化錳和錳酸鉀以及生成高錳酸鉀的質量求出小冰和小城加熱制得氧氣的質量比進行解答;
(5)根據溶質質量分數的計算方法進行分析.
解答 解:(1)高錳酸鉀在加熱的條件下生成錳酸鉀、二氧化錳、氧氣,化學方程式為:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)依據質量守恒定律可知,小城生成氧氣的質量為:60g-56.8g=3.2g,
設分解高錳酸鉀的質量為x,生成錳酸鉀的質量為y,生成二氧化碳的質量為z,
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 197 87 32
x y z 3.2g
$\frac{316}{x}$=$\frac{197}{y}$=$\frac{87}{z}$=$\frac{32}{3.2g}$
x=31.6g
z=19.7g
y=8.7g
(2)所以小城的實驗生成氧氣的質量為6.1g-3.2g=2.9g;
(3)設小城實驗中分解的高錳酸鉀質量為x
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 197 87 32
x 2.9g
$\frac{316}{x}$=$\frac{32}{2.9g}$
(4)小冰生成的錳酸鉀、二氧化錳的質量為:56.8g-19.7g-8.7g=28.4g,
高錳酸鉀制取氧氣是生成錳酸鉀和二氧化錳的質量比是197:87,所以小冰制取氧氣生成的錳酸鉀、二氧化錳的質量是19.7g,8.7g,生成的氧氣質量也是3.2g,
所以小冰和小城加熱制得氧氣的質量比為:3.2g:3.2g=1:1;
(5)最后所得不飽和濾液中溶質的質量分數為:$\frac{37.4g}{37.4g+160.6g}$×100%=18.9%.
故答案為:(1)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2).2g;
(3)$\frac{316}{x}$=$\frac{32}{3.2g}$;
(4)1:1;
(5)18.9%.
點評 本題難度不大,主要考查了根據化學方程式來計算有關的量,從而使學生來認識化學反應的本質,代入化學方程式計算的數據必須是純凈物的質量才行.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:初中化學 來源: 題型:選擇題
| A. | 由原子核和核外電子構成 | B. | 質子數是117 | ||
| C. | 質量主要集中在原子核上 | D. | 相對原子質量是117 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
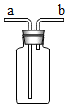 如圖裝置有較多用途,下列有關說法錯誤的是( )
如圖裝置有較多用途,下列有關說法錯誤的是( )| A. | 如瓶內為空氣,要收集氧氣,氣體應從a端進入 | |
| B. | 如瓶內裝滿水,要用排水法收集氧氣,氣體應從a端進入 | |
| C. | 醫院給病人輸氧時,也有類似裝置(瓶內裝半瓶蒸餾水)病人吸氧的塑料管接在b端 | |
| D. | 輸氧時,可通過此裝置觀察是否有氧氣輸出 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
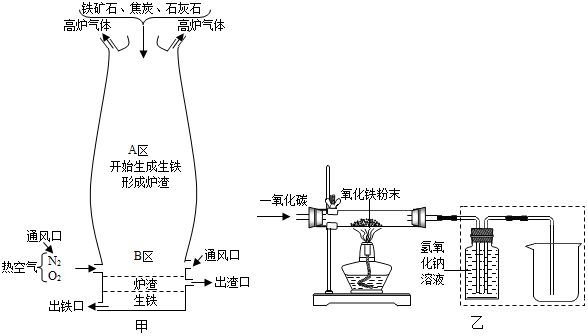
 | 四氧化三鐵 | 氧化亞鐵 | 氧化鐵 | 鐵粉 |
| 顏色 | 黑色 | 黑色 | 紅色 | 黑色 |
| 能否被磁鐵吸引 | 能 | 不能 | 不能 | 能 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
 某研究性學習小組的同學為探究實驗室制取氫氣的方案,分別用等質量的金屬A、B跟質量相同、溶質質量分數相同的稀硫酸反應,反應生成氫氣的質量與時間的關系如圖所示.分析圖象得到的下列結論中,不合理的是(已知A、B在生成物中均顯+2價,A、B的相對原子質量不相等)( )
某研究性學習小組的同學為探究實驗室制取氫氣的方案,分別用等質量的金屬A、B跟質量相同、溶質質量分數相同的稀硫酸反應,反應生成氫氣的質量與時間的關系如圖所示.分析圖象得到的下列結論中,不合理的是(已知A、B在生成物中均顯+2價,A、B的相對原子質量不相等)( )| A. | 反應速率A>B | B. | 生成氫氣的質量A=B | ||
| C. | 金屬的活動性A<B | D. | 硫酸均反應完,A、B有剩余 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
 某同學按如圖裝置對質量守恒定律進行實驗探究,反應前天平平衡,然后將稀鹽酸倒入燒杯中與碳酸鈉充分反應后,再稱量,觀察到反應后天平不平衡,天平指針向右偏轉(填“左”或“右”).該反應遵守質量守恒定律(填“遵守”或“不遵守”).反應后天平不平衡的原因是生成氣體逸散到空氣中去,應如何改進應在密閉條件下進行.
某同學按如圖裝置對質量守恒定律進行實驗探究,反應前天平平衡,然后將稀鹽酸倒入燒杯中與碳酸鈉充分反應后,再稱量,觀察到反應后天平不平衡,天平指針向右偏轉(填“左”或“右”).該反應遵守質量守恒定律(填“遵守”或“不遵守”).反應后天平不平衡的原因是生成氣體逸散到空氣中去,應如何改進應在密閉條件下進行.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com