
題目列表(包括答案和解析)
(2)某學生判斷SO2和Na2O2反應能生成硫酸鈉,你認為他的判斷合理嗎?_________(填“合理”或“不合理”)。簡要說明理由____________________。
(3)該同學無法確定反應中是否有氧氣生成,擬用如圖所示裝置進行實驗。

裝置B的作用是_____________________________________________。
D的作用是:_______________________________________________。
(4)為確認反應產物,請完成下表中所列實驗
操作 | 現象與結論 |
①確認是否有氧氣產生的操作是: | 現象: 結論: |
②確認是否有硫酸鈉產生的操作是: | 現象: 結論 |
(6分)按要求寫出有關的化學方程式。
(1)寫出一個濃硫酸只表現氧化性的化學方程式:________________________________________________。
(2)寫出一個能證明硫酸是強酸的化學方程式:![]() ____________________________________________。
____________________________________________。
(3)“綠色化學”要求綜合考慮經濟、技術、環保等方面來設計化學反應路線。若以銅為原料來制取CuSO4,請你設計符合“綠色化學”思路的反應路線(用化學方程式表示)_______________________________________。
(2)某學生判斷SO2和Na2O2反應能生成硫酸鈉,你認為他的判斷合理嗎?___________。簡要說明理由_________________________________________________________________。
(3)該同學無法斷定SO2和Na2O2反應中是否有氧氣生成,擬用下列裝置進行實驗。
(已知:Na2SO3+2H2SO4![]() Na2SO4+H2O+SO2↑)
Na2SO4+H2O+SO2↑)
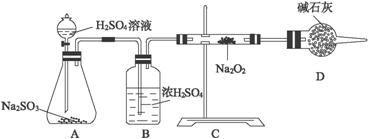
裝置B的作用是__________________________________________________________。
D的作用是____________________________________________________________。
(4)為確認SO2和Na2O2的反應產物,該同學設計了以下實驗步驟,請你從中挑選出正確的選項并按操作順序排列(填序號)_______________。
A.用帶火星的木條靠近干燥管口,觀察木條是否復燃
B.用C裝置中反應后的固體物質溶于適量水配成溶液
C.在配成的溶液中加入用硝酸酸化的硝酸鋇溶液,觀察是否有沉淀生成
D.在配成的溶液中先加入鹽酸,再加入氯化鋇溶液,觀察是否有氣泡或沉淀生成
(2)某學生判斷SO2和Na2O2反應能生成硫酸鈉,你認為他的判斷合理嗎?(填“合理”或“不合理”)__________。簡要說明理由___________________________________________。
(3)該同學無法確定反應中是否有氧氣生成,擬用如下圖所示裝置進行實驗。
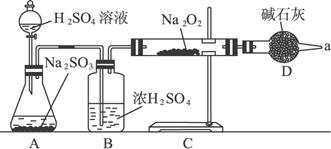
裝置B的作用是_________________________________________________。D的作用是:________________________________________。
(4)為確認反應產物,請完成下表中所列實驗
操作 | 現象與結論 |
①確認是否有氧氣產生的操作是: |
|
②確認是否有硫酸鈉產生的操作是: |
|
化學能與電能之間的相互轉化與人的生活實際密切相關,在生產、生活中有重要的應用,同時也是學生形成化學學科素養的重要組成部分。
(1)熔融狀態下,鈉的單質和氯化亞鐵能組成可充電電池(如圖1),反應原理為:2Na+FeCl2  Fe+2NaCl,該電池放電時,正極反應式為 ________________ _____:
Fe+2NaCl,該電池放電時,正極反應式為 ________________ _____:
充電時,__________(寫物質名稱)電極接電源的負極;
該電池的電解質為________ _。
(2)某同學用銅片、石墨作電極電解一定濃度的硫酸銅溶液(如圖2),一段時間停止通電取出電極。若在電解后的溶液中加入0.98g氫氧化銅粉末恰好完全溶解,經測定所得溶液與電解前完全相同。請回答下列問題:
①Y電極材料是 ,發生 (填“氧化或還原”)反應。
②電解過程中X電極上發生的電極反方應式是:
③如在電解后的溶液中加入足量的小蘇打,充分反應后產生氣體在標準狀況下所占的體積是
(3)常溫時,BaSO4的Ksp=1.08×10-10,現將等體積的BaCl2溶液與2.0×10-3mol/l的Na2SO4
溶液混合。若要生成BaSO4沉淀,BaCl2溶液的最小濃度為______________。
一.選擇題(本題包括8小題,每小題3分,共24分)
題號
1
2
3
4
5
6
7
8
答案
A
D
B
C
B
A
C
D
二.選擇題(本題包括8小題,每小題3分,共24分)
題號
9
10
11
12
13
14
15
16
答案
B
AC
C
BC
AD
C
AD
D
三.(本題包括2小題,共20分)
17.(共8分)
(1)Cu+4H++2NO3-=Cu2++2NO2↑+2H2O (2分)
(2)①不易控制反應。②產生有毒氣體,造成污染環境。(2分)
(3)c; a、b。(2分)
(4)關閉a, b,打開c (1分) 用手捂住(熱水、熱毛巾、加熱)試管② (1分)
(合理答案均給分)
18.(每空2分,共12分)
實驗一:(1)反應物本身的性質對反應速率的關系;(2分)
溫度相同;(2分)
(2)Mg(或Fe)和0.5mol/L硫酸和2mol/L硫酸;(2分)
測定一定時間產生氣體的體積(或者測定一定體積的氣體所需時間);(2分)
實驗二:(1)催化劑(或硫酸錳或Mn2+的催化作用);(2分)
 (2)B
(2分)
(2)B
(2分)
四.(本題包括2小題,共20分)
19.(每空2分,共10分)
(1)0.1;(2)1.69;
(3)①c;②(參看右圖)
(4)0<c(A)<0.2mol/L;(5)B
20.(每空2分,共10分)
(1) (2分)
(2分)
(2)均為氧化還原反應 (2分)
(3)3Fe+ 4H2O  Fe 3O4+4H2↑
(2分)
Fe 3O4+4H2↑
(2分)
(4)Fe+4H++2NO3-=Fe2++2NO2↑+2 H2O (2分)
(5)取少量樣品于試管中,加入KSCN溶液,如果出現紅色,說明變質;反之,沒有變質 (2分)
五.(本題包括1小題,共12分)
21.(共12分)
(1)1S22S22P6;(2分)(2)H2S或NH2-;(2分)
(3)A;(2分)(4)BC;(2分)(5)20; (2分)
(6)Cu2++4H2O=[Cu(H2O)4]2+ (2分)
六.(本題包括1小題,共10分)
22.(共10分)
(1)B (2分)
(2)2H2O 2H2↑+O2↑
(2分)
2H2↑+O2↑
(2分)
(3) SO2+I2+2H2O 2HI+H2SO4 (2分)
2HI+H2SO4 (2分)
SO2和I2可循環使用,無污染。 (2分)
(4)不現實,理由是現有的制取氫氣方法耗能大,制取的成本太高,另外是氫氣的熔沸點太低,給儲存和運輸帶來困難。(或:現實,制取氫氣用水為原料,來源豐富;氫氣燃燒的產物是水,不會給環境帶來任何污染等。) (2分)
 七.(本題包括1小題,共10分)
七.(本題包括1小題,共10分)
23.(10分)
(1)134.4;
(2) (參看右圖);
(3)0.068mol;
(4)
說明:本試卷中其他合理答案同樣給分。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com