
題目列表(包括答案和解析)

已知A、B、C、D、E是化學中常見的物質,常溫下,E是一種無色無味的液體,它們之間有如下反應關系。
(1)若A是一種黑色單質,B是一種常見的難揮發性酸,C、D都是氣體,試寫出此反應的化學方程式 。
(2)若A是一種紫紅色單質,B是一種常見的揮發性酸,反應時生成的C是無色氣體,反應的離子方程式是 ,B在反應中表現出的性質是 、 。
(3)若實驗室中利用A和B的反應制備氣體C,C是一種無色、刺激性氣味、密度比空氣小的氣體,試寫出此反應的化學方程式 ;實驗室檢驗C的方法 。


(14分)二氧化氯(ClO2)是一種在水處理等方面有廣泛應用的高效安全消毒劑。實驗室以NH4Cl、鹽酸、NaClO2(亞氯酸鈉)為原料制備ClO2的流程下如下:
已知:①NCl3是黃色黏稠狀液體或斜方形晶體,極易爆炸,有類似氯氣的刺激性氣味,自然爆炸點為95℃,在熱水中易分解,在空氣中易揮發,不穩定。②氣體B能使濕潤的紅色石蕊試紙變藍。
回答下列問題:
(1)電解時,發生反應的化學方程式為 。為保證實驗的安全,在電解時需注意的問題是:①控制好生成NCl3的濃度;② 。
(2)NCl3與NaClO2(亞氯酸鈉)按物質的量之比為1∶6混合,在溶液中恰好反應生成ClO2,該反應的離子方程式為 。
(3)實驗室制取氣體B的化學方程式為 。
(4)ClO2很不穩定,需隨用隨制,產物用水吸收得到ClO2溶液。為測定所得溶液中ClO2的含量,進行了下列實驗:
步驟1:準確量取ClO2溶液10 mL,稀釋成100 mL試樣;
步驟2:量取V1 mL試樣加入到錐形瓶中,調節試樣的pH≤2.0,加入足量的KI晶體,搖勻,在暗處靜置30 min。
步驟3:以淀粉溶液作指示劑,用c mol/L Na2S2O3溶液滴定至終點,消耗Na2S2O3溶液V2 mL。
(已知I2+2S2O32-=2I-+S4O62-)
①若步驟2中未將錐形瓶“在暗處靜置30 min”,立即進行步驟3,則測定的結果可能
(選填“偏大”、“偏小”、“無影響”);
②上述步驟3中滴定終點的現象是 。
③根據上述步驟可計算出原ClO2溶液的濃度為 g / L(用含字母的代數式表示)。
(14分)二氧化氯(ClO2)是一種在水處理等方面有廣泛應用的高效安全消毒劑。實驗室以NH4Cl、鹽酸、NaClO2(亞氯酸鈉)為原料制備ClO2的流程下如下:
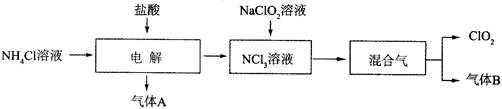
已知:①NCl3是黃色黏稠狀液體或斜方形晶體,極易爆炸,有類似氯氣的刺激性氣味,自然爆炸點為95℃,在熱水中易分解,在空氣中易揮發,不穩定。②氣體B能使濕潤的紅色石蕊試紙變藍。
回答下列問題:
(1)電解時,發生反應的化學方程式為 。為保證實驗的安全,在電解時需注意的問題是:①控制好生成NCl3的濃度;② 。
(2)NCl3與NaClO2(亞氯酸鈉)按物質的量之比為1∶6混合,在溶液中恰好反應生成ClO2,該反應的離子方程式為 。
(3)實驗室制取氣體B的化學方程式為 。
(4)ClO2很不穩定,需隨用隨制,產物用水吸收得到ClO2溶液。為測定所得溶液中ClO2的含量,進行了下列實驗:
步驟1:準確量取ClO2溶液10 mL,稀釋成100 mL試樣;
步驟2:量取V1 mL試樣加入到錐形瓶中,調節試樣的pH≤2.0,加入足量的KI晶體,搖勻,在暗處靜置30 min。
步驟3:以淀粉溶液作指示劑,用c mol/L Na2S2O3溶液滴定至終點,消耗Na2S2O3溶液V2 mL。
(已知I2+2S2O32-=2I-+S4O62-)
①若步驟2中未將錐形瓶“在暗處靜置30 min”,立即進行步驟3,則測定的結果可能
(選填“偏大”、“偏小”、“無影響”);
②上述步驟3中滴定終點的現象是 。
③根據上述步驟可計算出原ClO2溶液的濃度為 g / L(用含字母的代數式表示)。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com