
題目列表(包括答案和解析)
 硝酸與金屬反應時,還原產物可能是NO2、NO、N2O、N2或NH
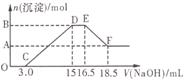
硝酸與金屬反應時,還原產物可能是NO2、NO、N2O、N2或NH![]() 中的一種或幾種。現有一定量的Al粉和Fe粉的混合物與100mL稀硝酸充分反應,反應過程中無任何氣體放出。在反應結束后的溶液中逐滴加入4mol/L的NaOH溶液,加入NaOH溶液的體積與產生沉淀的物質的量的關系如圖,則下列說法中不正確的是
中的一種或幾種。現有一定量的Al粉和Fe粉的混合物與100mL稀硝酸充分反應,反應過程中無任何氣體放出。在反應結束后的溶液中逐滴加入4mol/L的NaOH溶液,加入NaOH溶液的體積與產生沉淀的物質的量的關系如圖,則下列說法中不正確的是
A.與HNO3反應后,Fe元素的化合價為+3
B.D→E段反應的離子方程式為:NH![]() +OH-=NH3·H2O
+OH-=NH3·H2O
C.縱坐標A點數值為0.008
D.縱坐標B點數值為0.012
硝酸與金屬反應時,還原產物可能是NO2、NO、N2O、N2或NH 中的一種或幾種。現有一定量的Al粉和Fe粉的混合物與100mL稀硝酸充分反應,反應過程中無任何氣體放出。在反應結束后的溶液中逐滴加入4mol/L的NaOH溶液,加入NaOH溶液的體積與產生沉淀的物質的量的關系如圖,則下列說法中不正確的是
中的一種或幾種。現有一定量的Al粉和Fe粉的混合物與100mL稀硝酸充分反應,反應過程中無任何氣體放出。在反應結束后的溶液中逐滴加入4mol/L的NaOH溶液,加入NaOH溶液的體積與產生沉淀的物質的量的關系如圖,則下列說法中不正確的是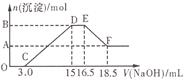
| A.與HNO3反應后,Fe元素的化合價為+3 |
B.D→E段反應的離子方程式為:NH +OH-=NH3·H2O +OH-=NH3·H2O |
| C.縱坐標A點數值為0.008 |
| D.縱坐標B點數值為0.012 |
 金屬腐蝕造成很大的經濟損失,甚至超過自然災害,其中鋼鐵銹蝕最為嚴重,尋求防止鋼鐵腐蝕的方法意義重大.
金屬腐蝕造成很大的經濟損失,甚至超過自然災害,其中鋼鐵銹蝕最為嚴重,尋求防止鋼鐵腐蝕的方法意義重大.| 1 |
| 5 |
| 2 |
| 9 |
| 1 |
| 4 |
| 1 |
| 3 |
| 1 |
| 2 |
金屬腐蝕造成很大的經濟損失,甚至超過自然災害,其中鋼鐵銹蝕最為嚴重,尋求防止鋼鐵腐蝕的方法意義重大。
(1)鋼鐵的表面發藍、發黑處理是常用的防腐方法。下列反應是主要反應之一。
請配平方程式:口 Na2FeO2+ 口 NaNO2+ 口 = 口 NaFeO2+ 口 NH3↑+ 口 NaOH
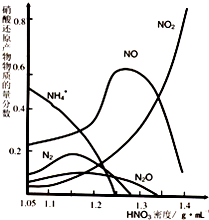
(2)鋼鐵的“鈍化”處理也能達到防腐目的,經冷、濃 HNO3 處理后,其表面有一層致密氧化物保護膜,但是加熱或在稀HNO3中 就不能 “鈍化”。不同濃度的HNO3 與鐵反應的還原產物很復雜,其分布曲線如圖。
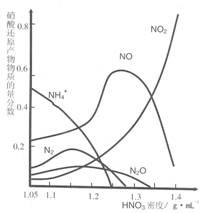
①圖示可知,密度為 1.05g?mL-1 的硝酸與鐵反應時,其最多的還原產物是
;密度大于1.35 g?mL-1的硝酸與鐵反應時,其還原產物主要是 NO2;分析HNO3 與鐵反應的規律是: 。
② mg 鐵與含 n g HNO3的硝酸溶液恰好完全反應,若硝酸的還原產物只有 NO, 則 m 的取值可能是 (填字母編號 )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]() E.
E.![]()
③工業上一般不用冷濃硝酸進行鐵表面處理,其可能的原因是:
。
(3)金屬 (M) 的腐蝕是因為發生反應: M-ne-→Mn+,除了上述表面處理的方法外,下列方法也能起到防腐作用的是 (填字母編號)
A.在鐵中摻入銘、鎮等金屬,改變其內部結構,制成不銹鋼
B.在鐵制品表面鍍辭
C.提高鐵中含碳量,制成生鐵
D.將水庫鐵閘門與直流電源的負極相連
(16分)(1)(6分)測定Na2O和Na的混合物中金屬鈉的質量分數可用下圖所示的幾套儀器組合: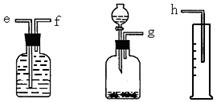
①用接口字母標出各儀器連接的順序 量筒在實驗中的作用是
②有一塊表面氧化成Na2O的金屬鈉,其質量為2.0g,實驗后在量筒中收集到0.224L水,求樣品中金屬鈉的質量分數是 。(假設在標準狀況下測定)
(2)(10分) HNO2是一種弱酸,且不穩定,易分解生成NO和NO2;它能被常見的強氧化劑氧化;在酸性溶液中它也是一種氧化劑,如能把Fe2+氧化成Fe3+。AgNO2是一種難溶于水、易溶于酸的化合物。試回答下列問題:
①人體正常的血紅蛋白含有Fe2+。若誤食亞硝酸鹽(如NaNO2),則導致血紅蛋白中的Fe2+轉化為Fe3+而中毒,服用維生素C可解毒。下列敘述不正確的是________(填序號)。
A.亞硝酸鹽被還原 B.維生素C具有還原性
C.維生素C將Fe3+還原為Fe2+ D.在上述變化中亞硝酸鹽是還原劑
②下列方法中,不能用來區分NaNO2和NaCl兩種溶液的是________(填序號)。
A.測定這兩種溶液的pH
B.分別在兩種溶液中滴加甲基橙
C.在酸性條件下加入KI—淀粉溶液來區別
D.用AgNO3和HNO3兩種試劑來區別
③某同學把新制的氯水加到NaNO2溶液中,觀察到氯水褪色,同時生成NaNO3和HCl,請寫出反應的離子方程式:___________________________________。
④ Fe與過量稀硫酸反應可以制取FeSO4。若用反應所得的酸性溶液,將Fe2+轉化為Fe3+,要求產物純凈,可選用的最佳試劑是________(填序號)。
a.Cl2 b.Fe c.H2O2 d.HNO3
⑤配平下列方程式:
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com