
�}Ŀ�б�(�����𰸺ͽ���)
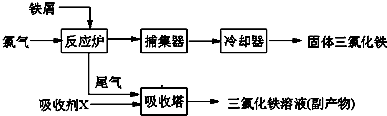
| �ض�/�� | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
| �ܽ�ȣ�g/100gH20�� | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
| 162.5cV |
| m |
| 162.5cV |
| m |
| ||
| ||
| �ض�/�� | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
| �ܽ��/g | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
| 162.5cV |
| m |
| 162.5cV |
| m |
����ʡ���W�`���Ͳ�����Ϣ�e��ƽ�_ | �W���к���Ϣ�e�^ | ����p�_�e�^ | ��vʷ̓�o���x�к���Ϣ�e�^ | �����֙��e�^
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com