
題目列表(包括答案和解析)
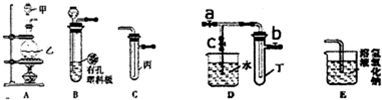
合成氨的流程示意圖如下:
回答下列問題:
(1)設備A中含有電加熱器,觸媒和熱交換器,其中發生的化學反應方程式為______,設備A的名稱是______;
(2)設備B中m和n是兩個通水口,入水口是______(填“m”或“n”).不宜從相反方向通水的原因是______;
(3)工業合成氨的原料是氮氣和氫氣.氮氣是從空氣中分離出來的,通常使用的兩種分離方法是______,______;
(4)天然氣、重油、煤都可以與水反應制得氫氣.下表是某合成氨廠采用不同原料的相對投資和能量消耗.
| 原料 | 天然氣 | 重油 | 煤 |
| 相對投資費用 | 1.0 | 1.5 | 2.0 |
| 能量消耗/J?t-1 | 28109 | 38109 | 48109 |
①依據上表信息,你認為采用______為原料最好;
②請寫出甲烷在高溫、催化劑的作用下與水蒸氣反應生成氫氣和一氧化碳的化學方程式:______;
③已知C(s)、CO(g)和H2(g)完全燃燒的熱化學方程式分別為:
C(s)+O2(g)═CO2(g)△H=-394kJ/mol;
2CO2(g)+O2(g)═CO2(g)△H=-566kJ/mol;
2H2(g)+O2(g)═2H2O(g)△H=-484kJ/mol;
試寫出由C與水蒸氣在高溫條件下反應生成氫氣與一氧化碳的熱化學方程式______;
(5)在合成氨生產中,將生成的氨及時從反應后的氣體中分離出來.運用化學平衡的知識分析這樣做的理由:______.
(14分)不同的金屬在化學反應中表現出來的活潑程度不同,瑞典化學家貝采里烏斯和俄國化學家貝開托夫稱之為金屬活動順序。另一方面,同一金屬在不同條件或不同化學反應中也可以表現出不同的活潑程度。
⑴根據金屬活動性順序,工業上冶煉金屬可以采用不同的冶煉方法。其中可以用“熱分解法”冶煉的金屬有 。
腐蝕速率/g.m-2.h-1
 ⑵工業上用氯化鐵溶液腐蝕銅制電路板。根據金屬活動性順序及該反應原理,比較Cu2+、Fe3+、Fe2+的氧化性由強到弱的順序: 。
⑵工業上用氯化鐵溶液腐蝕銅制電路板。根據金屬活動性順序及該反應原理,比較Cu2+、Fe3+、Fe2+的氧化性由強到弱的順序: 。
⑶合金Fe-Cr在不同酸中反應情況不同,其在三種稀硫
酸、稀硝酸和稀鹽酸中的腐蝕速率如圖所示,則下列
有關說法正確的是 (填寫序號)。
A.酸的氧化性越強,對該合金的腐蝕速率越大
B.稀硝酸對該合金的腐蝕性比另兩種酸弱
C.合金中Cr含量增加,稀硝酸對該合金的腐蝕性減弱
⑷已知粗銅中含有少量的鋅、鐵、銀、金等金屬和少量
|
以硫酸銅溶液為電解液,用電解的方法實現了粗銅的提純,
并對陽極泥和電解液中金屬進行回收。
步驟一:電解精制
電解時,粗銅應與電源的 極相連。電解過程中,硫酸銅的濃度會 (填“變大”、“不變”或“變小”)。
步驟二:電解完成后,該小組同學按以下流程對電解液進行處理:

稀硝酸處理陽極泥得到硝酸銀稀溶液,請你寫出該步反應的離子方程式: 。
殘渣含有極少量的黃金,如何回收金,他們查閱了有關資料,了解到了一些有關金的知識,以下是他們獲取的一些信息:
| 序號 | 反應 | 平衡常數 |
| 1 | Au + 6HNO3(濃)= Au(NO3)3 + 3NO2↑+ 3H2O | << 1 |
| 2 | Au3+ + 4Cl- = AuCl4- | >>1 |
從表中可知,金很難與硝酸反應,但卻可溶于王水(濃硝酸與鹽酸按體積比1:3的混合物),請你簡要解釋金能夠溶于王水的原因: 。
不同的金屬在化學反應中表現出來的活潑程度不同,瑞典化學家貝采里烏斯和俄國化學家貝開托夫稱之為金屬活動順序.另一方面,同一金屬在不同條件或不同化學反應中也可以表現出不同的活潑程度.
(1)根據金屬活動性順序,工業上冶煉金屬可以采用不同的冶煉方法.其中可以用“熱分解法”冶煉的金屬有________.
(2)
工業上用氯化鐵溶液腐蝕銅制電路板.根據金屬活動性順序及該反應原理,比較Cu2+、Fe3+、Fe2+的氧化性由強到弱的順序:________.(3)合金Fe-Cr在不同酸中反應情況不同,其在三種稀硫酸、稀硝酸和稀鹽酸中的腐蝕速率如圖所示,則下列有關說法正確的是________(填寫序號).

A.酸的氧化性越強,對該合金的腐蝕速率越大
B.稀硝酸對該合金的腐蝕性比另兩種酸弱
C.合金中Cr含量增加,稀硝酸對該合金的腐蝕性減弱
(4)已知粗銅中含有少量的鋅、鐵、銀、金等金屬和少量礦物雜質
(與酸不反應).某化學興趣小組在實驗室條件下,以硫酸銅溶液為電解液,用電解的方法實現了粗銅的提純,并對陽極泥和電解液中金屬進行回收.步驟一:電解精制電解時,粗銅應與電源的________極相連.電解過程中,硫酸銅的濃度會________(填“變大”、“不變”或“變小”).
步驟二:電解完成后,該小組同學按以下流程對電解液進行處理:

稀硝酸處理陽極泥得到硝酸銀稀溶液,請你寫出該步反應的離子方程式:________.
殘渣含有極少量的黃金,如何回收金,他們查閱了有關資料,了解到了一些有關金的知識,以下是他們獲取的一些信息:

從表中可知,金很難與硝酸反應,但卻可溶于王水(濃硝酸與鹽酸按體積比1∶3的混合物),請你簡要解釋金能夠溶于王水的原因:________.
| 實驗 序號 |
實驗操作 | 現象 | 結論 |
| I | 將氯水滴入品紅溶液 | 溶液褪色 | Cl2與水反應的產物有漂白性 |
| II | 氯水中加入NaHCO3粉末 | 有無色氣泡產生 | Cl2與水反應的產物具有較強的酸性 |

| 實驗序號 | 實驗操作 | 現象 | 結論 |
| Ⅰ | 將氯氣滴入品紅溶液中 | 溶液褪色 | 氯氣與水反應的產物有漂白粉 |
| Ⅱ | 向氯氣中加入碳酸氫鈉粉末 | 產生氣泡 | 氯氣與水反應的產物具有酸性 |
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com