
題目列表(包括答案和解析)
研究物質(zhì)的微觀結(jié)構(gòu),有助于人們理解物質(zhì)性質(zhì)和變化的本質(zhì).請(qǐng)回答下列問題.
(1)CH4中H為+1價(jià),SiH4中共用電子對(duì)偏向H,則C、Si、H的電負(fù)性由大到小的順序是:________.C60和金剛石都是碳的同素異形體,金剛石的熔點(diǎn)高于C60,原因是:________.C60被發(fā)現(xiàn)后,科學(xué)家又合成了結(jié)構(gòu)相似的Si60、N60等,C60、Si60、N60三者的熔點(diǎn)從高到低的順序是:________.
(2)A、B均為短周期金屬元素.依據(jù)下表數(shù)據(jù)和已學(xué)知識(shí),寫出B原子的電子排布式:________.
![]()
(3)過渡金屬離子與水分子形成的配合物是否有顏色,與其d軌道電子排布有關(guān).一般地,為d0或d10排布時(shí),無顏色;為d1~d9排布時(shí),有顏色,如[Co(H2O)6]2+顯粉紅色.據(jù)此判斷,[Mn(H2O)6]2+________顏色,[Zn(H2O)6]2+________顏色,(填“無”或“有”)
(4)CO與Cl2在催化劑作用下生成COCl2,COCl2俗稱光氣,極毒,光氣分子呈平面三角形,結(jié)構(gòu)式為![]() ,則其碳原子的雜化類型是________,COCl2分子內(nèi)含有________(填標(biāo)號(hào))
,則其碳原子的雜化類型是________,COCl2分子內(nèi)含有________(填標(biāo)號(hào))
A.4個(gè)σ鍵
B.2個(gè)σ鍵、2個(gè)π鍵
C.3個(gè)σ鍵、1個(gè)π鍵
D.2個(gè)σ鍵、1個(gè)π鍵
某校化學(xué)研究性學(xué)習(xí)小組的同學(xué)在學(xué)習(xí)了金屬的知識(shí)后,為了解Cu的常見化合物性質(zhì),運(yùn)用類比學(xué)習(xí)的思想提出如下的問題,進(jìn)行探究。請(qǐng)你協(xié)助該小組的同學(xué)完成下列研究。
用類比學(xué)習(xí)的思想提出如下的問題,進(jìn)行探究。請(qǐng)你協(xié)助該小組的同學(xué)完成下列研究。
[提出問題]
①Cu金屬活潑性小于Al,Al(OH)3具有兩性,Cu(OH)2也具有兩性嗎?
②通常情況下,+2價(jià)Fe穩(wěn)定性小于+3價(jià)Fe,+1價(jià)Cu的穩(wěn)定性也小于+2價(jià)Cu嗎?
③CuO能被H2、CO等還原,也能被NH3還原嗎?
[實(shí)驗(yàn)方案]
(1)為解決問題①,需用到的藥品有CuSO4溶液、 (填試劑),同時(shí)進(jìn)行相關(guān)實(shí)驗(yàn)。
(2)解決問題②的實(shí)驗(yàn)步驟和現(xiàn)象如下:取98gCu(OH)2固體,加熱至80°C~110°C時(shí),得到黑色固體粉末,繼續(xù)加熱到1100°以上,黑色粉末全部變成紅色粉末A。冷卻后稱量,A的質(zhì)量為72g。向A中加入適量的稀硫酸,得到藍(lán)色溶液,同時(shí)觀察到容器中還有紅色固體存在。據(jù)此可推得,A的化學(xué)式為 。
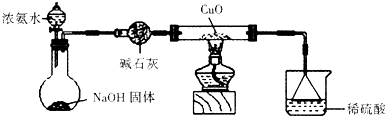
(3)為解決問題③,設(shè)計(jì)的實(shí)驗(yàn)裝置為(夾持及尾氣處理裝置未畫出):
實(shí)驗(yàn)中觀察到CuO變?yōu)榧t色物質(zhì),無水CuSO4變藍(lán)色。同時(shí)生成一種無污染的氣體。
[實(shí)驗(yàn)結(jié)論]
(1)Cu(OH)2具有兩性。證明Cu(OH)2具有兩性的實(shí)驗(yàn)現(xiàn)象是 。
(2)根據(jù)“實(shí)驗(yàn)方案(2)”,得出的+1介Cu和+2價(jià)Cu穩(wěn)定性大小的結(jié)論是:
在高于1100°C時(shí), 價(jià)Cu穩(wěn)定;在溶液中 價(jià)Cu穩(wěn)定。
(3)CuO能被NH3還原。該反應(yīng)的化學(xué)方程式為 。
某校化學(xué)研究性學(xué)習(xí)小組的同學(xué)在學(xué)習(xí)了金屬的知識(shí)后,為了解Cu的常見化合物性質(zhì),運(yùn)用類比學(xué)習(xí)的思想提出如下的問題,進(jìn)行探究。請(qǐng)你協(xié)助該小組的同學(xué)完成下列研究。
用類比學(xué)習(xí)的思想提出如下的問題,進(jìn)行探究。請(qǐng)你協(xié)助該小組的同學(xué)完成下列研究。
[提出問題]
①Cu金屬活潑性小于Al,Al(OH)3具有兩性,Cu(OH)2也具有兩性嗎?
②通常情況下,+2價(jià)Fe穩(wěn)定性小于+3價(jià)Fe,+1價(jià)Cu的穩(wěn)定性也小于+2價(jià)Cu嗎?
③CuO能被H2、CO等還原,也能被NH3還原嗎?
[實(shí)驗(yàn)方案]
(1)為解決問題①,需用到的藥品有CuSO4溶液、 (填試劑),同時(shí)進(jìn)行相關(guān)實(shí)驗(yàn)。
(2)解決問題②的實(shí)驗(yàn)步驟和現(xiàn)象如下:取98gCu(OH)2固體,加熱至80°C~110°C時(shí),得到黑色固體粉末,繼續(xù)加熱到1100°以上,黑色粉末全部變成紅色粉末A。冷卻后稱量,A的質(zhì)量為72g。向A中加入適量的稀硫酸,得到藍(lán)色溶液,同時(shí)觀察到容器中還有紅色固體存在。據(jù)此可推得,A的化學(xué)式為 。
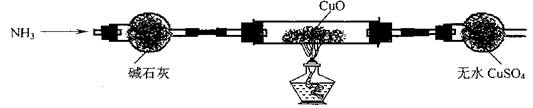
(3)為解決問題③,設(shè)計(jì)的實(shí)驗(yàn)裝置為(夾持及尾氣處理裝置未畫出):

實(shí)驗(yàn)中觀察到CuO變?yōu)榧t色物質(zhì),無水CuSO4變藍(lán)色。同時(shí)生成一種無污染的氣體。
[實(shí)驗(yàn)結(jié)論]
(1)Cu(OH)2具有兩性。證明Cu(OH)2具有兩性的實(shí)驗(yàn)現(xiàn)象是 。
(2)根據(jù)“實(shí)驗(yàn)方案(2)”,得出的+1介Cu和+2價(jià)Cu穩(wěn)定性大小的結(jié)論是:
在高于1100°C時(shí), 價(jià)Cu穩(wěn)定;在溶液中 價(jià)Cu穩(wěn)定。
(3)CuO能被NH3還原。該反應(yīng)的化學(xué)方程式為 。
(8分) 研究物質(zhì)的微觀結(jié)構(gòu),有助于人們理解物質(zhì)變化的本質(zhì)。請(qǐng)回答下列問題。
(1)C、Si、N元素的電負(fù)性由大到小的順序是 。C60和金剛石都是碳的同素異形體,金剛石熔點(diǎn)高于C60熔點(diǎn),原因是
。
(2)A、B均為短周期金屬元素。依據(jù)下表數(shù)據(jù)和已學(xué)知識(shí),
| 電離能/KJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
寫出B原子的電子排布式: 。
(3)過渡金屬離子與水分子形成的配合物是否有顏色,與其d軌道電子排布有關(guān)。一般地,為d0或d10排布時(shí),無顏色;為d1~d9排布時(shí),有顏色,如[Co(H2O)6]2+顯粉紅色。據(jù)此判斷,[Mn(H2O) 6]]2+ (填“無”或“有”)顏色。
(4)利用CO可以合成化工原料COCl2、絡(luò)合物Fe(CO)5等。
①已知COCl2分子的結(jié)構(gòu)式為,則 COCl2分子內(nèi)含_______(填標(biāo)號(hào))。
A.4個(gè)![]() 鍵
鍵
B.2個(gè)![]() 鍵、2個(gè)
鍵、2個(gè)![]() 鍵
鍵
C.2個(gè)![]() 鍵、1個(gè)
鍵、1個(gè)![]() 鍵
鍵
D.3個(gè)![]() 鍵、1個(gè)
鍵、1個(gè)![]() 鍵
鍵
②Fe(CO)5在一定條件下發(fā)生分解反應(yīng):Fe(CO)5=Fe(s)+5CO,反應(yīng)過程中,斷裂的化學(xué)鍵只有配位鍵,形成的化學(xué)鍵是 。
百度致信 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com