
題目列表(包括答案和解析)
某溶液中只可能含有下列離子中的幾種(不考慮溶液中較少的H+和OH-)Na+、NH4+、SO42-、CO32-、NO3-。取200mL該溶液,分為等體積的兩份分別做下列實驗。實驗1:第一份加入足量的燒堿并加熱,產生的氣體在標準狀況下為224mL。實驗2:第二份先加入足量的鹽酸,無現象,再加足量的BaCl2溶液,得固體2.33g。下列說法正確的是( )
A.該溶液中可能含有Na+ B.該溶液中肯定含有NH4+、S042-、CO32-、NO3-
C.該溶液中一定不含NO3- D.該溶液中一定含Na+,且c(Na+)≥0.1mol/L
下列是酸溶液與堿溶液發生反應的各種關系,請用“>”“<”或“=”填空:
(1) 取0.2 mol/LHX溶液與0.2 mol/L NaOH溶液等體積混合,測得混合溶液中c(Na+)>c(X-)。
①混合溶液中c(HX) c(X-);
②混合溶液中c(HX) + c(X-) 0.1mol/L(忽略溶液體積變化);
③混合溶液中由水電離出的c(OH-) 0.1 mol/L 的HX溶液中由水電離出的c(H+)。
(2) 如果取0.2 mol/LHX溶液與0.1 mol/LNaOH溶液等體積混合,測得混合溶液的PH>7,則說明在相同濃度時HX的電離程度 NaX的水解程度。
(3) 分別取pH=2的硫酸和醋酸各50mL,加入足量的鎂粉,反應開始時,反應速率前者_________后者;充分反應后,相同條件下產生氫氣的體積前者_________后者。
(4) 等濃度等體積的鹽酸和醋酸,分別與等濃度的NaOH溶液反應,恰好中和時,消耗NaOH的體積前者__________后者,所得溶液的pH前者________后者。
分別取40mL的0.50mol/L鹽酸與40mL 0.55mol/L氫氧化鈉溶液進行中和反應。通過測定反應過程中所放出的熱量可計算中和熱。請回答下列問題。
(1)理論上稀強酸、稀強堿反應生成1mol水時放出57.3kJ的熱量,寫出表示稀硫酸和稀氫氧化鈉溶液反應的中和熱的熱化學方程式 ;
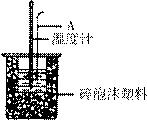 (2)如右圖所示,儀器A的名稱是_______________;在實驗過程中,如果不把溫度計上的酸用水沖洗干凈直接測量NaOH溶液的溫度,則測得的△H (填“偏大”、“偏小”或“無影響”);
(2)如右圖所示,儀器A的名稱是_______________;在實驗過程中,如果不把溫度計上的酸用水沖洗干凈直接測量NaOH溶液的溫度,則測得的△H (填“偏大”、“偏小”或“無影響”);
(3)假設鹽酸和氫氧化鈉溶液的密度都是1g/cm3,又知中和后生成溶液的比熱容c=4.18J/(g?℃)。為了計算中和熱,某學生實驗記錄數據如下:
實驗序號 | 起始溫度t1℃ | 終止溫度t2℃ | |
鹽酸 | 氫氧化鈉 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
依據該學生的實驗數據計算,該實驗測得的中和熱△H=________________;(結果保留一位小數)
(4) (填“能”或“不能”)用Ba(OH)2和硫酸代替鹽酸和氫氧化鈉溶液,理由是 。
已知NaHSO3溶液呈酸性、NaHCO3溶液呈堿性。現有濃度均為0.1mol?L―1的NaHSO3的溶液和NaHCO3溶液,溶液中各粒子的物質的量濃度存在下列關系(R表示S或C),其中正確的是( )
A.c(Na+)>c(HRO3―)>c(H+)>c(RO32―)>c(OH―)
B.c(Na+)+ c(H+)=c(HRO3―)+c(RO32―)+c(OH―)
C.c(H+)+ c(HRO3―)= c(RO32―)+c(OH―)
D.兩溶液中c(Na+)、c(HRO3―)、c(RO32―)分別相等
已知NaHSO3溶液呈酸性、NaHCO3溶液呈堿性。現有濃度均為0.1mol/L-1的NaHSO3溶液和NaHCO3溶液,溶液中各粒子的物質的量濃度存在下列關系(R表示S或C),其中一定正確的是
A.c(Na+)>c(HRO3-)>c(H+)>c(RO32-)>c(OH-)
B.c(Na+)+c(H+)=c(HRO3-)+c(RO32-)+c(OH-)
C.兩溶液中c(Na+)、c(HRO3-)、c(RO32-)分別相等
D. c(H+)+c(H2RO3)=c(RO32-)+c(OH-)
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com