
題目列表(包括答案和解析)
(8分)經研究知Cu2+對H2O2分解也具有催化作用,為比較Fe3+和Cu2+對H2O2分解的催化效果,某研究小組的同學分別設計了如圖甲、乙所示的實驗。回答相關問題:
(1)定性分析:如圖甲可通過觀察___________________________________定性比較得出結論。有同學提出將FeCl3改為Fe2(SO4)3更為合理,其理由是____________________,
寫出H2O2在二氧化錳作用下發生反應的化學方程式:
_____________________________________________________。
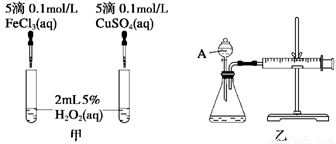
(2)定量分析:如圖乙所示,實驗時均以生成40 mL氣體為準,其他可能影響實驗的因素均已忽略。圖中儀器A的名稱為________,實驗中需要測量的數據是_________________。
(共14分)為研究鐵質材料與熱濃硫酸的反應,某學習小組用碳素鋼(即鐵和碳的合金)進行了以下探究活動:
[探究一]
(1)將已去除表面氧化物的鐵釘(碳素鋼)放入冷濃硫酸中,10分鐘后移入硫酸銅溶液中,片刻后取出觀察,鐵釘表面無明顯變化,其原因是____________。
(2)稱取碳素鋼6.0g放入15.0mL濃硫酸中,加熱,充分反應后得到溶液X并收集到混合氣體Y。
①甲同學認為X中除Fe3+之外還可能含有Fe2+。若要確認其中的Fe2+,應選用 (選填序號)。
A.KSCN溶液和氯水 B.鐵粉和KSCN溶液 C.濃氨水 D.酸性KMnO4溶液
②乙同學取560mL(標準狀況)氣體Y通入足量溴水中,發生SO2+Br2+2H2O===2HBr+H2SO4反應,然后加入足量BaCl2溶液,經適當操作后得干燥固體4.66g。由此推知氣體Y中SO2的體積分數為 。
[探究二]
根據上述實驗中SO2體積分數的分析,丙同學認為氣體Y中還可能含有Q1和Q2兩種氣體,其中Q1氣體,在標準狀況下,密度為0.0893g·L-1。為此設計了下列探究實驗裝置(圖中夾持儀器省略,假設有關氣體完全反應)。
(3)裝置B中試劑的作用是
(4)分析Y氣體中的Q2氣體是如何生成的 (用化學方程式表示)。
(5)為確認Q2的存在,需在裝置中添加洗氣瓶M于 (選填序號)。
A.A之前 B.A-B間 C.B-C間 D.C-D間
(6)如果氣體Y中含有Q1,預計實驗現象應是
(8分)為探究生活中兩種常見的有機物的性質,某同學設計如下實驗,請根據題目要求填寫下列空格:
(1)如圖1所示,試管中裝乙醇產生的氣體為 ;
(2)如圖2所示,把加熱的銅絲插入到裝有乙醇的試管中,聞到有刺激性氣味,該反應中產生的有機物為 ;
(3)用食醋浸泡有水垢(主要成分CaCO3)的水壺,可以清除水垢,說明醋酸的酸性 碳酸的酸性。(填“強于”或“弱于”)
(4)按如圖3所示裝置,甲試管中裝有乙酸、乙醇、濃硫酸,則在裝有飽和碳酸鈉溶液的乙試管上方可聞到有特殊香味的物質,該物質為 。
(14分)為研究盛裝濃硫酸的鐵質材料(碳素鋼)與濃硫酸的反應,某學習小組進行了以下探究活動:
[實驗]取一鐵釘放入一定體積濃硫酸中,加熱,充分反應后得到溶液X并收集到氣體Y。
①甲同學認為x中除Fe3+外還可能含有Fe2+。若要確認其中的Fe2+,應選用 (選填序號)
KSCN溶液和氯水 b.鐵粉和KSCN溶液 c.濃氨水 d.酸性:KMn04溶液
②為分析氣體成分,乙同學取448mL(標準狀況)氣體Y通人足量溴水中,發生的反應式 為:Br2+SO2+2H20====2HBr+H2S04,然后加入足量BaCl2溶液,經適當操作后得干燥 固體2.33 g
[提出猜想]
分析上述實驗中SO2的體積分數的結果,同學們認為Y中還可能含有其它氣體并作如下
猜測:
猜想一:Y氣體中可能含有H2;
猜想二:
猜想三:
[設計實驗,驗證猜想]
為驗證以上猜想,同學們準備用下列裝置設計探究實驗(裝置可重復使用,夾持儀器省
略)。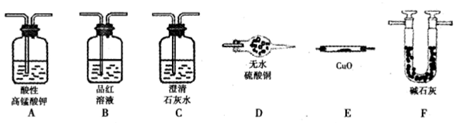
(1)實驗裝置連接次序為A→ → →F → →F
(2)裝置B中試劑作用是 。
(3)猜想一的理由是 (用化學方程式表示)。
(4)如果猜想一成立,預計實驗現象應該是 。
(共14分)為研究鐵質材料與熱濃硫酸的反應,某學習小組用碳素鋼(即鐵和碳的合金)進行了以下探究活動:
[探究一]
(1)將已去除表面氧化物的鐵釘(碳素鋼)放入冷濃硫酸中,10分鐘后移入硫酸銅溶液中,片刻后取出觀察,鐵釘表面無明顯變化,其原因是____________。
(2)稱取碳素鋼6.0g放入15.0mL濃硫酸中,加熱,充分反應后得到溶液X并收集到混合氣體Y。
① 甲同學認為X中除Fe3+之外還可能含有Fe2+。若要確認其中的Fe2+,應選用 (選填序號)。
A.KSCN溶液和氯水 B.鐵粉和KSCN溶液 C.濃氨水 D.酸性KMnO4溶液
② 乙同學取560mL(標準狀況)氣體Y通入足量溴水中,發生SO2+Br2+2H2O===2HBr +H2SO4反應,然后加入足量BaCl2溶液,經適當操作后得干燥固體4.66g。由此推知氣體Y中SO2的體積分數為 。
[探究二]
根據上述實驗中SO2體積分數的分析,丙同學認為氣體Y中還可能含有Q1和Q2兩種氣體,其中Q1氣體,在標準狀況下,密度為0.0893g·L-1。為此設計了下列探究實驗裝置(圖中夾持儀器省略,假設有關氣體完全反應)。

(3)裝置B中試劑的作用是
(4)分析Y氣體中的Q2氣體是如何生成的 (用化學方程式表示)。
(5)為確認Q2的存在,需在裝置中添加洗氣瓶M于 (選填序號)。
A.A之前 B.A-B間 C.B-C間 D.C-D間
(6)如果氣體Y中含有Q1,預計實驗現象應是
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com