
題目列表(包括答案和解析)
(14分)孔雀石的主要成分為Cu2(OH)2CO3,還含少量Fe、Si的化合物。實驗室以孔雀石為原料制備CuCl2·3H2O及CaCO3的步驟如下:
為解決有關問題,興趣小組同學查得有關物質沉淀的pH數據如下:
| 物質 | pH (開始沉淀) | pH(完全沉淀) |
| Fe(OH)3 | 1.9 | 3.2 |
| Fe(OH)2 | 7.0 | 9.0 |
| Cu(OH)2 | 4.7 | 6.7 |
⑴“除雜”時先通入足量Cl2將Fe2+氧化成Fe3+,再加入CuO固體調節溶液的pH至 (填寫范圍)。檢驗Fe(OH)3是否沉淀完全的實驗方案是 。
⑵操作X包括 、 、過濾和洗滌等。CuCl2·3H2O加熱灼燒的最終產物的化學式是 。
⑶某種胃藥片的治酸劑為CaCO3,該藥片中CaCO3質量分數的測定步驟如下:
a.配制0.1mol·L-1的HCl溶液和0.1mol·L-1的NaOH溶液各250mL。
b.取0.1g磨碎后的胃藥于錐形瓶中。
c.向錐形瓶內加入25.00mL 0.1 mol·L-1的HCl溶液。
d.以酚酞為指示劑,用0.1mol·L-1的NaOH溶液滴定,至達到滴定終點。
e.重復bcd三步的操作2次。
① 操作c中量取鹽酸體積的儀器是 。
② 若洗滌后的堿式滴定管未用NaOH溶液潤洗,則所測CaCO3的質量分數將 (選填“偏大”、“偏小”或“無影響”)。
③ 若滴定中NaOH溶液的平均用量為15.00mL,則胃藥中碳酸鈣的質量分數為 。
(14分) 電池的發明和應用是化學家們對人類社會的重要貢獻之一。
Ⅰ.每一次化學電池技術的突破,都帶來了電子設備革命性的發展。最近,我國在甲醇燃料電池的相關技術上獲得了新突破,原理如下圖1所示。
(1)請寫出從C口通入O2發生的電極反應式 。
(2)以石墨做電極電解飽和食鹽水,如下圖2所示。電解開始后在 的周圍(填“陰極”或“陽極”)先出現紅色。假設電池的理論效率為80%(電池的理論效率是指電池產生的最大電能與電池反應所釋放的全部能量之比),若消耗6.4g甲醇氣體,外電路通過的電子個數為 (保留兩位有效數字,NA取6.02×1023)。

Ⅱ.隨著電池使用范圍的日益擴大,廢舊電池潛在的污染已引起社會各界的廣泛關注。
(1)電池生產企業排放的工業廢水中常含有Cu2+等重金屬離子,直接排放會造成污染,目前在工業廢水處理過程中,依據沉淀轉化的原理,常用FeS等難溶物質作為沉淀劑除去這些離子。已知室溫下Ksp(FeS)=6.3×10-18mol2·L-2,Ksp(CuS)=1.3×10-36mol2·L-2。請用離子方程式說明上述除雜的原理 。
(2)工業上為了處理含有Cr2O72-的酸性工業廢水,用綠礬(FeSO4·7H2O)把廢水中的六價鉻離子還原成三價鉻離子,再加入過量的石灰水,使鉻離子轉變為Cr(OH)3沉淀。
①氧化還原過程的離子方程式為 。
②常溫下,Cr(OH)3的溶度積Ksp=1×10-32 mol4·L-4,溶液的pH至少為 ,才能使Cr3+沉淀完全。
③現用上述方法處理100m3含鉻(+6價)78mg•L-1的廢水,需用綠礬的質量為 kg。(寫出主要計算過程)
(14分)孔雀石的主要成分為Cu2(OH)2CO3,還含少量Fe、Si的化合物。實驗室以孔雀石為原料制備CuCl2·3H2O及CaCO3的步驟如下:
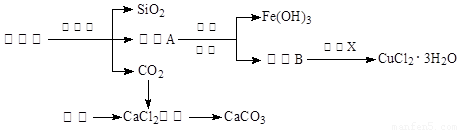
為解決有關問題,興趣小組同學查得有關物質沉淀的pH數據如下:
|
物質 |
pH (開始沉淀) |
pH(完全沉淀) |
|
Fe(OH)3 |
1.9 |
3.2 |
|
Fe(OH)2 |
7.0 |
9.0 |
|
Cu(OH)2 |
4.7 |
6.7 |
⑴“除雜”時先通入足量Cl2將Fe2+氧化成Fe3+,再加入CuO固體調節溶液的pH至 (填寫范圍)。檢驗Fe(OH)3是否沉淀完全的實驗方案是 。
⑵操作X包括 、 、過濾和洗滌等。CuCl2·3H2O加熱灼燒的最終產物的化學式是 。
⑶某種胃藥片的治酸劑為CaCO3,該藥片中CaCO3質量分數的測定步驟如下:
a.配制0.1mol·L-1的HCl溶液和0.1mol·L-1的NaOH溶液各250mL。
b.取0.1g磨碎后的胃藥于錐形瓶中。
c.向錐形瓶內加入25.00mL 0.1 mol·L-1的HCl溶液。
d.以酚酞為指示劑,用0.1mol·L-1的NaOH溶液滴定,至達到滴定終點。
e.重復bcd三步的操作2次。
① 操作c中量取鹽酸體積的儀器是 。
② 若洗滌后的堿式滴定管未用NaOH溶液潤洗,則所測CaCO3的質量分數將 (選填“偏大”、“偏小”或“無影響”)。
③ 若滴定中NaOH溶液的平均用量為15.00mL,則胃藥中碳酸鈣的質量分數為 。
(14分)孔雀石的主要成分為Cu2(OH)2CO3,還含少量Fe、Si的化合物。實驗室以孔雀石為原料制備CuCl2·3H2O及CaCO3的步驟如下:
為解決有關問題,興趣小組同學查得有關物質沉淀的pH數據如下:
| 物質 | pH (開始沉淀) | pH(完全沉淀) |
| Fe(OH)3 | 1.9 | 3.2 |
| Fe(OH)2 | 7.0 | 9.0 |
| Cu(OH)2 | 4.7 | 6.7 |
(14分)欲用濃硝酸法(測定反應后生成氣體的量)測定某銅銀合金中銅的質量分數。資料表明:①反應中除生成NO2氣體外還有少量的NO生成;②常溫下N02與N2O4混合存在,在低于0℃時幾乎只有無色N2O4液體或晶體存在。為完成測定并驗證有NO生成,有人設計下圖實驗裝置。
(1)實驗開始前要先打開A部分的活塞K1,持續通一段時間的氮氣再關閉K1,這樣做的目的是_____________________________________________________________。
(2)裝置B瓶的作用是__________________________________________________。
(3)A中反應停止后,打開D中的活塞K2并通人氧氣,若反應中確有NO產生,則D中應出現的現象是________________;實驗發現,通人氧氣溫度的高低對實驗現象有較大影響,則為了便于觀察應通人_______________(填“冷”或“熱”)的氧氣。
(4)為了減少測量誤差,在A中反應完成和D中出現現象后,還應繼續進行的操作是__________________________________________________________。
(5)實驗測得下列數據:所用銅銀合金質量為15.0 g,濃硝酸的體積為40 mL,濃度為13.5mol·L-1。實驗后:A中溶液體積為40mL,H+濃度為1.0mol·L-1。若設反應中硝酸既無揮發也無分解,則:
①參加反應的硝酸的物質的量為______________;
②若已測出反應后E裝置的生成物含氮元素的質量,則為確定合金中銅的質量分數,還需要測定的數據是__________。
(6)實驗中只測定銅的質量分數,不驗證NO的產生,則在銅銀合金與硝酸反應后,只需簡單的實驗操作就可以達到目的,請簡述實驗過程________________________。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com