
題目列表(包括答案和解析)
(16分)以煤為原料,經過化學加工使煤轉化為氣體、液體、固體燃料以及各種化工產品的工業叫煤化工。
(1)將水蒸氣通過紅熱的碳即可產生水煤氣。反應為:
C(s)+H2O(g)  CO(g)+H2(g) ΔH=+131.3 kJ?mol-1,
CO(g)+H2(g) ΔH=+131.3 kJ?mol-1,
①該反應在常溫下 自發進行(填“能”與“不能”);
②恒溫,在容積可變的密閉容器中,進行如上可逆反應。一段時間后,下列物理量不發生變化時,能表明該反應已達到平衡狀態的有
Ⅰ混合氣體的密度; Ⅱ容器內氣體的壓強;
Ⅲ混合氣體的總物質的量; ⅣCO物質的量濃度
A.只有Ⅳ B.只有Ⅰ和Ⅳ C.只有Ⅱ和Ⅲ D.Ⅰ、Ⅲ和Ⅳ
(2)水煤氣再進一步反應可制取氫氣。反應為H2O(g)+CO(g) H2(g)+CO2(g),某溫度下該反應的平衡常數K= 4/9。該溫度下在甲、乙、丙三個恒容密閉容器中,只投入H2(g)和CO2(g),其起始濃度如下表所示。下列判斷不正確的是 。
H2(g)+CO2(g),某溫度下該反應的平衡常數K= 4/9。該溫度下在甲、乙、丙三個恒容密閉容器中,只投入H2(g)和CO2(g),其起始濃度如下表所示。下列判斷不正確的是 。
| 起始濃度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
 CH3OH(g)+H2O(g) ,右圖表示該反應進行過程中能量(單位為kJ?mol—1)的變化。在體積為1 L的恒容密閉容器中,充入1mol CO2和3mol H2反應
CH3OH(g)+H2O(g) ,右圖表示該反應進行過程中能量(單位為kJ?mol—1)的變化。在體積為1 L的恒容密閉容器中,充入1mol CO2和3mol H2反應
 CO(g)+H2(g) ΔH=+131.3 kJ?mol-1,
CO(g)+H2(g) ΔH=+131.3 kJ?mol-1, H2(g)+CO2(g),某溫度下該反應的平衡常數K= 4/9。該溫度下在甲、乙、丙三個恒容密閉容器中,只投入H2(g)和CO2(g),其起始濃度如下表所示。下列判斷不正確的是 。
H2(g)+CO2(g),某溫度下該反應的平衡常數K= 4/9。該溫度下在甲、乙、丙三個恒容密閉容器中,只投入H2(g)和CO2(g),其起始濃度如下表所示。下列判斷不正確的是 。| 起始濃度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
 CH3OH(g)+H2O(g) ,右圖表示該反應進行過程中能量(單位為kJ?mol—1)的變化。在體積為1 L的恒容密閉容器中,充入1mol CO2和3mol H2反應
CH3OH(g)+H2O(g) ,右圖表示該反應進行過程中能量(單位為kJ?mol—1)的變化。在體積為1 L的恒容密閉容器中,充入1mol CO2和3mol H2反應
已知可逆反應:![]()
請回答下列問題:
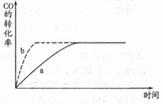
(1)圖中曲線a表示反應進行過程中CO的轉化率隨時間變化的關系,若要改變起始條件,使反應過程按b曲線進行,可采取的措施是_____ (填序號)
A.升高溫度 B.加催化劑 C.加壓 D.增加CO的用量 E.擴大容器的體積
(2)830K時,若起始時c(CO)=2m01.L-1,c(H20)=3m01.L-1,經5min后該反應達到平衡,此時CO的轉化率為60%,該時間段內,此反應的平均速率v(CO)=____;若起始時,c(CO)=4m01.L-1,c(H2O)____,達到平衡時,反應體系中各組分的百分含量與上述情況相同,此時該反應的化學平衡常數為___。
(3)830K時,若起始時,c(CO)=2m01.L-1,c(H2O)=6m01.L-1,達到化學平衡后,水蒸氣的轉化率為____。
(4)TK時,起始濃度為:c(CO)=am01.L-1,c(H2O)=bm01.L-1,達到化學平衡后,c(H2)=cm01.L-1;若a、b、c之間的關系滿足:ab>(a+b)?c,則此時T____830。(填“大于”“等于”或“小于”)
|
在溫度和壓強不變時,1 L NO2高溫分解(2NO2 | |
| [ ] | |
A. |
40% |
B. |
20% |
C. |
60% |
D. |
5% |
|
在溫度和壓強不變時,1 L NO2高溫分解(2NO2 | |
| [ ] | |
A. |
40% |
B. |
20% |
C. |
60% |
D. |
5% |
必考卷
第Ⅰ卷
一、選擇題:每小題3分,共45分
題號
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
答案
A
C
D
C
C
D
B
A
B
B
A
A
D
D
C
第Ⅱ卷
二、填空題:
16.(10分)
每空2分,化學方程式、離子方程式沒有配平不給分,條件未標扣1分,沉淀、氣體符
號未標不扣分。
(1)O
(2)
(3)


(4)
(5)O=C=O
17.(10分)
每空2分,化學方程式、離子方程式沒有配平不給分,條件未標扣1分,沉淀、氣體符
號未標不扣分。
(1) 
(2)第三周期第ⅥA族
(3)氧,B
(4)
18.(12分)
實驗一
(1)膠頭滴管、250mL容量瓶 (每空1分,共2分)
(2)0.2000mol?L (2分)
(2分)
實驗二
(1)0.0100mo1?L 醋酸的pH大于2或醋酸稀釋10倍時,pH的變化值小于l
醋酸的pH大于2或醋酸稀釋10倍時,pH的變化值小于l
(3分,其它合理答案酌情給分)
(2)增大 、(2分)
實驗三
答:用pH計(或pH試紙)測定相同濃度的醋酸在幾種不同'溫度時的pH(3分其他合
19.(10分)
每空2分,其它合理答案酌情給分
(1)
(2)CD
(3)
(4)甲醇、氫氧化鈉、水(答出甲醇即給2分) 
選考卷
20(A).(13分)
(1)分子晶體 (2分)
(2)沒有 (2分)
(3) . (3分)
. (3分)
(4)O N C (2分)
(5) 鍵和
鍵和 鍵 (2分)
鍵 (2分)
(6)CO中斷裂第一個 鍵消耗的能量(273
kJ?mol
鍵消耗的能量(273
kJ?mol )比N
)比N 中斷裂第一個
中斷裂第一個 鍵消耗的能量(523.3kJ?mol
鍵消耗的能量(523.3kJ?mol )小,CO的第一個鍵較容易斷裂,因此CO較活潑。(其它合理答案酌情給分)(2分)
)小,CO的第一個鍵較容易斷裂,因此CO較活潑。(其它合理答案酌情給分)(2分)
20(B).(13分)
(1)羥基,羧基(2分)
(2)消去反應(2分)
(3) 
(4) 
(5) 4 (2分)
(6) 
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com