
題目列表(包括答案和解析)
| 容器 編號 |
起始時各物質物質的量/mol | 達平衡時體系能量的變化 | ||
| XY2 | Y2 | XY3 | ||
| ① | 2 | 1 | 0 | 放熱 0.25 Q kJ |
| ② | 1.2 | 0.6 | 0.8 | |
A、容器①、②中反應的平衡常數均為
| ||
| B、達到平衡時,兩個容器中Y2的物質的量濃度均為1.5 mol?L-1 | ||
| C、容器②中反應達到平衡時放出的熱量為0.15 Q kJ | ||
| D、若容器①的其他條件不變,恒壓下通入稀有氣體,則達到平衡時放出的熱量小于0.25 Q kJ |
化學在能源開發與利用中起著十分關鍵的作用。氫氣是一種新型的綠色能源,又是一種重要的化工原料。
I.氫氧燃料電池能量轉化率高,具有廣闊的發展前景。現用氫氧燃料電池進行如圖實驗(圖中所用電極均為惰性電極):

(1)對于氫氧燃料電池中,下列表達不正確的是________
A.a電極是負極,OH-移向正極
B.b電極的電極反應為:O2+2H2O+4e-=4OH-
C.電池總反應式為:2H2+O2 2H2O
2H2O
D.電解質溶液的pH保持不變
E.氫氧燃料電池是一種不需要將還原劑和氧化劑全部儲藏在電池內的新型發電裝置
(2)上圖裝置中盛有100mL、0.1mol·L—1AgNO3溶液,當氫氧燃料電池中消耗氫氣112mL(標準狀況下)時,則此時上圖裝置中溶液的pH=________(溶液體積變化忽略不計)
II.氫氣是合成氨的重要原料。工業上合成氨的反應是:
N2(g)+3H2(g) 2NH3(g)
ΔH=-92.20 kJ·mol-1。
2NH3(g)
ΔH=-92.20 kJ·mol-1。
(1)下列事實中,不能說明上述可逆反應已達到平衡的是________
①單位時間內生成2n mol NH3的同時生成3n mol H2
②單位時間內生成n mol N—H的同時生成n mol N≡N
③用N2、H2、NH3的物質的量濃度變化表示的反應速率之比為1︰3︰2
④N2、H2、NH3的體積分數不再改變
⑤混合氣體的平均摩爾質量不再改變
⑥混合氣體的總物質的量不再改變
(2)已知合成氨反應在某溫度下2L的密閉容器中進行,測得如下數據:
|
時間(h) 物質的量(mol) |
0 |
1 |
2 |
3 |
4 |
|
N2 |
1.50 |
n1 |
1.20 |
n3 |
1.00 |
|
H2 |
4.50 |
4.20 |
3.60 |
n4 |
3.00 |
|
NH3 |
0 |
0.20 |
n2 |
1.00 |
1.00 |
根據表中數據計算:
反應進行到2小時時放出的熱量為________
0~1小時內N2的平均反應速率________mol·L-1·h-1;
③此條件下該反應的化學平衡常數K=________(保留兩位小數)
④反應達到平衡后,若往平衡體系中再加入N2、H2和NH3各1.00mol,化學平衡將向________ 方向移動(填“正反應”或“逆反應”、“不移動”)。
相同溫度下,體積均為0.5 L的兩個恒容密閉容器中發生可逆反應:
2XY2(g)
+ Y2(g)  2XY3(g) △H=-Q kJ·mol-1(Q>0)
2XY3(g) △H=-Q kJ·mol-1(Q>0)
實驗測得反應在起始、達到平衡時的有關數據如下表所示:
|
容器 編號 |
起始時各物質物質的量/mol |
達平衡時體系能量的變化 |
||
|
XY2 |
Y2 |
XY3 |
||
|
① |
2 |
1 |
0 |
放熱 0.25 Q kJ |
|
② |
1.2 |
0.6 |
0.8 |
|
下列敘述不正確的是
A.容器①、②中反應的平衡常數均為1/13.5
B.達到平衡時,兩個容器中Y2的物質的量濃度均為1.5 mol·L-1
C.容器②中反應達到平衡時放出的熱量為0.15 Q kJ
D.若容器①的其他條件不變,恒壓下通入稀有氣體,則達到平衡時放出的熱量小于0.25 Q kJ
相同溫度下,體積均為0.5 L的兩個恒容密閉容器中發生可逆反應:
2XY2(g)+Y2(g)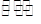 2XY3(g)
2XY3(g)
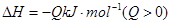
實驗測得反應在起始、達到平衡時的有關數據如下表所示:
|
容器 |
起始時各物質物質的/mol |
達平衡時體系能量的變化 |
||
|
編號 |
XY2 |
Y2 |
XY3 |
|
|
① |
2 |
1 |
0 |
放熱0.25QkJ |
|
② |
1.2 |
0.6 |
0.8 |
|
下列敘述不正確的是
A.達到平衡時,①和②兩容器中氣體的平均相對分子質量相同
B.容器②中反應達到平衡時放出的熱量為0.15 Q kJ
C.達到平衡時,兩個容器中Y2的物質的量濃度均為1.5 mol·L-1
D.若容器①的其他條件不變,只增加1mol稀有氣體,則達到平衡時放出的熱量等于0.25 Q kJ
工業上合成氨的反應是:N2(g)+3H2(g)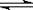 2NH3(g) ΔH=-92.20 kJ·mol-1。
2NH3(g) ΔH=-92.20 kJ·mol-1。
(1)下列事實中,不能說明上述可逆反應已達到平衡的是________
①單位時間內生成2n mol NH3的同時生成3n mol H2
②單位時間內生成n mol N—H的同時生成n mol N≡N
③用N2、H2、NH3的物質的量濃度變化表示的反應速率之比為1︰3︰2
④N2、H2、NH3的體積分數不再改變
⑤混合氣體的平均摩爾質量不再改變
⑥混合氣體的總物質的量不再改變
(2)已知合成氨反應在某溫度下2L的密閉容器中進行,測得如下數據:
|
時間(h) 物質的量(mol) |
0 |
1 |
2 |
3 |
4 |
|
N2 |
1.50 |
n1 |
1.20 |
n3 |
1.00 |
|
H2 |
4.50 |
4.20 |
3.60 |
n4 |
3.00 |
|
NH3 |
0 |
0.20 |
N2 |
1.00 |
1.00 |
根據表中數據計算:
①反應進行到2小時時放出的熱量為________
②0~1小時內N2的平均反應速率________ mol·L-1·h-1;
③此條件下該反應的化學平衡常數K= ________ (保留兩位小數)
④反應達到平衡后,若往平衡體系中再加入N2、H2和NH3各1.00mol,化學平衡將向________ 方向移動(填“正反應”或“逆反應”、“不移動”)。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com