(10分)工業上目前使用兩種方法制取乙醛:(1)乙炔水化法;(2)乙烯氧化法。下列兩表提供生產過程中原料、反應條件、原料平衡轉化率、產量等有關的信息情況:
表一:原料、反應條件、平衡轉化率、日產量
| 乙炔水化法
| 乙烯氧化法
|
原料
| 乙炔、水
| 乙烯、空氣
|
反應條件
| HgSO4、100~125℃
| PdCl2-CuCl2、100~125℃
|
平衡轉化率
| 乙炔平衡轉化率90%左右
| 乙烯平衡轉化率80%左右
|
日產量
| 2.5噸(某設備條件下)
| 3.6噸(相同設備條件下)
|
表二:原料來源生產工藝
| 原料生產工藝過程
|
乙炔
| 
|
乙烯
| 來源于石油裂解氣
|
根據上述兩表,回答下列問題:
(1)寫出下列化學方程式:
a.乙炔水化法制乙醛__________________________________________________。
b.乙烯氧化法制乙醛______________________________________________。
(2)從兩表中分析,現代工業上乙烯氧化法逐步取代乙炔水化法(從環境、原料來源、產率和產量、能耗等角度),分析可能的原因:________________________________。
(3)從化學反應速率角度分析,在相同條件下,兩種制取乙醛的方法哪種快?
___________________________________________________________________。
(4)若將上述兩種方法的反應條件,均增加“100atm”,原料平衡轉化率_______(填增大、減小、不變);而實際生產中不采用的理由是_____________________________。
(5)若乙烯由石油裂化(裂化氣混合氣體的平均化學式C
nH
m、m>2n),進一步完全催化裂解而來,得到體積百分含量分別為:甲烷:5%、乙烯:40%、丙烯:10%、其余為丁二烯和氫氣(氣體體積均在同溫同壓下測定)。若得到40mol乙烯,求:能夠得到丁二烯和氫氣的物質的量各為多少?

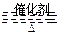 2SO3(正反應放熱)。反應達到平衡后,將容器中的混合氣體通過過量NaOH溶液,氣體體積減少了21.28L;再將剩余氣體通過焦性沒食子酸的堿性溶液吸收O2,氣體的體積又減少了5.6L(以上氣體體積均為標準狀況下的體積)。(計算結果保留一位小數)
2SO3(正反應放熱)。反應達到平衡后,將容器中的混合氣體通過過量NaOH溶液,氣體體積減少了21.28L;再將剩余氣體通過焦性沒食子酸的堿性溶液吸收O2,氣體的體積又減少了5.6L(以上氣體體積均為標準狀況下的體積)。(計算結果保留一位小數)