
題目列表(包括答案和解析)
(15分)、對于弱酸,在一定溫度下達到電離平衡時,各微粒的濃度存在一種定量的關系。若25℃時有HA H++A―,則K=
H++A―,則K= 。式中:K為電離平衡常數,只與溫度有關,c為各微粒的平衡濃度。下表是幾種常見弱酸的電離平衡常數(25℃)。
。式中:K為電離平衡常數,只與溫度有關,c為各微粒的平衡濃度。下表是幾種常見弱酸的電離平衡常數(25℃)。
回答下列問題:
(1)當升高溫度時,K值____(填“變大”“變小”或“不變”)。
(2)在溫度相同時,各弱酸的K值不同,那么K值的大小與酸性的相對強弱有何關系? ____ ________。
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、
H2PO4-、HPO42-都看做是酸,其中酸性最強的是_ ,最弱的是_ __。
(4)同一多元弱酸的K1、K2、K3之間存在著數量上的規律,此規律是_____________,產生此規律的原因是_____________ ___。
(5) Na2CO3溶液呈_ _(填“酸性”“堿性”或“中性”),其原因(用離子方程式表示)是_ 。
(6)已知NaH2PO4溶液呈酸性,則該溶液中c(H3PO4)____c(HPO42-)(填“大于”或“小于” )。
(15分)、對于弱酸,在一定溫度下達到電離平衡時,各微粒的濃度存在一種定量的關系。若25℃時有HA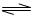 H++A―,則K=
H++A―,則K= 。式中:K為電離平衡常數,只與溫度有關,c為各微粒的平衡濃度。下表是幾種常見弱酸的電離平衡常數(25℃)。
。式中:K為電離平衡常數,只與溫度有關,c為各微粒的平衡濃度。下表是幾種常見弱酸的電離平衡常數(25℃)。

回答下列問題:
(1)當升高溫度時,K值____(填“變大”“變小”或“不變”)。
(2)在溫度相同時,各弱酸的K值不同,那么K值的大小與酸性的相對強弱有何關系? ____ ________。
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、
H2PO4-、HPO42-都看做是酸,其中酸性最強的是_ ,最弱的是_ __。
(4)同一多元弱酸的K1、K2、K3之間存在著數量上的規律,此規律是_____________,產生此規律的原因是_____________ ___。
(5) Na2CO3溶液呈_ _(填“酸性”“堿性”或“中性”),其原因(用離子方程式表示)是_ 。
(6)已知NaH2PO4溶液呈酸性,則該溶液中c(H3PO4)____c(HPO42-)(填“大于”或“小于” )。
有主族元素形成的3種離子Xn+,Ym-,Zm+,已知m>n,Xn+比Zm+多一個電子層,Z與Y同周期,三種原子的M層電子數均為偶數,下列推斷不正確的是
A.原子半徑X>Y>Z
B.離子半徑Ym->Xn+>Zm+
C.三種元素最高價氧化物對應水化物堿性依次減弱,酸性依次增強的順序是X,Z,Y
D.Y在自然界中沒有游離態,可形成原子晶體
| A.原子半徑X>Y>Z |
| B.離子半徑Ym->Xn+>Zm+ |
| C.三種元素最高價氧化物對應水化物堿性依次減弱,酸性依次增強的順序是X,Z,Y |
| D.Y在自然界中沒有游離態,可形成原子晶體 |
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com