
題目列表(包括答案和解析)
| C(A-).C(H+) |
| C(HA) |
| C(A-).C(H+) |
| C(HA) |
| 酸 | 電離方程式 | 電離平衡常數K |
| CH3COOH | CH3COOH?CH3COOH-+H+ | 1.76×10-5 |
| H2CO3 | H2CO3?H++HCO3- HCO3-?H++HCO32- |
K1=4.31×10-7 K2=5.61×10-11 |
| H2S | H2S?H++HS- HS-?H++S2- |
K1=9.1×10-8 K2=1.1×10-12 |
| H3PO4 | H3PO4?H++H2PO4- H2PO4-H++HPO42- HPO42-?H++PO43- |
K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 |
| 酸 | 電離方程式 | 電離平衡常數K |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.76×10-5 |
| HClO | HClO?ClO-+H+ | 2.95×10-8 |
| H2S | H2S?H++HS- HS-?H++S2- |
K1=9.1×10-8 K2=1.1×10-12 |
| H2CO3 | H2CO3?H++HCO3- HCO3-?H++CO32- |
K1=4.31×10-7 K2=5.61×10-11 |
| H3PO4 | H3PO4?H++H2PO4- H2PO4-?H++HPO42- HPO42-?H++PO43- |
K1=7.1×10-3 K2=6.3×10-8 K3=4.2×10-13 |
| 酸 | 電離方程式 | 電離平衡常數Ka |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.76×10-5 |
| H2S | H2S?H++HS- HS-?H++S2- |
Ka1=9.1×10-8 Ka2=1.1×10-12 |
| H3PO4 | H3PO4?H++H2PO4- H2PO4-?H++HPO42- HPO42-?H++PO43- |
Ka1=7.52×10-3 Ka2=6.23×10-8 Ka3=2.20×10-13 |
對于弱酸,在一定溫度下達到電離平衡時,各微粒的濃度存在一種定量的關系.下表是25℃時幾種常見弱酸的電離平衡常數
| 酸 | 電離方程式 | 電離平衡常數K |
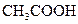 | 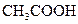  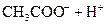 |  |
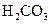 |  | 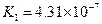 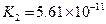 |
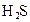 | 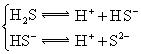 | 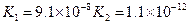 |
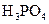 | 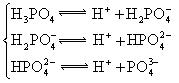 | 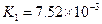 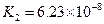 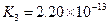 |
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com