
題目列表(包括答案和解析)
3.下列各物質中,能將MgSO4溶液、Na2CO3溶液、BaCl2溶液一次就可以鑒別開的是( )
A.AgNO3溶液 B.NaOH溶液 C.Ca(OH)2溶液 D.H2SO4溶液
分析:本題考查的是SO42-、Cl-、CO32-的鑒別方法及學生綜合分析解決問題的能力。此題還涉及某些鹽和堿的溶解性,要求學生在熟記這些知識點基礎上根據提問“一次鑒別”三種物質,應產生不同現象,一般為一種沉淀、一種氣體、一種無變化或無明顯現象,最易找出可能有氣體產生的是Na2CO3溶液與稀硫酸的反應且稀硫酸與MgSO4溶液混合無變化,與BaCl2溶液混合會產生白色沉淀,所以答案選擇D。
填空:
有下列幾種物質:a.鹽酸 b.硫酸 c.熟石灰 d.硫酸銅 e.純堿 f.食鹽
請選擇合適的標號(a-f)填空(不得重復)
(1)用來清除鐵銹的物質____ (2)常用降低土壤酸性的是____
(2)在日常生活中用做調味劑的是____ (4)少量存于胃液中幫助消化的是___
(5)農業上用于配制波爾多液的是____ (6)做饅頭時用于除去面團發酵生成的酸的是____
分析:此題的測試點是常見的酸、堿、鹽的用途,屬綜合題型,重點考查學生的記憶能力,但難度不大。答案應為(1)b (2)c (3)f (4)a (5)d (6)e
附錄4-2《酸、堿、鹽》練習
選擇:
2.下列物質中能與稀硫酸發生中和反應,又能產生白色沉淀的是( )
A.Ba(OH)2 B.K2CO3 C.Mg(OH)2 D.BaCl2
分析:此題考察酸的通性及復分解反應發生條件,綜合性較強,根據酸的通性及復分解反應發生的條件可知四種物質都能與硫酸反應,但若要產生白色沉淀只能從A、D中選,而只有A與稀硫酸的反應為中和反應,故此題選擇A。
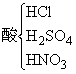
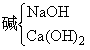
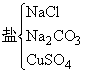
附錄4-1《酸、堿、鹽》部分典型例題
例題:
選擇題:
1.下列物質中能與鹽酸反應并有氣體生成的是( )
A.鋁 B.銀 C.銅 D.汞
分析:此題的測試點是金屬活動性順序的應用,排在氫前邊的金屬能置換出酸中的氫,而排在氫后邊的金屬則不能,故答案為A。
(五)板書設計
復習《酸、堿、鹽》
(四)鞏固深化:
1.學生小結:本節主要內容
2.練習(見附錄4-1)
3.布置作業:(附錄4-2)深化本節內容
(三)討論:
書寫酸、堿、鹽之間的復分解反應方程式應注意哪些問題?
學生分組討論,培養發散思維能力及獨立思考習慣。
教師引導學生總結歸納,培養歸納、思維能力。
(二)實驗啟發、探索新知:
1.常見的酸、堿、鹽
教師:提供學生實驗所需儀器藥品,并指導學生正確實驗,培養學生實驗能力。
學生:①討論:常見酸、堿、鹽的鑒別方法
②實驗探索鑒別的最佳方案
通過實驗探索得到常見的酸、堿、鹽之間的相同點和不同點及它們的性質的理解。
2.酸、堿、鹽的性質:
教師:投影性質并指導學生完成有關習題,培養學生解決實際問題的能力和分析能力。
學生:思考、口答,并獨立完成習題,學會用化學知識解決實際問題。
3.金屬活動性順序
學生實驗:(1)①Fe+H2SO4 ②Zn+H2SO4 ③Cu+H2SO4
(2)①Zn+CuSO4 ②Cu+AgNO3
并根據實驗探究:(1)金屬活動性順序及應用
(2)金屬與酸反應,金屬與鹽反應的條件
教師:引導學生實驗,注意訓練學生的思維能力,引導學生注意知識間的聯系。
(一)復習提問,引入復習
教師:提出問題①我們學過哪些常見的酸、堿、鹽。②如何鑒別它們(有哪些方法)
學生:思考,探究得到結論并回答
投影、滴管、滴瓶、試管等。
教學重點:酸、堿、鹽的性質。
教學難點:酸、堿、鹽的性質的應用。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com