
科目: 來源: 題型:
物質的量相同的戊烷,苯和苯酚完全燃燒需要氧氣的物質的量依次是x,y,Z,則x,y,Z的關系正確的是 ( )
A.x>y>z B.y>z>x C.z>y>x D.y>x>z
查看答案和解析>>
科目: 來源: 題型:
濃度為0.1mol/L的8種溶液:①HNO3 ②H2SO4③HCOOH ④Ba(OH)2 ⑤NaOH ⑥CH3COONa ⑦KCl ⑧NH4Cl溶液pH值由小到大的順序是(填寫編號)____________。
查看答案和解析>>
科目: 來源: 題型:
下列說法正確的是 ( )
A.電離平衡常數受溶液濃度的影響
B.電離平衡常數可以表示弱電解質的相對強弱
C.電離常數大的酸溶液中c(H+)一定比電離常數小的酸中大
D.H2CO3的電離常數表達式:![]()
查看答案和解析>>
科目: 來源: 題型:
二氧化氯(ClO2)作為一種高效強氧化劑已被聯合國世界衛生組織(WHO)列為AI級安全消毒劑,常溫下二氧化氯為黃綠色或橘黃色氣體,易溶于水,易與堿液反應,其性質非常不穩定,溫度過高、二氧化氯的水溶液質量分數高于30%等均有可能引起爆炸。某研究小組設計下圖所示實驗裝置制備ClO2。

現稱取12.25gKClO3和9g草酸(H2C2O4)放入燒瓶中,然后再加入足量的稀硫酸,水浴加熱。
回答下列問題:
(1)已知反應后的產物中有ClO2、CO2和一種酸式鹽,該反應的化學方程式為 。
(2)在反應開始之前將燒杯中的水加熱到80℃,然后停止加熱,并使其保持在60℃~
80℃之間。這樣操作的目的是 ,
圖示裝置中缺少的一種必須的玻璃儀器是 。
(3)A裝置用于吸收產生的二氧化氯,其中最好盛放 (填序號)。
a. 50mL 60℃的溫水 b. 50mL冰水 c. 50mL飽和食鹽水 d. 50mL NaOH溶液
(4)本實驗所制得的二氧化氯水溶液質量分數約為 。(小數點后保留兩位)
(5)二氧化氯可迅速氧化硫化物,以除去有機硫產生的臭味,改善水產養殖水體的水質。取適量二氧化氯溶液加入到硫化氫溶液中,再向其中加入少量氯化鋇溶液,發現有白色沉淀生成。硫化氫溶液與二氧化氯發生反應的離子方程式為 。
查看答案和解析>>
科目: 來源: 題型:
能源問題是人類社會面臨的重大課題,甲醇是未來重要的能源物質之一。
![]() (1)合成甲醇的反應為:CO(g)+2H2(g) CH3OH(g);△H
(1)合成甲醇的反應為:CO(g)+2H2(g) CH3OH(g);△H
如圖表示某次合成實驗過程中甲醇的體積分數 φ(CH3OH)與反應溫度的關系曲線,
則該反應的△H 0(填“>、< 或 = ”)
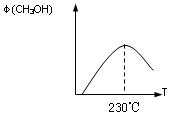
(2)若在230℃時,平衡常數K=1。若其它條件不變,將溫度升高到500℃時,達到平衡時,K 1 (填“>、< 或 = ”)
(3)在某溫度下,向一個容積不變的密閉容器中通入2.5mol CO和7.5mol H2,達到平衡時CO的轉化率為90%,此時容器內的壓強為開始時的 倍。
(4)利用甲醇燃料電池設計如圖所示的裝置:
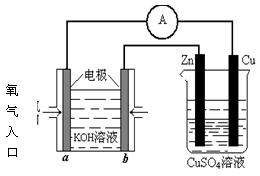
則該裝置中Cu極為 極;寫出b極的電極反應式
當銅片的質量變化為12.8 g時:a極上消耗的O2在標準狀況下的體積為 L。
(5)工業中常將BaSO4轉化為BaCO3后,再將其制成各種可溶性的鋇鹽(如:BaCl2)。
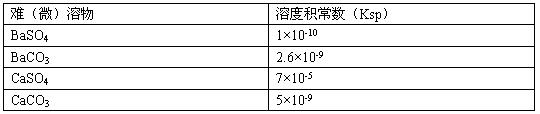
具體做法是用飽和的純堿溶液浸泡BaSO4粉末,并不斷補充純堿,最后BaSO4轉化為BaCO3。現有足量的BaSO4懸濁液,在該懸濁液中加純堿粉末并不斷攪拌,為使SO42-物質的量濃度達到0.0lmol·L-1以上,則溶液中CO32-物質的量濃度應≥ mol·L-1
查看答案和解析>>
科目: 來源: 題型:
主族元素W、X、Y、Z位于同一周期,原子序數依次增大,W、X是金屬元素.Y、Z是非金屬元素。W、X的最高價氧化物對應的水化物可以相互反應,W與Y可形成化合物W2Y,Y的最外層電子數是核外電子層數的2倍。下列說法正確的是
A.Y的氣態氧化物比z的氣態氫化物穩定
B.W的最高價氧化物對應的水化物是已知最強的堿
C.Y單質和氧氣、氫氣都能發生化合反應,且產物都具有還原性
D.W、X、Y、Z四種元素的原子半徑由小到大的順序是:W<X<Y<Z
查看答案和解析>>
科目: 來源: 題型:
為了防治環境污染并對尾氣進行綜合利用,某硫酸廠用氨水吸收尾氣中的SO2,再向吸收液中加入濃硫酸,以制取高濃度的SO2及(NH4)2SO4和NH4HSO4固體。
為測定上述(NH4)2SO4和NH4HSO4固體混合物的組成,現稱取該樣品四份,分別加入相同濃度的NaOH溶液各40.00 mL,加熱至1200C左右,使氨氣全部逸出[(NH4)2SO4和NH4HSO4的分解溫度均高于200℃],測得有關實驗數據如下(氣體體積均折算到標準狀況的體積):

(1)實驗過程中有關反應的離子方程式為: 。
(2)計算用1.85克樣品進行同樣實驗時,生成氨氣在標準狀況的體積為 。
(3)計算確定該混合物中(NH4)2SO4和NH4HSO4的物質的量之比 。
(4)欲計算該NaOH溶液的物質的量濃度應選擇第 組數據,由此求得NaOH溶液的物質的量濃度為 。
查看答案和解析>>
科目: 來源: 題型:
Ⅰ、已知一個碳原子上連有兩個羥基時,易發生下列轉化。請根據下圖回答問題:

Ⅱ、已知F具有如下特點:①能跟FeCl3溶液發生顯色反應;②1mol F最多可消耗2mol NaOH;③F只有一個環且苯環上的一氯代物只有兩種。

(1)已知B的相對分子質量為178,其燃燒產物中![]() ,則B的分子式是 ,所有F可能的結構簡式為: 。
,則B的分子式是 ,所有F可能的結構簡式為: 。
(2)寫出①的反應方程式: ;
寫出③的反應方程式: 。
(3)若F的同分異構體中,屬于酯類的芳香族化合物有 種。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com