
科目: 來源: 題型:
下列反應中,屬于氧化還原反應的是( )
A. CaO + H2O = Ca(OH)2
B. 2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
C. NH4HCO3![]() NH3↑+CO2↑+H2O
NH3↑+CO2↑+H2O
D、 2NaOH+H2SO4==Na2SO4 + 2H2O
查看答案和解析>>
科目: 來源: 題型:
臭氧(O3)能與KI溶液反應,生成O2等。在反應后的溶液中滴入酚酞變為紅色,若滴入淀粉則變為藍色。為測定某環境空氣中的臭氧含量,將0℃、1.01×105Pa的空氣33.6m3通過KI溶液,使之完全反應,所得溶液用0.0100mol·L-1的Na2S2O3溶液60.0mL恰好滴定達終點。反應方程式為:2Na2S2O3+I2=Na2S4O6+2NaI。
(1)臭氧通入KI溶液中的化學方程式: ;
(2)滴定過程中選擇的指示劑是 ,達到滴定終點時的現象為 ;
(3)計算該空氣中臭氧的體積分數。
查看答案和解析>>
科目: 來源: 題型:
已知:A、B、C、D四種短周期元素,A與D的原子序數之和等于B與C的原子序數之和,由D元素組成的單質在通常狀況下呈黃綠色,B、C、D三種元素位于同一周期,A、B、C三種元素的最高價氧化物對應的水化物分別為X、Y、Z,且存在如下轉化關系,試推斷回答下列問題。
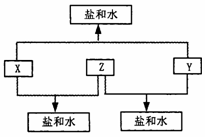
(1)D元素原子的結構示意圖為 ;
(2)A、B、C三種元素的原子半徑由小到大的順序為
(用元素符號表示);
(3)Y與C元素的最高價氧化物可以發生反應,該反應的離子方程式為 ;
(4)A與D兩元素的氣態氫化物之間可以反應生成一種鹽,該鹽的水溶液呈 (填“酸”、“堿”或“中”)性,該水溶液中各離子濃度由小到大的順序為 (用具體離子符號表示);
(5)實驗室中,應將X的濃溶液保存在棕色試劑瓶中,其原因是
(用化學方程式表示)。
查看答案和解析>>
科目: 來源: 題型:
已知反應:
![]()
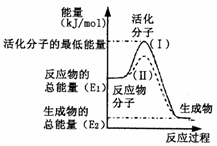
(1)寫出反應的平衡常數表達式K= ;
(2)右圖表示反應過程中有關物質的能量,則反應的![]() 0(填“>”、“<”或“=”);
0(填“>”、“<”或“=”);
(Ⅰ)、(Ⅱ)兩線中,使用催化劑的是 線;
(3)反應中發生反應的I-與被氧化的I-的物質的量比為 ;
(4)反應的速率可以用![]() 與加入的淀粉溶液反應顯藍色的時間t來度量,t越小,反應速率越大。某探究性學習小組在20℃進行實驗,記錄的數據如下:
與加入的淀粉溶液反應顯藍色的時間t來度量,t越小,反應速率越大。某探究性學習小組在20℃進行實驗,記錄的數據如下:
實驗編號 | ① | ② | ③ | ④ | ⑤ |
c(I-)/mol·L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
c( | 0.040 | 0.040 | 0.080 | 0.080 | 0.040 |
t/s | 88 | 44 | 22 | 11 | t1 |
則:該實驗的目的是 ,
顯色時間t1= s,
分析表中數據,得出的結論是 。
查看答案和解析>>
科目: 來源: 題型:
含有弱酸HA和其鈉鹽NaA的混合溶液,在化學上用作緩沖溶液。向其中加入少量酸或堿時,溶液的酸堿性變化不大。
(1)向該溶液中加入少量鹽酸時,發生反應的離子方程式是 ,向其中加入少量KOH溶液時,發生反應的離子方程式是 ;
(2)現將0.04mol·L-1HA溶液和0.02mol·L-1NaOH溶液等體積混合,得到緩沖溶液。
①若HA為HCN,該溶液顯堿性,則溶液中c(Na+) c(CN-)(填“<”、“=”或“>”),你得出該結論的依據是
;
②若HA為CH3COOH,該溶液顯酸性。溶液中所有的離子按濃度由大到小排列的順序是
。
查看答案和解析>>
科目: 來源: 題型:
已知Fe(OH)2是白色難溶于水的物質,很容易被空氣中的氧氣氧化為Fe(OH)3。如圖所示裝置可用來制取和觀察Fe(OH)2在空氣中被氧化時顏色的變化。實驗時必須使用鐵屑和6mol/L的硫酸,其它試劑自選。
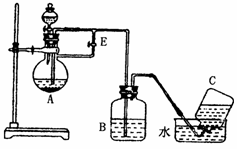
請填寫下列空白:
(1)B中盛有一定量的NaOH溶液,A中應預先加入的試劑是 ;
(2)實驗開始時應先將活塞E (填“打開”或“關閉”),C中收集到的氣體的主要成份是 ;
(3)簡述生成Fe(OH)2的操作過程
;
(4)(3)操作后拔出裝置B中的橡皮塞,使空氣進入,寫出有關反應的化學方程式
。
查看答案和解析>>
科目: 來源: 題型:
某化學小組的同學到實驗室學習。在實驗桌上擺有下列儀器:
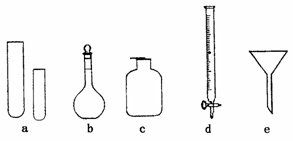 |
儀器編號 | a | b | c | d | e |
名稱 | 試管 | 溶量瓶 | 集氣瓶 | 堿式滴定管 | 普通漏斗 |
改正的名稱 |
(2)關于e的用途,乙同學說:組成防倒吸裝置。你還能說出其他兩種用途嗎?
① ;
② 。
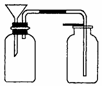 (3)丙同學想用右圖裝置以大理石和稀鹽酸反應制取CO2。教師指出,這需要太多的稀鹽酸,造成浪費。該同學選用了上面的一種儀器,加在裝置上,解決了這個問題。請你把該儀器畫在圖中合適的位置。
(3)丙同學想用右圖裝置以大理石和稀鹽酸反應制取CO2。教師指出,這需要太多的稀鹽酸,造成浪費。該同學選用了上面的一種儀器,加在裝置上,解決了這個問題。請你把該儀器畫在圖中合適的位置。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com