
科目: 來源: 題型:
【題目】已知某有機物A的紅外光譜和核磁共振氫譜如圖所示,下列說法中錯誤的是( )
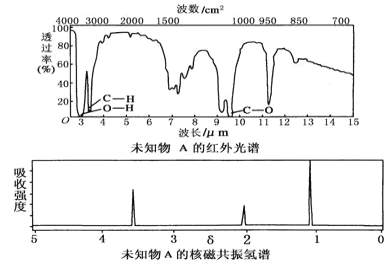
A.由紅外光譜可知,該有機物中至少有三種不同的化學鍵
B.由核磁共振氫譜可知,該有機物分子中有三種不同化學環境的氫原子
C.僅由其核磁共振氫譜無法得知其分子中的氫原子總數
D.若A的化學式為C2H6O,則其結構簡式為CH3—O—CH3
查看答案和解析>>
科目: 來源: 題型:
【題目】下列有關說法正確的是
A.MgO(s)+C(s)=CO(g)+Mg(g)高溫下能自發進行,則該反應ΔH>0、ΔS>0
B.常溫下等物質的量濃度的CH3COOH溶液和HCl溶液中,水的電離程度相同
C.0.1 mol·L-1 NH4Cl溶液加水稀釋,![]() 的值增大
的值增大
D.對于反應2SO2+O22SO3,使用催化劑能加快反應速率并提高SO2的平衡轉化率
查看答案和解析>>
科目: 來源: 題型:
【題目】下列實驗操作能達到實驗目的的是
A.用向上排空氣法收集NO
B.用裝置甲配制100 mL 0.100 mol·L-1的硫酸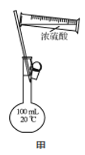
C.用裝置乙蒸發CuCl2溶液可得到CuCl2固體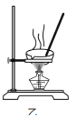
D.向含少量水的乙醇中加入生石灰后蒸餾可得到無水乙醇
查看答案和解析>>
科目: 來源: 題型:
【題目】Li2CO3是生產鋰電池的重要原料,電解鋁廢渣(主要含AlF3、LiF、NaF、CaO等物質)可用于制備Li2CO3。
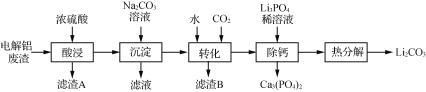
已知:①Li2CO3的溶解度:0 ℃ 1.54 g;20 ℃ 1.33 g;80 ℃ 0.85 g。
②20 ℃,Ksp[Ca3(PO4)2]=2×10-33,Ksp(CaHPO4)=1×10-7。
(1)在加熱條件下酸浸,反應生成能腐蝕玻璃的氣體,寫出AlF3發生反應的化學方程式:______。

(2)濾渣B的主要成分是________。
(3)“轉化”后所得LiHCO3溶液中含有的Ca2+需要加入Li3PO4除去。除鈣步驟中其他條件不變,反應相同時間,溫度對除鈣率和Li2CO3產率的影響如右圖所示。
①隨著溫度升高最終Li2CO3的產率逐漸減小的原因是___________。
②當溫度高于50 ℃時,除鈣率下降的原因可能是__________________。
(4)熱分解后,獲得Li2CO3需趁熱過濾的原因是_______________________。
(5)將酸浸時產生的氣體通入Al(OH)3和Na2SO4溶液的混合物中可產生難溶物冰晶石(Na3AlF6),該反應的離子方程式為_______________________________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】硫酸鐵銨(NH4Fe(SO4)2·xH2O)是一種重要鐵鹽,為充分利用資源,變廢為寶,在實驗室中探究采用廢鐵屑來制備硫酸鐵氨,具體流程如下:

(1)步驟②需要加熱的目的是_______________
(2)步驟②溫度保持80-95℃,采用的合適加熱方式是_____________________
(3)步驟③加入5%H2O2的目的是將Fe2+全部氧化為Fe3+,不引入雜質,請寫出反應的離子方程式__________________________
查看答案和解析>>
科目: 來源: 題型:
【題目】根據如下物質的轉化關系圖,回答有關問題:
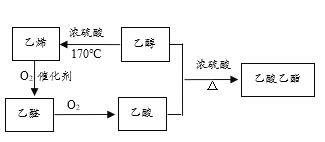
(1)上述物質中,_________(填結構簡式,下同)的產量是衡量一個國家石油化工發展水平的標志;常見的酸性調味品中含有3%~5%的_________;具有香味的油狀液體是_____________。
(2)乙醇中![]() 官能團名稱是______,比乙醇少一個碳原子的同系物的結構簡式是______。
官能團名稱是______,比乙醇少一個碳原子的同系物的結構簡式是______。
(3)生成乙酸乙酯的化學方程式是__________________________。
查看答案和解析>>
科目: 來源: 題型:
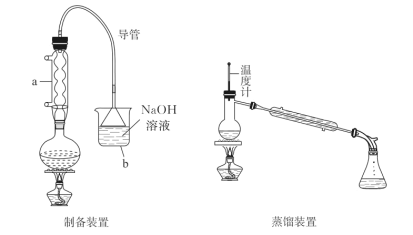
【題目】正溴丁烷是稀有元素萃取的溶劑及有機合成的中間體,其制備如圖(夾持裝置略):
已知:i.NaBr+H2SO4(濃)=HBr↑+NaHSO4
ii.CH3CH2CH2CH2OH十HBr→CH3CH2CH2CH2Br+H2O
iii.2HBr+H2SO4![]() Br2+SO2+2H2O
Br2+SO2+2H2O
iv.正溴丁烷密度:1.27g·mL-1;濃硫酸密度:1.84g·mL-1
請回答下列問題:
(1)正溴丁烷粗產品的制備:
①儀器a的名稱是__,向圓底燒瓶中添加藥品順序正確的是__(填正確選項字母)。
A.濃H2SO4→適量水→正丁醇→溴化鈉粉末
B.適量水→濃H2SO4→正丁醇→溴化鈉粉末
C.適量水→正丁醇→濃H2SO4→溴化鈉粉末
D.適量水→正丁醇→溴化鈉粉末→濃H2SO4
②裝置b中裝入NaOH溶液,目的是__。
③加熱回流,在此期間要不斷地搖動反應裝置,其原因為__;冷卻后改為蒸餾裝置,蒸出其正溴丁烷的粗品。
(2)正溴丁烷的提純:
①把正溴丁烷粗品倒入分液漏斗中,加入適量水洗滌,分出有機層;
②在另一干燥的分液漏斗中,加入濃硫酸洗去有機層中少量的未反應的正丁醇及副產物,從__(選填“上口”或“下口”)分出有機層;
③有機層依次用適量的水、濃硫酸、水、飽和NaHCO3溶液、水洗滌,用無水CaCl2干燥。以上三次用水洗滌簡化為一次用水洗滌是否合理,并說明理由__。
(3)①若洗滌后產物有紅色,說明含有溴單質,應加入適量的飽和NaHSO3溶液洗滌,將溴單質全部除去,其反應的離子方程式為__。
②若投入正丁醇11.84g,得到產物12.50g。則正丁醇的轉化率為__(保留兩位小數)。
查看答案和解析>>
科目: 來源: 題型:
【題目】以A、B、C為原料制取藥物AspirinSustained-ReleaseTablets(緩釋阿司匹林)的合成路線如圖:

已知:ⅰ.A、B為烴,其中A的產量可作為石油化工水平的標志;
ⅱ. 。
。
回答下列問題:
(1)Z所含官能團名稱為___。
(2)B和Y的結構簡式為__、__。
(3)完成方程式:
①X→CH2OHCH2OH__。
②C→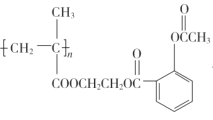 __。
__。
(4)滿足以下條件的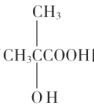 的同分異構體共有__種(不含立體異構),其中核磁共振氫譜峰面積比為6:1:1的同分異構體的結構簡式為__。
的同分異構體共有__種(不含立體異構),其中核磁共振氫譜峰面積比為6:1:1的同分異構體的結構簡式為__。
a.能發生水解反應 b.能與鈉反應放出氫氣 c.能發生銀鏡反應
(5)以乳酸(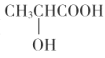 )和甲醇為原料,其他無機試劑任選,設計合成
)和甲醇為原料,其他無機試劑任選,設計合成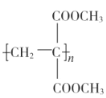 的路線:__。
的路線:__。
查看答案和解析>>
科目: 來源: 題型:
【題目】A、B、C均為短周期元素,它們在周期表中的位置如下圖所示。已知:B、C兩元素原子最外層電子數之和等于A元素原子最外層電子數的2倍;B.C兩元素的核電荷數之和是A元素原子序數的4倍。下列說法正確的是
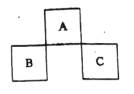
A.C位于元素周期表中第3周期第VA族
B.B的非金屬性比A強
C.C的氣態氫化物的穩定性比B的強
D.原子半徑:r(B)<r(C)
查看答案和解析>>
科目: 來源: 題型:
【題目】鈦酸鋇粉體是電子陶瓷元器件的重要基礎原料。工業上以TiCl4、BaCO3、H2C2O4等物質為原料制備草酸氧鈦鋇晶體[BaTiO(C2O4)2·4H2O],再高溫煅燒制得鈦酸鋇粉體。請回答下列問題:
(1)基態Ti原子的價電子排布圖為__,同周期元素中,基態原子未成對電子數與Ti相同的元素有___(填元素符號)。
(2)第IIA族(堿土金屬)元素的原子序數、原子半徑、第一電離勢(從元素的氣態基態原子中將一個電子移至無窮遠處時所需做的功)如下表所示。
元素 | 原子序數 | 原子半徑/pm | 每一電離勢/eV |
Be | 4 | 89 | 9.32 |
Mg | 12 | 136 | 7.644 |
Ca | 20 | 174 | 6.111 |
Sr | 38 | 191 | 5.692 |
Ba | 56 | 198 | 5.21 |
①由上表數據可知,相鄰元素原子半徑差值r(Be-Mg)、r(Mg-Ca)明顯大于r(Ca-Sr)、r(Sr-Ba),試解釋其原因__。
②由上表數據可知,隨原子序數的遞增,第IIA族元素的第一電離勢依次減小,試解釋其原因__。
(3)已知草酸分子的結構簡式為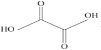 。
。
①草酸分子中,碳原子的雜化方式為__。
②由此結構簡式可預測草酸__(填“難溶”“微溶”或“易溶”)于水和乙醇。
③已知草酸和液溴的相關數據如下,草酸熔點高于液溴的原因是__。
名稱 | 化學式 | 相對子質量 | 熔點 |
草酸 | H2C2O4 | 90 | 101℃ |
液溴 | Br2 | 160 | -7.2℃ |
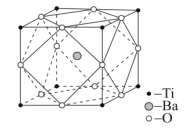
(4)設NA是阿伏加德羅常數的值,已知鈦酸鋇的立方晶胞結構如圖所示,晶胞中Ti原子的配位數為__,其晶胞參數約為apm,鈦酸鋇晶體的密度ρ=__g.cm-3。(列式即可)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com