
【題目】以A、B、C為原料制取藥物AspirinSustained-ReleaseTablets(緩釋阿司匹林)的合成路線如圖:

已知:ⅰ.A、B為烴,其中A的產量可作為石油化工水平的標志;
ⅱ. 。
。
回答下列問題:
(1)Z所含官能團名稱為___。
(2)B和Y的結構簡式為__、__。
(3)完成方程式:
①X→CH2OHCH2OH__。
②C→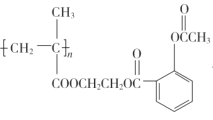 __。
__。
(4)滿足以下條件的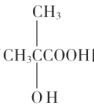 的同分異構體共有__種(不含立體異構),其中核磁共振氫譜峰面積比為6:1:1的同分異構體的結構簡式為__。
的同分異構體共有__種(不含立體異構),其中核磁共振氫譜峰面積比為6:1:1的同分異構體的結構簡式為__。
a.能發生水解反應 b.能與鈉反應放出氫氣 c.能發生銀鏡反應
(5)以乳酸(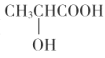 )和甲醇為原料,其他無機試劑任選,設計合成
)和甲醇為原料,其他無機試劑任選,設計合成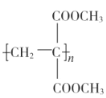 的路線:__。
的路線:__。
【答案】碳碳雙鍵、羧基 CH2=CH-CH3 ![]() BrCH2CH2Br+2NaOH
BrCH2CH2Br+2NaOH![]() CH2OHCH2OH+2NaBr(或其它合理答案)
CH2OHCH2OH+2NaBr(或其它合理答案) 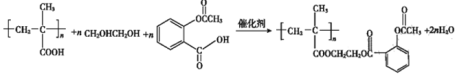 5 HCOOC(OH)(CH3)2
5 HCOOC(OH)(CH3)2 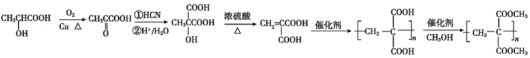
【解析】
A的產量可作為石油化工水平的標志,則A為CH2=CH2,由產物CH2OHCH2OH可逆推出X為A與鹵素單質加成的產物,可能為BrCH2CH2Br或ClCH2CH2Cl。由B的水化產物可逆推出B為CH2=CH-CH3,由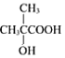 可逆推出Y為
可逆推出Y為![]() ,Z為
,Z為![]() 。
。
(1)Z的結構簡式為![]() ,所含官能團名稱為碳碳雙鍵、羧基。答案為:碳碳雙鍵、羧基;
,所含官能團名稱為碳碳雙鍵、羧基。答案為:碳碳雙鍵、羧基;
(2)由以上推斷,可確定B和Y的結構簡式為CH2=CH-CH3、![]() 。答案為:CH2=CH-CH3;
。答案為:CH2=CH-CH3;![]() ;
;
(3)①X為BrCH2CH2Br或ClCH2CH2Cl,在堿性條件下水解生成CH2OHCH2OH的方程式為BrCH2CH2Br+2NaOH![]() CH2OHCH2OH+2NaBr。答案為:BrCH2CH2Br+2NaOH
CH2OHCH2OH+2NaBr。答案為:BrCH2CH2Br+2NaOH![]() CH2OHCH2OH+2NaBr(或其它合理答案);
CH2OHCH2OH+2NaBr(或其它合理答案);
②C→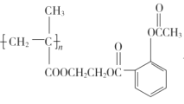 的反應方程式為
的反應方程式為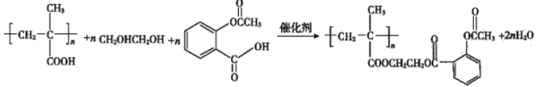 。答案為:
。答案為: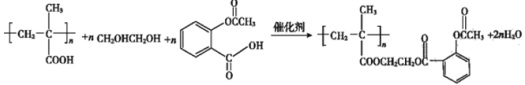 ;
;
(4)滿足條件:a.能發生水解反應、b.能與鈉反應放出氫氣、c.能發生銀鏡反應的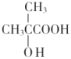 的同分異構體中,應含有HCOO-、-OH,所以其可能結構簡式為HCOOCH2CH2CH2OH、HCOOCH2CH(CH3)OH、HCOOCH(OH)CH2CH3、HCOOC(OH)(CH3)2、HCOOCH(CH3)CH2OH共5種;其中核磁共振氫譜峰面積比為6:1:1的同分異構體的結構簡式為HCOOC(OH)(CH3)2。答案為:5;HCOOC(OH)(CH3)2;
的同分異構體中,應含有HCOO-、-OH,所以其可能結構簡式為HCOOCH2CH2CH2OH、HCOOCH2CH(CH3)OH、HCOOCH(OH)CH2CH3、HCOOC(OH)(CH3)2、HCOOCH(CH3)CH2OH共5種;其中核磁共振氫譜峰面積比為6:1:1的同分異構體的結構簡式為HCOOC(OH)(CH3)2。答案為:5;HCOOC(OH)(CH3)2;
(5)以乳酸(![]() )和甲醇為原料,先將乳酸轉化為丙酮
)和甲醇為原料,先將乳酸轉化為丙酮![]() ,再與HCN加成,在酸性條件下水解,生成
,再與HCN加成,在酸性條件下水解,生成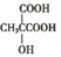 ,然后發生消去反應,生成
,然后發生消去反應,生成![]() ,再加聚、酯化可得
,再加聚、酯化可得 ,合成路線為:
,合成路線為: 。答案為:
。答案為: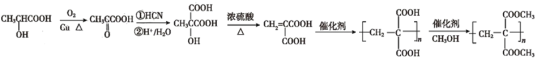 。
。


科目:高中化學 來源: 題型:
【題目】已知常溫下H2A的K1=1.0×10-4,K2=5.0×10-7。向20mLlmol·L-1的H2A溶液中逐滴滴入2mol·L-1的NaOH溶液,溶液中水電離出的c水(OH-)隨加入NaOH溶液的體積V的變化如圖所示,下列分析正確的是( )
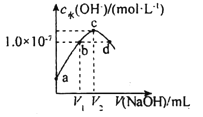
A.V1<10,V2=20
B.a點溶液的pH=3
C.c點溶液c水(H+)≈1.0×10-4mol·L-1
D.b、d點溶液均呈中性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鎂電池因具有高的安全性和低廉的價格而備受關注,我國科學 家最近研發出一種新型鎂電池,其工作原理如圖所示。下列說法正確的是

A.I 室中的電解質溶液可以是稀 H2SO4
B.外電路中轉移 2mol 電子時,N 極質量增加 24a g
C.離子交換膜為陽離子交換膜
D.電子流向:M 電極→I 室→離子交換膜→II 室→N 極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對甲基苯乙酮是重要的化工原料,某實驗小組利用如圖裝置制備對甲基苯乙酮。

制備原理: (放熱反應)。 反應物和產物的相關數據列表:
(放熱反應)。 反應物和產物的相關數據列表:
試劑名稱 | 分子式 | 分子量 | 熔點/℃ | 沸點/℃ | 密度/g·mL-1 |
甲苯 | C7H8 | 92 | -93 | 110.6 | 0.8669 |
乙酸酐 | (CH3CO)2 | 102 | -73.1 | 138.6 | 1.08 |
對甲基苯乙酮 | C9H10O | 134 | 28 | 94(0.93kPa) | 1.0051 |
實驗步驟:
步驟 1:如圖所示,在 100mL 三頸燒瓶上安裝攪拌器、儀器 x 和上口裝有無水氯化鈣的冷凝管,干燥管與一氣體 吸收裝置相連。
步驟 2:三頸燒瓶中快速加入研碎的催化劑和 20mL 無水甲苯,在攪拌的條件下通過儀器 x 緩慢地滴加 3.4mL 醋酸酐與 5mL 甲苯的混合液,約需 15min 滴完。
步驟 3:反應結束后,將三頸燒瓶在 95℃時加熱 25~30min。
步驟 4:反應混合液冷卻后轉移到盛有 30mL 濃鹽酸與 30mL 冰水的燒杯中(目的是將對甲基苯乙酮從其與鋁的化 合物中分離出來),用分液漏斗分出有機層、水層。每次用 5mL 甲苯萃取兩次,并將所有甲苯層合并,然后依次 用水、10%氫氧化鈉溶液、水各 10mL 洗滌有機層,最后用無水硫酸鎂處理。
步驟 5:將干燥后的溶液濾入蒸餾瓶,減壓蒸餾(整套裝置必須是干燥的),收集 94℃(0.93kPa)餾分,得到對甲 基苯乙酮 4.1g。
請回答下列問題:
(1)儀器 x 的名稱為________。與普通的分液漏斗相比,本實驗采用儀器 x 的優點為_______。
(2)本實驗中的氯化鋁若水解則會影響催化效率,除了使用干燥管的措施外,還應該采取哪些措施防止水解_____(答兩點)。
(3)步驟③中最適宜的加熱方式為 _____。
(4)步驟④中加入 10%的氫氧化鈉溶液的目的為 _____,加入無水硫酸鎂的目的為_________。
(5)步驟④中水層每次用 5mL 甲苯萃取兩次并將所有甲苯層合并的目的為________。
(6)步驟⑤中減壓蒸餾時所需的冷凝裝置能否選用題給裝置圖中的球形冷能管_____(答“能”或“不能”)。 本實驗中,對甲基苯乙酮的產率為_____(結果保留 2 位有效數字)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】黃色固體聚合硫酸鐵(SPFS)是一種重要的無機高分子絮凝劑,極易溶于水,作為工業和生活污水處理等領域具有重要的應用。SPFS可表示成Fex(OH)y(SO4)z·nH2O。工業上常用的一種制備流程為:(綠礬化學式為FeSO4·7H2O)
![]()
在SPFS的多個質量指標中,鹽基度是重要的質量指標之一,鹽基度定義為:鹽基度=n(OH-)/3n( Fe) ×100%。式中n(OH-)、n(Fe)分別表示固體聚合硫酸鐵中OH一和Fe的物質的量。試回答下列問題。
(1)在綠礬中加人酸性介質的NaClO3目的是__________ 。
(2)SPFS溶于水后并與水反應生成__________ 能吸附水中的懸浮物來凈化水。
(3)取15.05g某固體聚合硫酸鐵溶解于水,向其中加人過量的BaCI2溶液到沉淀完全,經過濾、洗滌、干燥得白色沉淀20.97g.向上述濾液中加人NH3H2O,調節溶液pH= 6,經過濾、洗滌、干燥得Fe2O3固體5.60g。該固體聚合硫酸鐵的鹽基度為_________ 。
(4)計算出該固體聚合硫酸鐵樣品的化學式______________(寫出計算過程)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗操作能達到實驗目的的是
A.用向上排空氣法收集NO
B.用裝置甲配制100 mL 0.100 mol·L-1的硫酸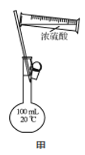
C.用裝置乙蒸發CuCl2溶液可得到CuCl2固體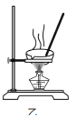
D.向含少量水的乙醇中加入生石灰后蒸餾可得到無水乙醇
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25 ℃時,將SO2通入NaOH溶液得到一組c(H2SO3)+c(HSO3-)+c(SO32-)=0.100 mol·L-1的混合溶液,溶液中部分微粒的物質的量濃度隨pH的關系曲線如右下圖所示。下列敘述正確的是
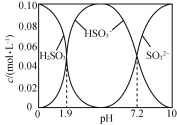
A.H2SO3的Ka2=10-7.2
B.pH=1.9的溶液中:c(Na+)>c(H2SO3)=c(HSO3-)> c(SO32-)
C.c(Na+)=0.100 mol·L-1的溶液中:c(H+)+c(SO32-)=c(OH-)+c(H2SO3)
D.c(HSO3-)=0.050 mol·L-1的溶液中:c(H+)+c(Na+)<0.150 mol·L-1+c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鉛的單質、氧化物、鹽在現代T業中有著重要用途。
I.(1)鉛能形成多種氧化物,如堿性氧化物PbO、酸性氧化物PbO2、還有組成類似Fe3O4的PbO2。請將Pb3O4改寫成簡單氧化物的形式: ___。
Ⅱ.以廢舊鉛酸電池中的含鉛廢料鉛膏(Pb、PbO、PbO2、PbSO4等)為原料,制備超細PbO,實現鉛的再生利用。其工作流程如下:
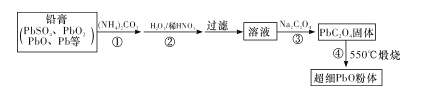
(2)步驟①的目的是“脫硫”,即將PbSO4轉化為PbCO3,反應的離子方程式為____。 “脫硫過程”可在如圖所示的裝置中進行。實驗條件為:轉化溫度為35℃,液固比為5:1,轉化時間為2h。
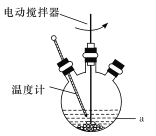
①儀器a的名稱是____;轉化溫度為35℃,采用的合適加熱方式是____。
②步驟②中H2O2的作用是____(用化學方程式表示)。
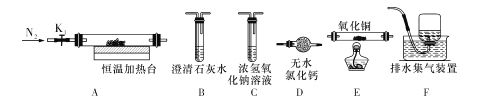
(3)草酸鉛受熱分解生成PbO時,還有CO和CO2生成,為檢驗這兩種氣體,用下圖所示的裝置(可重復選用)進行實驗。實驗裝置中,依次連接的合理順序為A ___(填裝置字母代號),證明產物中有CO氣體的實驗現象是____。
(4)測定草酸鉛樣品純度:稱取2.5 g樣品,酸溶后配制成250 mL溶液,然后量取25. 00 mL該溶液,用0. 050 00 mol/L的EDTA( Na2H2Y)標準溶液滴定其中的Pb2+(反應方程式為____,雜質不反應),平行滴定三次,平均消耗EDTA標準溶液14. 52 mL。
①若滴定管未用EDTA標準液潤洗,測定結果將 ___(填“偏高”“偏低”或“不變”)。
②草酸鉛的純度為 ___(保留四位有效數字)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用釕(Ru)基催化劑催化CO2(g)和H2(g)的反應時,每生成92g液態HCOOH放出62.4kJ的熱量,下列說法正確的是( )
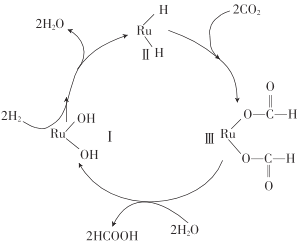
A.圖示中物質II為該反應的催化劑
B.圖示中參與循環的物質只有CO2和H2
C.反應的活化能為62.4kJ·mol-1
D.該反應的熱化學方程式為H2(g)+CO2(g)=HCOOH(l) △H=-31.2kJ·mol-1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com