
科目: 來源: 題型:
【題目】從鋁土礦(主要成分是Al2O3,含SiO2、Fe2O3、MgO等雜質)中提取氧化鋁的兩種流程如下:

請回答下列問題:
(1)給濾液E中通入過量的NH3,其反應的離子方程式是____________________。
(2)流程Ⅱ中加入燒堿溶液后,生成SiO![]() 的離子方程式是__________________。
的離子方程式是__________________。
(3)驗證濾液A中含Fe3+,可取少量濾液并加入______________(填寫試劑名稱)。
(4)濾液C中溶質的主要成分是___________(填化學式)。
(5)濾液F中離子電荷守恒的關系式為___________________________。
(6)濾液C和濾液F共同的溶質為G,用惰性電極電解500mL 0.1 mol·L-1的G溶液,若陽極得56 mL氣體(標準狀況),則所得溶液在常溫下pH為_____________(忽略電解前后溶液體積的變化)。
(7)已知25 ℃時Mg(OH)2的溶度積常數Ksp=1.8×10-11。取適量的濾液A,加入一定量的燒堿溶液至達到沉淀溶解平衡,測得該溶液的pH=13.00,則25℃時殘留在溶液中的c(Mg2+)=________ mol·L-1。
查看答案和解析>>
科目: 來源: 題型:
【題目】下列做法符合原子經濟性原理的是
A.SO3與H2O反應制取硫酸:SO3+H2O=H2SO4
B.用氫氧化鈉溶液吸收SO2:SO2+2NaOH=Na2SO3+H2O
C.CO2與H2反應制取甲醇:CO2+3H2 CH3OH+H2O
CH3OH+H2O
D.H2還原氧化銅:H2+CuO![]() Cu+H2O
Cu+H2O
查看答案和解析>>
科目: 來源: 題型:
【題目】硫酸是重要的化工原料,工業制取硫酸最重要的一步反應為:2SO2(g)+O2(g) ![]() 2SO3(g) H<0。
2SO3(g) H<0。
(1)為提高SO2的轉化率,可通入過量O2,用平衡移動原理解釋其原因:_______。
(2)某興趣小組在實驗室對該反應進行研究,在一密閉容器內加入一定量的SO2和O2,部分實驗圖像如圖1

① 該反應的平衡常數表達式為___________________。
② t1、t2、t3中,達到化學平衡狀態的是________________。
③ t2到t3的變化是因為改變了一個反應條件,該條件可能是___________________。
(3)將SO2和O2充入恒壓密閉容器中,原料氣中SO2 和O2的物質的量之比m[m=n(SO2)/n(O2)] 不同時,SO2的平衡轉化率與溫度(T)的關系如圖所示,則m1、m2、m3的從大到小的順序為___________________。
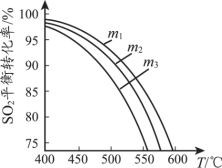
(4)已知25℃,NH3·H2O的Kb=1.8×105,H2SO3的Ka1=1.3×102,Ka2=6.2×108。若氨水的濃度為2.0 mol·L1,溶液中的c(OH-)=_______mol·L1。將原料氣SO2和O2通入該氨水中,當c(OH-)降至1.0×107 mol·L1時,溶液中的c(![]() )/c(
)/c(![]() )=____。
)=____。
查看答案和解析>>
科目: 來源: 題型:
【題目】常溫下,有關物質的溶度積如下
物質 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
下列有關說法不正確的是( )
A.常溫下,除去NaCl溶液中的MgCl2雜質,選用NaOH溶液比Na2CO3溶液效果好
B.常溫下,除去NaCl溶液中的CaCl2雜質,選用NaOH溶液比Na2CO3溶液效果好
C.向含有Mg 2+、Fe3+的溶液中滴加NaOH溶液,當兩種沉淀共存且溶液的pH=8時,c(Mg 2+)∶c(Fe3+)=2 .125×1021
D.將適量的Ca(OH)2固體溶于100mL水中,剛好達到飽和[c(Ca2+)=1.054×10-2mol/L],若保持溫度不變, 向其中加入100mL 0.012mol/L的NaOH,則該溶液變為不飽和溶液。
查看答案和解析>>
科目: 來源: 題型:
【題目】有下列六種物質的溶液:①NaCl ②NH4Cl ③Na2CO3 ④Al2(SO4)3 ⑤CH3COOH ⑥NaHCO3。
(1)25℃時,0.1mol·L-1②溶液的pH________7(填“>”、“=”或“<”);其原因是______________________________________(用離子方程式表示);
(2)常溫下,濃度均為0.1mol/L的③和⑥的溶液中離子種類________(填“相同”或是“不相同”);
(3)將④溶液加熱蒸干并灼燒最終得到的物質是____________(填化學式);
(4)常溫下0.1 mol/L的⑤溶液加水稀釋過程中,下列表達式的數據一定變大的是_________。
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)·c(OH-)
查看答案和解析>>
科目: 來源: 題型:
【題目】實驗小組探究酸雨對低碳鋼腐蝕的影響,實驗流程如圖:

實驗使用了3種模擬酸雨。模擬酸雨中的離子濃度如表所示,其中平衡電荷的陽離子以NH![]() 或Na+補充,實驗均在室溫下進行,低碳鋼片樣品的大小和質量均相同。
或Na+補充,實驗均在室溫下進行,低碳鋼片樣品的大小和質量均相同。

(1)將模擬酸雨1和模擬酸雨2進行對比實驗,實驗的目的是___。模擬酸雨3對鋼片的腐蝕速率大于模擬酸雨2對鋼片的腐蝕速率,可以得到結論是___。
(2)在用模擬酸雨2進行實驗時,腐蝕沖洗液中檢測到Fe2+和NH![]() 的含量升高。腐蝕時硝酸和鐵反應的離子方程式為___。
的含量升高。腐蝕時硝酸和鐵反應的離子方程式為___。
(3)在上述三組腐蝕實驗中,都檢測到鋼片內部持續產生腐蝕電流。產生腐蝕電流的原因是___。
(4)鋼鐵的腐蝕研究中,通常用“腐蝕速率(單位為mg·h-1)"對鋼鐵腐蝕過程和結果進行評估。則計算“腐蝕速率”需要測量的實驗數據為___。
查看答案和解析>>
科目: 來源: 題型:
【題目】PET(聚對二苯甲酸乙二醇酯)是制備醫用防護服的重要材料。以石油作為原料合成PET中間體的流程如圖:
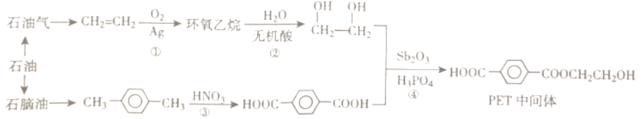
(1)環氧乙烷的分子式為C2H4O,分子中存在一個環狀結構。環氧乙烷的結構簡式為___,環氧乙烷有多種同分異構體,下列結構與環氧乙烷互為同分異構體的是___ (填代號)
a.CH3CHO b.HOCH2CH2OOH c.CH2=CHOH
(2)反應②的產物是乙二醇。乙二醇屬于醇類化合物,性質與乙醇類似。乙二醇的官能團是___。(填名稱或者結構簡式)
(3)從石腦油中可以提煉出對二甲苯(![]() )。對二甲苯的分子式為___。對二甲苯在濃硫酸和濃硝酸存在的條件下,可以在苯環上形成硝基取代產物(分子式為C8H8N2O4),該硝基取代產物的所有可能的結構簡式為___。
)。對二甲苯的分子式為___。對二甲苯在濃硫酸和濃硝酸存在的條件下,可以在苯環上形成硝基取代產物(分子式為C8H8N2O4),該硝基取代產物的所有可能的結構簡式為___。
(4)反應④的化學方程式為___。該反應的反應類型為___。
查看答案和解析>>
科目: 來源: 題型:
【題目】納米TiO2在涂料、光催化、化妝品等領域有著極其廣泛的應用.制備納米TiO2的方法之一是TiCl4水解生成TiO2xH2O,經過濾、水洗除去其中的Cl-,再烘干、焙燒除去水分得到粉體TiO2.用氧化還原滴定法測定TiO2的質量分數:一定條件下,將TiO2溶解并還原為Ti3+,再以KSCN溶液作指示劑,用NH4Fe(SO4)2標準溶液滴定Ti3+至全部生成Ti4+.請回答下列問題:
(1)TiCl4水解生成TiO2x H2O的化學方程式為____________________________________.
(2)配制NH4Fe(SO4)2標準溶液時,加入一定量H2SO4的原因是__________________;使用的儀器除天平、藥匙、玻璃棒、燒杯、量筒外,還需要如圖中的______(填字母代號)

(3)滴定分析時,稱取TiO2(摩爾質量為M gmol-1)試樣w g,消耗c molL-1 NH4Fe(SO4)2標準溶液V mL,則TiO2質量分數表達式為______.
(4)判斷下列操作對TiO2質量分數測定結果的影響(填 “偏高”、“偏低”或“無影響”)
①若在配制標準溶液過程中,燒杯中的NH4Fe(SO4)2溶液有少量濺出,使測定結果______.
②若在滴定終點讀取滴定管刻度時,俯視標準液液面,使測定結果______.
查看答案和解析>>
科目: 來源: 題型:
【題目】染料化工企業產生的廢水中含有高濃度的氨氮(氨和銨鹽)成分,直接排放會造成環境污染。實驗小組探索下列方法對氨氮廢水進行處理。

(1)實驗室檢測上述廢水中是否含有氨氮的方法是___。
(2)“吹脫”步驟中,在廢水池的底部吹入大量熱氣泡,其目的是___。
(3)“氧化”步驟中加入了微生物,NH3被氧化為N2。反應的化學方程式為___。
(4)“沉淀"步驟中將剩余的NH3·H2O轉化為NH4MgPO46H2O沉淀,發生反應的離子方程式為___。NH4MgPO46H2O在農業生產中具有重要應用價值,其原因是___。
查看答案和解析>>
科目: 來源: 題型:
【題目】Ⅰ.(1)室溫下,使用pH計測定0.1mol/L NH4Cl溶液的pH=5.12.由此可以得到的結論是_____________(填字母).
a、溶液中c(H+)>c(OH) b、NH4+水解是微弱的
c、NH3H2O是弱堿 d、由H2O電離出的c(H+)<107mol/L
e、物質的量濃度相等的氨水和鹽酸等體積混合,溶液pH=7
(2)室溫下,用0.1mol/LNaOH溶液分別滴定20.00mL0.1mol/L的鹽酸和醋酸,滴定曲線如圖所示,下列說法正確的是

①表示滴定鹽酸的曲線是____________(填序號).
②滴定醋酸溶液的過程中:
i、V(NaOH)=10.00mL時,溶液中離子濃度由大到小的順序為________________________.
ii、當c(Na+)=c(CH3COO)+c(CH3COOH)時,溶液pH________7(填“>”、“=”或“<”).
Ⅱ.復分解反應是中學化學中常見的一種反應類型。
(1)已知在常溫下測得濃度均為0.1molL1的下列6種溶液的pH值:
溶質 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
復分解存在這樣一個規律:一種較強酸與另一種較弱酸的鹽可以自發地反應,生成較弱酸和較強酸的鹽,如:2CH3COOH+Na2CO3=2CH3COONa+CO2↑+H2O 若換個角度看,它同時揭示出另一條規律,即堿性較強的物質發生類似反應可以生成堿性較弱的物質。依照該規律,請判斷下列反應不能成立的是______(填編號).
A.CO2+H2O+2NaClO═Na2CO3+2HClO
B.CO2+H2O+NaClO═NaHCO3+HClO
C.CO2+H2O+C6H5ONa→NaHCO3+C6H5OH
D.CO2+H2O+2C6H5ONa→Na2CO3+2C6H5OH
E.Na2CO3+C6H5OH→NaHCO3+C6H5ONa
F.CH3COOH+NaCN═CH3COONa+HCN
(2)根據前述信息判斷,常溫下,濃度均為0.05molL1的下列5種物質的溶液中,pH最小的是______(填編號),其pH值為______(填數值);pH最大的是______(填編號).
①HCN ②CH3COOH ③HClO4 ④HClO ⑤H2SO4
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com