
【題目】染料化工企業產生的廢水中含有高濃度的氨氮(氨和銨鹽)成分,直接排放會造成環境污染。實驗小組探索下列方法對氨氮廢水進行處理。

(1)實驗室檢測上述廢水中是否含有氨氮的方法是___。
(2)“吹脫”步驟中,在廢水池的底部吹入大量熱氣泡,其目的是___。
(3)“氧化”步驟中加入了微生物,NH3被氧化為N2。反應的化學方程式為___。
(4)“沉淀"步驟中將剩余的NH3·H2O轉化為NH4MgPO46H2O沉淀,發生反應的離子方程式為___。NH4MgPO46H2O在農業生產中具有重要應用價值,其原因是___。
【答案】取廢水樣品3-5mL于試管中,滴加濃燒堿溶液,加熱,用濕潤的紅色石蕊試靠近試管口,若試紙變藍色,則說明廢水中含有氨氮 加熱并攪拌廢水,促進氨水分解和揮發 4NH3+3O2![]() 2N2+6H2O 5H2O+NH3·H2O+Mg2++HPO
2N2+6H2O 5H2O+NH3·H2O+Mg2++HPO![]() =NH4MgPO46H2O↓ 磷酸鎂銨含有植物生長所需要的氮、磷、鎂元素
=NH4MgPO46H2O↓ 磷酸鎂銨含有植物生長所需要的氮、磷、鎂元素
【解析】
從信息和流程知,處理氨氮廢水時,在廢水池的底部吹入大量熱空氣,把廢液中的氨水分解揮發后轉變成氨氣,再通過微生物,把NH3氧化為N2,剩余的氨氮通過和MgCl2及Na2HPO4反應產生NH4MgPO46H2O沉淀而除去,據此分析回答;
(1)可通過檢驗銨根的方法檢測上述廢水中是否含有氨氮,即:取廢水樣品3-5mL于試管中,滴加濃燒堿溶液,加熱,用濕潤的紅色石蕊試靠近試管口,若試紙變藍色,則說明廢水中含有氨氮;答案為:取廢水樣品3-5mL于試管中,滴加濃燒堿溶液,加熱,用濕潤的紅色石蕊試靠近試管口,若試紙變藍色,則說明廢水中含有氨氮;
(2)一水合氨受熱易分解,在廢水池的底部吹入大量熱氣泡,故熱氣可促使氨水分解,而底部通入的氣體在逸出的過程中還起到攪拌作用,有助于氨氣揮發;答案為:加熱并攪拌廢水,促進氨水分解和揮發;
(3)NH3被氧化為N2的過程中,微生物起催化劑作用,反應的化學方程式為4NH3+3O2![]() 2N2+6H2O;答案為:4NH3+3O2
2N2+6H2O;答案為:4NH3+3O2![]() 2N2+6H2O;
2N2+6H2O;
(4)“沉淀"步驟中將剩余的NH3·H2O轉化為NH4MgPO46H2O沉淀,發生反應的離子方程式為5H2O+NH3·H2O+Mg2++HPO![]() =NH4MgPO46H2O↓;NH4MgPO46H2O是一種復合肥,而且所含有的Mg也是植物生長所需要,因此在農業生產中具有重要應用價值;答案為:5H2O+NH3·H2O+Mg2++HPO
=NH4MgPO46H2O↓;NH4MgPO46H2O是一種復合肥,而且所含有的Mg也是植物生長所需要,因此在農業生產中具有重要應用價值;答案為:5H2O+NH3·H2O+Mg2++HPO![]() =NH4MgPO46H2O↓;磷酸鎂銨含有植物生長所需要的氮、磷、鎂元素。
=NH4MgPO46H2O↓;磷酸鎂銨含有植物生長所需要的氮、磷、鎂元素。


科目:高中化學 來源: 題型:
【題目】結合下表回答下列問題(均為常溫下的數據):
酸 | 電離常數(Ka) | 酸 | 電離常數(Ka) | 酸 | 電離常數(Ka) | 酸 | 電離常數(Ka) |
CH3COOH | 1.8×10-5 | H2CO3 | K1=4.4×10-7 K2=4.7×10-11 | H2C2O 4 | K1=5.4×10-2 K2=5.4×10-5 | H2S | K1=1.3×10-7 K2=7.1×10-15 |
HClO | 3×10-8 |
請回答下列問題:
(1)同濃度的CH3COO-、HCO3-、CO32-、HC2O4-、ClO-、S2-中結合H+的能力最弱的是__________。
(2)常溫下0.1 molL-1的CH3COOH溶液在加水稀釋過程中,下列表達式的數據一定變小的是_______(填序號)。
A.c(H+) B. c(H+)/c(CH3COOH) C. c(H+)/c(OH-) D. c(OH-)
(3)0.1 molL-1的H2C2O4溶液與0.1 molL-1的KOH的溶液等體積混合后所得溶液呈酸性,該溶液中各離子濃度由大到小的順序為______________。
(4)pH相同的NaClO和CH3COOK溶液,其溶液的物質的最濃度的大小關系是:CH3COONa______NaClO,兩溶液中:[c(Na+)-c(ClO-)]______[c(K+)-c(CH3COO-)](填“>”“<”或“=”)。
(5)向0.1 molL-1CH3COOH 溶液中滴加 NaOH 溶液至 c(CH3COOH): c(CH3COO-)=5 : 9,此時溶液pH=_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物C常用于食品行業。已知9.0gC在足量O2中充分燃燒,將生成的混合氣體依次通過足量的濃硫酸和堿石灰,分別增重5.4g和13.2g,其質譜圖如圖所示,則:
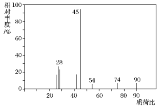
(1)C的分子式是___。
(2)若C能與NaHCO3溶液發生反應,則C中一定含有的官能團名稱是_____。又知C分子的核磁共振氫譜有4個峰,峰面積之比是1∶1∶1∶3,則C的結構簡式是_____。寫出C與NaHCO3溶液反應的化學方程式__。
(3)0.1molC與足量Na反應,在標準狀況下產生H2的體積是_____L。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、W均為短周期主族元素,X、Y、Z原子的最外層電子數之和為10。X與Z同族,Y最外層電子數等于X次外層電子數,且Y原子半徑大于Z。W的最外層電子數等于X的核外電子總數,且W單質常溫下為固體。請回答下列問題:
(1)Z在周期表中的位置為______________。
(2)Y元素形成的離子的結構示意圖為____________。
(3)X、Y、Z三種元素對應的原子半徑大小關系為____________(填元素符號)。
(4)X和Z形成的簡單氫化物,熱穩定性較好的是______________(填化學式)。
(5)Y與X的最高價氧化物在一定條件下反應的實驗現象是___________________________。
(6)下列說法正確的是_______。
A.W的氧化物,均滿足8e—穩定結構
B.最高價氧化物對應的水化物的酸性W>Z
C.由于Z的氧化物ZO2既可與酸反應,又能與堿反應,所以ZO2為兩性氧化物
D.W的氧化物WO2,具有還原性,能使酸性KMnO4溶液褪色
(7)足量的單質Y與一定量的W的最高價氧化物對應的水化物的濃溶液,在一定條件下充分反應,所得氣體的成分為_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2019年諾貝爾化學獎頒給了三位為鋰離子電池發展作出重要貢獻的科學家。磷酸鐵鋰電池充電時陽極反應式為:LiFePO4 -xLi+ -xe-→ xFePO4 + (1-x)LiFePO4。放電工作示意圖如下圖。下列敘述不正確的是

A.放電時,Li+ 通過隔膜移向正極
B.放電時,電子由鋁箔沿導線流向銅箔
C.放電時正極反應為:FePO4 + xLi+ + xe-→ xLiFePO4 + (1-x)FePO4
D.該電池充放電過程通過Li+ 遷移實現,C、Fe、P元素化合價均不發生變化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,有關物質的溶度積如下
物質 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
下列有關說法不正確的是( )
A.常溫下,除去NaCl溶液中的MgCl2雜質,選用NaOH溶液比Na2CO3溶液效果好
B.常溫下,除去NaCl溶液中的CaCl2雜質,選用NaOH溶液比Na2CO3溶液效果好
C.向含有Mg 2+、Fe3+的溶液中滴加NaOH溶液,當兩種沉淀共存且溶液的pH=8時,c(Mg 2+)∶c(Fe3+)=2 .125×1021
D.將適量的Ca(OH)2固體溶于100mL水中,剛好達到飽和[c(Ca2+)=1.054×10-2mol/L],若保持溫度不變, 向其中加入100mL 0.012mol/L的NaOH,則該溶液變為不飽和溶液。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用如圖所示裝置進行以下實驗,能得到相應實驗結論的是
① | ② | ③ | 實驗結論 |
| |
A | 濃氨水 | NaOH | 酚酞 | NaOH的堿性比 NH3H2O的強 | |
B | 濃鹽酸 | MnO2 | 淀粉溶液 | 非金屬性:氯元素大于碘元素 | |
C | 濃硝酸 | Na2CO3 | Na2SiO3 | 酸性:HNO3 > H2CO3 > H2SiO3 | |
D | 濃硫酸 | 蔗糖 | 溴水 | 濃硫酸具有脫水性、氧化性 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關CuCl2溶液的敘述中正確的是
A.溶液中存在自由移動的離子:CuCl2![]() Cu2+ + 2Cl-
Cu2+ + 2Cl-
B.溶液中:c(Cu2+)+c(H+)=c(Cl-)+c(OH-)
C.用惰性電極電解該溶液時,陽極有黃綠色氣體產生
D.配制CuCl2溶液時,需加入少量稀硫酸抑制其水解
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氧化鎂在易燃材料中常被用作阻燃劑,碳酸鎂高溫分解法是工業上制備輕質氧化鎂的常用方法。鎂硅礦主要成分為Mg3(Si2O5)(OH)4和還有少量的Fe2O3、Al2O3等。以鎂硅礦為原料制備碳酸鎂晶體(MgCO3nH2O)的生產流程如下:
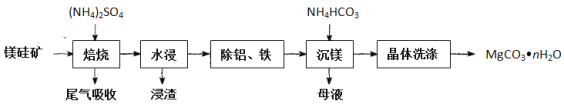
已知“焙燒”過程中的主要反應為:Mg3(Si2O5)(OH)4+5(NH4)2SO4![]() 3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑
3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑
(1)Mg3(Si2O5)(OH)4用氧化物的形式表示為___,焙燒產物NH3的電子式為__。
(2)為提高水浸速率,可采取的措施為__(任寫一種)。“浸渣”的主要成分為__。
(3)“除鋁、鐵”時,需將溶液pH調至8.0左右,適宜作調節劑的是__(填字母代號)。
a.Ca(OH)2 b.Mg(OH)2 c.NH3H2O
(4)“沉鎂”過程中反應的離子方程式為__。“沉鎂”時若溫度超過60℃,將會產生較多的堿式碳酸鎂雜質,原因是___。
(5)流程中可以循環利用的物質是___(填化學式)。
(6)為測定產品MgCO3nH2O中的n值,稱取15.6g產品進行充分加熱至恒重,冷卻,稱得固體質量為4g,則n=__。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com