
科目: 來源: 題型:
【題目】下列離子方程式書寫正確的是( )
A.食醋除水垢:![]()
B.稀硝酸中加入少量亞硫酸鈉:![]()
C.處理工業廢水時Cr(Ⅵ)的轉化:![]()
D.用酸性KMnO4測定草酸溶液濃度:![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】某興趣小組在實驗室用乙醇、濃硫酸和溴化鈉反應來制備溴乙烷,并探究溴乙烷的性質。反應原理和實驗裝置如下(加熱裝置未畫出):
H2SO4(濃)+NaBr![]() NaHSO4+HBr↑ CH3CH2OH+HBr
NaHSO4+HBr↑ CH3CH2OH+HBr![]() CH3CH2Br+H2O
CH3CH2Br+H2O

有關數據見下表:
乙醇 | 溴乙烷 | 溴 | |
狀態 | 無色液體 | 無色液體 | 深紅色液體 |
密度/(g·cm3) | 0.79 | 1.44 | 3.1 |
沸點/℃ | 78.5 | 38.4 | 59 |
Ⅰ.溴乙烷的制備:
(1)若圖甲中A加熱溫度過高或濃硫酸的濃度過大,均會使C中收集到的粗產品呈橙色,原因是A中發生了副反應,其化學方程式為__________;F連接導管通入稀NaOH溶液中,其目的主要是_________;導管E的末端須低于D的水面,其目的是__________。
(2)為了除去粗產品中的氧化性雜質,宜選擇下列_________ (填序號)溶液來洗滌所得粗產品。
A.氫氧化鈉 B.碘化鉀 C.碳酸氫鈉 D.亞硫酸鈉
(3)粗產品用上述溶液洗滌、分液后,再經過蒸餾水洗滌、分液,然后加入少量的無水硫酸鎂固體,靜置片刻后過濾,再將所得濾液進行蒸餾,收集到的餾分約10.0g。從乙醇的角度考慮,本實驗所得溴乙烷的產率是___________。
Ⅱ.溴乙烷性質的探究
用如圖乙實驗裝置(鐵架臺、酒精燈略)驗證溴乙烷的性質:在試管中加入10mL6mol·L1NaOH溶液和2mL溴乙烷,振蕩、靜置,液體分層,水浴加熱。
(4)觀察到___________,表明溴乙烷與NaOH溶液已完全反應。
(5)為證明溴乙烷在NaOH乙醇溶液中反應的氣體產物為乙烯,將生成的氣體通入如圖丙裝置。a試管中的水的作用是 ___________,若無a試管,b試管中的試劑應為___________ 。
查看答案和解析>>
科目: 來源: 題型:
【題目】一定條件下,在一恒容密閉容器中,能表示反應 X(g)+2Y(g)![]() 2Z(g) 一定達到化學平衡狀態的是( )
2Z(g) 一定達到化學平衡狀態的是( )
①容器中氣體的密度不再發生變化 ② X、Y、Z的濃度不再發生變化 ③容器中的壓強不再發生變化 ④單位時間內生成n mol Z,同時生成2n mol Y
A.①②B.②③C.③④D.①④
查看答案和解析>>
科目: 來源: 題型:
【題目】在20世紀90年代末期,科學家發現并證明碳有新的單質形態![]() 存在。后來人們又相繼得到了
存在。后來人們又相繼得到了![]() 、
、![]() 、
、![]() 、
、![]() 等另外一些球碳分子。21世紀初,科學家又發現了管狀碳分子和洋蔥狀碳分子,大大豐富了碳元素單質的家族。下列有關說法錯誤的是
等另外一些球碳分子。21世紀初,科學家又發現了管狀碳分子和洋蔥狀碳分子,大大豐富了碳元素單質的家族。下列有關說法錯誤的是

A. 熔點比較: ![]()
B. ![]() 、
、![]() 、管狀碳和洋蔥狀碳之間的轉化屬于化學變化
、管狀碳和洋蔥狀碳之間的轉化屬于化學變化
C. ![]() 晶體結構如上圖所示,每個
晶體結構如上圖所示,每個![]() 分子周圍與它最近且等距離的
分子周圍與它最近且等距離的![]() 分子有12個
分子有12個
D. ![]() 、
、![]() 、管狀碳和洋蔥狀碳都不能與
、管狀碳和洋蔥狀碳都不能與![]() 發生反應
發生反應
查看答案和解析>>
科目: 來源: 題型:
【題目】氧化還原反應在生產生活中有著重要的應用。請按要求寫出相應的方程式。
(1)ClO2是一種高效安全的殺菌消毒劑。氯化鈉電解法生產ClO2工藝原理示意圖如下:
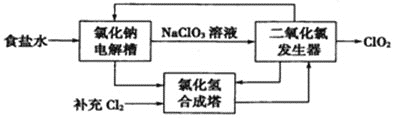
①寫出氯化鈉電解槽內發生反應的離子方程式:________________________。
②寫出ClO2發生器中的化學方程式,并標出電子轉移的方向及數目:_____________。
(2)甲醇燃料電池是采用鉑作電極催化劑,其工作原理的示意圖如下:
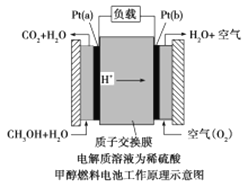
請回答下列問題:
Pt(a)電極是電池的_______極,電極反應式為______________________;
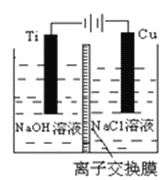
(3)方法Ⅱ采用離子交換膜控制電解液中OH-的濃度而制備納米Cu2O,裝置如圖所示,該電池的陽極反應式為______________________________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】某學生想制作一種家用環保型消毒液發生器,用石墨作電極解飽和氯化鈉溶液,通電時,為使Cl2被完成吸收投籃有較強殺菌能力的消毒液,設計了如圖所示的裝置,以下對電源電極名稱和消毒液和主要成分判斷正確的是( )
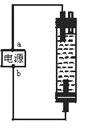
A.a為正極,b為負極:NaClO和NaCl
B.a為負極,b為正極:NaClO和NaCl
C.a為陽極,b為陰極:HClO和NaCl
D.a為陰極,b為陽極:HClO和NaCl
查看答案和解析>>
科目: 來源: 題型:
【題目】下列生產或實驗事實引出的相應結論不正確的是( )
選項 | 事實 | 結論 |
A | 其他條件相同,Na2S2O3溶液和H2SO4溶液反應,升高溶液的溫度,析出硫沉淀所需時間變短 | 當其他條件不變時,升高反應溫度,化學反應速率加快 |
B | 工業制硫酸中,在SO3的吸收階段,吸收塔里要裝填瓷環 | 增大氣液接觸面積,使SO3的吸收速率增大 |
C | 在容積可變的密閉容器中發生反應:2NH3(g) | 正反應速率加快,逆反應速率減慢 |
D | A、B兩支試管中分別加入等體積5%的H2O2,在B試管中加入2~3滴FeCl3溶液,B試管中產生氣泡快 | 當其他條件不變時,催化劑可以改變化學反應速率 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 來源: 題型:
【題目】有人設計將兩根鉑絲做電極插入到KOH溶液中,然后在兩極上分別通過甲烷和氧氣而構成燃料電池。該電池中反應的化學方程式為:CH4+2O2+2KOH![]() K2CO3+3H2O,則關于此燃料電池的下列說法中錯誤的是(1個電子所帶電量為1.6×10-19C)
K2CO3+3H2O,則關于此燃料電池的下列說法中錯誤的是(1個電子所帶電量為1.6×10-19C)
A.通過甲烷的電極為電池的負極,通過氧氣的電極為正極
B.在標準狀況下,每消耗5.6 L O2,可向外提供2.4×104C的電量
C.通過甲烷電極的電極反應為:CH4+10OH--8e-![]() CO32-+7H2O
CO32-+7H2O
D.放電一段時間后,溶液的pH減小
查看答案和解析>>
科目: 來源: 題型:
【題目】反應A(g)+3B(g)![]() 2C(g)+2D(g),在不同情況下測得反應速率,反應速率最快的是( )
2C(g)+2D(g),在不同情況下測得反應速率,反應速率最快的是( )
A. υ (C)=0.5 mol / L·s B. υ(D)=0.4 mol / L·s
C. υ(B)=0.6 mol / L·s D. υ(A)=0.15 mol / L·s
查看答案和解析>>
科目: 來源: 題型:
【題目】NiSO4·xH2O是一種綠色易溶于水的晶體,廣泛用于鍍鎳、電池等,可由電鍍廢渣(除鎳外,還含有銅、鋅、鐵等元素)為原料獲得。操作步驟如下:
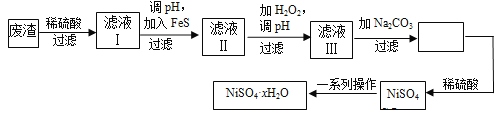
(1)在待鍍件上鍍鎳時,待鍍件應作_____極,電鍍過程中電解質溶液濃度 _____(填“增大”、“減小”、“不變”)
(2)向濾液Ⅰ中加入FeS是為了除去Cu2+、Zn2+等雜質,則除去Cu2+的離子方程式為_____________。當Zn2+恰好沉淀完全時,在CuS、ZnS共存的混合液中c(Zn2+)=10-5mol/L ,則c(Cu2+)=_____mol/L (已知Ksp(CuS)=1.3×10-36,Ksp(ZnS)=1.6×10-24)。
(3)對濾液Ⅱ中先加H2O2再調pH,調pH的目的是__________________________。
(4)濾液Ⅲ溶質的主要成分是NiSO4,加入Na2CO3過濾后再加適量稀硫酸溶解又生成NiSO4,這兩步操作的目的是______________________________。
(5)為測定NiSO4·xH2O晶體x的值,稱取26.3 g晶體加熱至充全失去結晶水,剩余固體15.5 g,則x的值等于___________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com