
科目: 來源: 題型:
【題目】次氯酸溶液是常用的消毒劑和漂白劑。某學習小組根據需要欲制備濃度不小于0.8mol/L的次氯酸溶液。
資料1:常溫常壓下,Cl2O為棕黃色氣體,沸點為3.8℃,42 ℃以上會分解生成Cl2和O2,Cl2O易溶于水并與水立即反應生成 HClO。
資料2:將氯氣和空氣(不參與反應)按體積比1∶3混合通入潮濕的碳酸鈉中發生反應2Cl2+2Na2CO3+H2O=Cl2O+2NaCl+2NaHCO3,用水吸收Cl2O(不含Cl2)制得次氯酸溶液。
(裝置及實驗)用以下裝置制備次氯酸溶液。
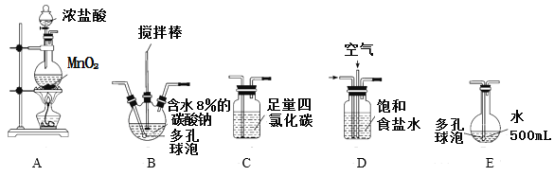
回答下列問題:
(1)各裝置的連接順序為_____→_____→_____→____→E。
(2)裝置A中反應的離子方程式是__________________________。
(3)實驗中控制氯氣與空氣體積比的方法是_____________________。
(4)反應過程中,裝置B需放在冷水中,其目的是_________________________。
(5)裝置E采用棕色圓底燒瓶是因為______________________。
(6)若裝置B中生成的Cl2O氣體有20%滯留在E前各裝置中,其余均溶于裝置E的水中,裝置E所得500mL次氯酸溶液濃度為0.8mol/L,則至少需要含水8%的碳酸鈉的質量為_________g。
(7)已知次氯酸可被H2O2、FeCl2等物質還原成Cl-。測定E中次氯酸溶液的物質的量濃度的實驗方案為:用________________準確量取20.00 mL次氯酸溶液,加入足量的________溶液,再加入足量的________溶液,過濾,洗滌,真空干燥,稱量沉淀的質量。(可選用的試劑:H2O2溶液、FeCl2溶液、AgNO3溶液。)
查看答案和解析>>
科目: 來源: 題型:
【題目】“中和滴定”原理在實際生產生活中應用廣泛。用I2O5可定量測定CO的含量,該反應原理為5CO+I2O5![]() 5CO2+I2。其實驗步驟如下:
5CO2+I2。其實驗步驟如下:
①取250 mL(標準狀況)含有CO的某氣體樣品通過盛有足量I2O5的干燥管中在170 ℃下充分反應;
②用水一乙醇液充分溶解產物I2,配制100 mL溶液;
③量取步驟②中溶液25.00 mL于錐形瓶中,然后用0.01 mol·L-1的Na2S2O3標準溶液滴定。消耗標準Na2S2O3溶液的體積如表所示。
第一次 | 第二次 | 第三次 | |
滴定前讀數/mL | 2.10 | 2.50 | 1.40 |
滴定后讀數/mL | 22.00 | 22.50 | 21.50 |
(1)步驟②中配制100 mL待測溶液需要用到的玻璃儀器的名稱是燒杯、量筒、玻璃棒、膠頭滴管和____________________。
(2)Na2S2O3標準液應裝在__________(填字母)中。

(3)指示劑應選用__________,判斷達到滴定終點的現象是____________________________________。
(4)氣體樣品中CO的體積分數為__________(已知:氣體樣品中其他成分不與I2O5反應:2Na2S2O3+I2=2NaI+Na2S4O6)
(5)下列操作會造成所測CO的體積分數偏大的是__________(填字母)。
a.滴定終點俯視讀數
b.錐形瓶用待測溶液潤洗
c.滴定前有氣泡,滴定后沒有氣泡
d.配制100 mL待測溶液時,有少量濺出
查看答案和解析>>
科目: 來源: 題型:
【題目】菱錳礦的主要成分是MnCO3,還含有少量Fe、Al、Ca、Mg等元素。氯化銨焙燒菱錳礦制備高純度碳酸錳的工藝流程如下:

已知:①相關金屬離子[c0(Mn+)=0.1 mol/L]形成氫氧化物沉淀的pH范圍如下:
金屬離子 | Al3+ | Fe3+ | Fe2+ | Ca2+ | Mn2+ | Mg2+ |
開始沉淀的pH | 3.8 | 1.5 | 6.3 | 10.6 | 8.8 | 9.6 |
沉淀完全的pH | 5.2 | 2.8 | 8.3 | 12.6 | 10.8 | 11.6 |
②常溫下,CaF2、MgF2的溶度積常數分別為1.46×10-10、 7.42×10-11
回答下列問題:
(1) “焙燒”時發生的主要反應的化學方程式為__________。氣體X為________(填化學式),寫出它生活中的一種用途_______________。
(2)焙燒時溫度對錳浸出率的影響如圖所示。焙燒時適應溫度為_______________。

(3)浸出液“凈化除雜”過程如下:首先用MnO2將Fe2+氧化為Fe3+,再調節溶液的pH將Al3+、Fe3+變成沉淀除去,溶液的pH的范圍為____然后加入NH4F將Ca2+、Mg2+轉化為CaF2、MgF2沉淀除去,兩種沉淀共存時,溶液中![]() =________(所得結果保留兩位小數)。
=________(所得結果保留兩位小數)。
(4)碳化結晶的原理(用離子方程式表示): ______________________。
(5)將制得的高純度碳酸錳溶于過量稀硫酸后用惰性電極電解,在某極得到重要的無機功能材料MnO2,該電極的電極反應式為_________。
(6)在該工藝流程中可以循環使用的物質有__________。(填化學式)
查看答案和解析>>
科目: 來源: 題型:
【題目】下列有關說法正確的是
A.電解精煉銅時,電解液CuSO4溶液的物質的量濃度不變
B.NaClO溶液中通入少量CO2后,ClO-水解程度增大,溶液堿性增強
C.SO3(g)+H2O(l)=H2SO4(aq)在常溫下能自發進行,則該反應的△H<0
D.0.1 mo1·L-1CH3COOH溶液加水稀釋后,溶液中![]() 的值減小
的值減小
查看答案和解析>>
科目: 來源: 題型:
【題目】可逆反應aA(s)+bB(g)![]() cC(g) +dD(g), 當其他條件不變時,某物質在混合物中的含量與溫度(T)、壓強(p)的關系如圖所示,以下正確的是( )
cC(g) +dD(g), 當其他條件不變時,某物質在混合物中的含量與溫度(T)、壓強(p)的關系如圖所示,以下正確的是( )
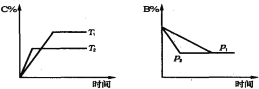
A. T1>T2,正反應放熱
B. Tl<T2,正反應吸熱
C. P1>P2,a+b>c+d
D. Pl<P2,b=c+d
查看答案和解析>>
科目: 來源: 題型:
【題目】工業上,從精制黑鎢礦(FeWO4、MnWO4)中提取金屬鎢的一種流程如下圖所示,該流程同時獲取副產物Fe2O3和MnCl2。

已知:I.過程①~④中,鎢的化合價均不變;
Ⅱ.常溫下鎢酸難溶于水;
Ⅲ.25℃時,Ksp[Fe(OH)3]=1.0×10-38,Ksp [Mn(OH)2]=4.0×10-14
回答下列問題:
(1)上述流程中的“濾渣1”除MnO2外還有_____、“氣體”除水蒸氣、HCl外還有____(均填化學式);
(2)過程①中MnWO4參與反應的化學方程式為______;FeWO4參與的反應中氧化劑與還原劑的物質的量之比為___________;
(3)已知WO3(s)+3H2(g)=W(s)+3H2O(g) ΔH=a kJ·mol-1
WO3(s)=WO3(g) ΔH=b kJ·mol-1
寫出WO3(g)與H2(g)反應生成W(s)的熱化學方程式:_______;
(4)過程⑦在25℃時調pH,至少應調至_______(當離子濃度等于1.0×10-5mol·L-1時,可認為其已沉淀完全);
(5)過程⑧要獲得MnCl2固體,在加熱時必須同時采取的一項措施是__________;
(6)鈉鎢青銅是一類特殊的非化學計量比化合物,其通式為NaxWO3,其中0<x<1,這類化合物具有特殊的物理化學性質,是一種低溫超導體。應用惰性電極電解熔融的Na2WO4和WO2混合物可以制備鈉鎢青銅,寫出WO42-在陰極上放電的電極反應式:___________。
查看答案和解析>>
科目: 來源: 題型:
【題目】磷酸亞鐵鋰(LiFePO4)電池是新能源汽車的動力電池之一。廢舊電池正極片(磷酸亞鐵鋰、炭黑和鋁箔等)可再生利用,其工藝流程如下:

已知:碳酸鋰在水中的溶解度,0℃時為1.54g,90℃時為0.85g,100℃時為0.71g。
(1)上述流程中至少需要經過______次過濾操作。
(2)“氧化”發生反應的離子方程式為__________;若用HNO3代替H2O2不足之處是_____。
(3)①已知Ksp[Fe(OH)3]=2.6×10-39。常溫下,在Fe(OH)3懸濁液中,當溶液的pH=3.0時,Fe3+的濃度為________mol/L。
②實際生產過程中,“調節pH”生成沉淀時,溶液pH與金屬元素的沉淀百分率(ω)的關系如下表:
pH | 3.5 | 5.0 | 6.5 | 8.0 | 10.0 | 12.0 |
ω(Fe)/% | 66.5 | 79.2 | 88.5 | 97.2 | 97.4 | 98.1 |
ω(Li)/% | 0.9 | 1.3 | 1.9 | 2.4 | 4.5 | 8.0 |
則最佳的沉淀pH=________。
(4)“沉鋰" 時的溫度應選(填標號)______為宜,并用___洗滌(填“熱水" 或“冷水")。
a.90℃ b.60 ℃ c.30 ℃ d.0 ℃
(5)磷酸亞鐵鋰電池在工作時,正極發生LiFePO4和FePO4的轉化,該電池放電時正極的電極反應式為________。
(6)工業上可以用FePO4、Li2CO3和H2C2O4作原料高溫焙燒制備 LiFePO4,該反應的化學方程式為________
查看答案和解析>>
科目: 來源: 題型:
【題目】常溫下鈦的化學活性很小,在較高溫度下可與多種物質反應。工業上由金紅石(含TiO2大于96%)為原料生產鈦的流程如下:
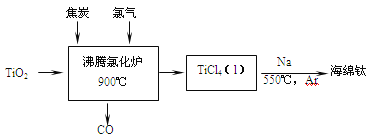
(1)TiCl4遇水強烈水解,寫出其水解的化學方程式___________________。
(2)①若液氯泄漏后遇到苯,在鋼瓶表面氯與苯的反應明顯加快,原因是___________。
②Cl2含量檢測儀工作原理如下圖,則Cl2在Pt電極放電的電極反應式為_______。
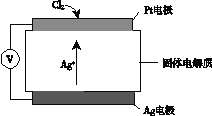
③實驗室也可用KClO3和濃鹽酸制取Cl2,方程式為:KClO3+ 6HCl(濃) =" KCl" + 3Cl2↑+ 3H2O。
當生成6.72LCl2(標準狀況下)時,轉移的電子的物質的量為____mol。
(3)一定條件下CO可以發生如下反應:4H2(g)+2CO(g)![]() CH3OCH3(g)+H2O(g) △H。
CH3OCH3(g)+H2O(g) △H。
①該反應的平衡常數表達式為K=_____________。
②將合成氣以n(H2)/n(CO)=2通入1 L的反應器中,CO的平衡轉化率隨溫度、壓強變化關系如圖所示,下列判斷正確的是___________(填序號)。
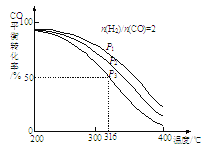
a.△H <0
b.P1<P2<P3
c.若在P3和316℃時,起始時n(H2)/n(CO)=3,則達到平衡時,CO轉化率小于50%
③采用一種新型的催化劑(主要成分是Cu-Mn的合金),利用CO和H2制備二甲醚(簡稱DME)。觀察下圖回答問題。
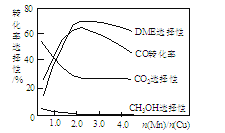
催化劑中n(Mn)/n(Cu)約為___________時最有利于二甲醚的合成。
查看答案和解析>>
科目: 來源: 題型:
【題目】某含鎳(Ni)廢催化劑中主要含有Ni,還含有Al、Al2O3、Fe及其它不溶于酸、堿的雜質。部分金屬氫氧化物Ksp近似值如下表所示:
化學式 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 |
Ksp近似值 | 10-17 | 10-39 | 10-34 | 10-15 |
現用含鎳廢催化劑制備NiSO47H2O晶體,其流程圖如下:
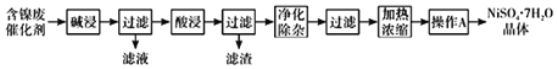
回答下列問題:
(1)“堿浸”時發生反應的離子方程式為______。
(2)“酸浸”所使用的酸為______。
(3)“凈化除雜”需加入H2O2溶液,其作用是______。然后調節pH使溶液中鐵元素恰好完全沉淀,列式計算此時的pH。______
(4)“操作A”為______、過濾、洗滌、干燥,即得產品。
(5)NiSO4在強堿性溶液中可被NaClO氧化為NiOOH,該反應的離子方程式為______。
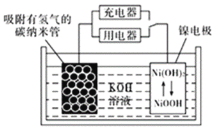
(6)NiOOH可作為鎳氫電池的電極材料,該電池的工作原理如圖所示,其放電時,正極的電極反應式為______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com