
科目: 來源: 題型:
【題目】碳酸二甲酯(DMC)是一種無毒、環保性能優異、用途廣泛的化工原料.在催化劑作用下,可由甲醇和CO2直接合成碳酸二甲酯:CO2+2CH3OH→CO(OCH3)2 + H2O 。某研究小組在其他條件不變的情況下,通過研究催化劑用量分別對轉化數(TON ) 的影響來評價催化劑的催化效果.計算公式為TON=轉化的甲醇的物質的量/催化劑的物質的量.根據該研究小組的實驗及催化劑用量TON的影響圖,判斷下列說法不正確的是
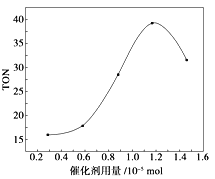
A.由甲醇和CO2直接合成碳酸二甲酯,可以利用價廉易得的甲醇把影響環境的溫室氣體CO2轉化為資源,在資源循環利用和環境保護方面都具有重要意義
B.在反應體系中添加合適的吸水劑,將提高該反應的TON
C.當催化劑用量為1.2×10-5mol時,該反應的TON 達到最高點
D.當催化劑用量高于1.2×10-5mol時,隨著催化劑用量的增加,甲醇的平衡轉化率逐漸降低
查看答案和解析>>
科目: 來源: 題型:
【題目】已知反應X(g)+Y(g)![]() R(g)+Q(g)的平衡常數與溫度的關系如表所示。830 ℃時,向一個2 L的密閉容器中充入0.2 mol X和0.8 mol Y,反應初始4 s內v(X)=0.005 mol/(L·s)。下列說法正確的是
R(g)+Q(g)的平衡常數與溫度的關系如表所示。830 ℃時,向一個2 L的密閉容器中充入0.2 mol X和0.8 mol Y,反應初始4 s內v(X)=0.005 mol/(L·s)。下列說法正確的是
溫度/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
平衡常數 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
A. 4 s時容器內c(Y)=0.76 mol/L
B. 830 ℃達平衡時,X的轉化率為80%
C. 反應達平衡后,升高溫度,平衡正向移動
D. 1 200 ℃時反應R(g)+Q(g) ![]() X(g)+Y(g)的平衡常數K=0.4
X(g)+Y(g)的平衡常數K=0.4
查看答案和解析>>
科目: 來源: 題型:
【題目】將一定量的Cu和濃硫酸反應(裝置中的夾持、加熱儀器省略),反應后,圓底燒瓶內的混合液倒入水中,得到藍色溶液與少量黑色不溶物。
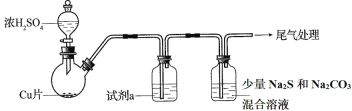
(1)反應后藍色溶液呈酸性的原因有①______________,②______________。
(2)為檢驗反應產生氣體的還原性,試劑 a 是______________。
(3)已知酸性:H2SO3>H2CO3>H2S。反應后測得 Na2S 和 Na2CO3 混合溶液中有新氣體生成。該氣體中 ______________ (填“含或不含”) H2S,理由是______________;
(4)少量黑色不溶物不可能是 CuO 的理由是______________。
查閱資料后發現該黑色固體可能是 CuS 或 Cu2S 中的一種或兩種,且 CuS 和 Cu2S 在空氣中煅燒易轉 化成 Cu2O 和 SO2。稱取 2.000g 黑色固體,灼燒、冷卻、……最后稱得固體 1.680g。
(5) 灼燒該固體除用到酒精燈、坩堝、坩堝鉗、三腳架等儀器,還需要______________。 確定黑色固體灼燒充分的依據是______________,黑色不溶物其成分化學式為______________。
查看答案和解析>>
科目: 來源: 題型:
【題目】已知某有機物結構為: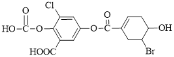 ,下列說法中正確的是
,下列說法中正確的是
A.該物質的化學式為C15H8O8BrCl
B.該物質能與FeCl3 溶液發生顯色反應
C.1 mol 該物質最多能與 2 mol 溴水發生反應
D.一定條件下,1 mol 該物質最多能與 9 mol NaOH 反應
查看答案和解析>>
科目: 來源: 題型:
【題目】過氧化鈣![]() 難溶于水,在常溫下穩定,在潮濕空氣及水中緩慢分解放出氧氣,因而廣泛應用于漁業、農業、環保等許多方面。下圖是以大理石
難溶于水,在常溫下穩定,在潮濕空氣及水中緩慢分解放出氧氣,因而廣泛應用于漁業、農業、環保等許多方面。下圖是以大理石![]() 主要雜質是氧化鐵
主要雜質是氧化鐵![]() 等為原料制取過氧化鈣
等為原料制取過氧化鈣![]() 的流程。
的流程。
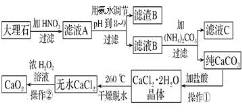
請回答下列問題:
![]() 操作
操作![]() 應包括下列操作中的________。
應包括下列操作中的________。![]() 填序號
填序號![]()
A 溶解 ![]() 過濾
過濾 ![]() 蒸餾
蒸餾 ![]() 分液
分液 ![]() 蒸發結晶
蒸發結晶
![]() 用氨水調節pH至
用氨水調節pH至![]() 的目的是________。
的目的是________。
![]() 若測得濾液C中
若測得濾液C中![]() ,則
,則![]() ________
________![]() 填“是”或“不”
填“是”或“不”![]() 沉淀完全。
沉淀完全。![]() 已知
已知![]() 時即可視為沉淀完全;
時即可視為沉淀完全;![]()
![]() 若在濾液C中,加入
若在濾液C中,加入![]() 使溶液呈酸性以得到副產物
使溶液呈酸性以得到副產物![]() ,則酸化后溶液中
,則酸化后溶液中![]() ____________
____________![]() 填“
填“![]() ”、“
”、“![]() ”、“
”、“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() 。
。
![]() 操作
操作![]() 是:在低溫下,往過氧化氫濃溶液中投入無水氯化鈣進行反應,一段時間后,再加入氫氧化鈉溶液,當調節溶液pH至
是:在低溫下,往過氧化氫濃溶液中投入無水氯化鈣進行反應,一段時間后,再加入氫氧化鈉溶液,當調節溶液pH至![]() ,才出現大量沉淀。寫出該反應的化學方程式________;用簡要的文字解釋用氫氧化鈉調節pH至
,才出現大量沉淀。寫出該反應的化學方程式________;用簡要的文字解釋用氫氧化鈉調節pH至![]() 的原因_________。
的原因_________。
![]() 已知大理石含
已知大理石含![]() 的質量分數為a,
的質量分數為a,![]() 大理石可以制得
大理石可以制得![]() ,請計算:
,請計算:![]() 轉化為
轉化為![]() 過程中,Ca原子的利用率________。
過程中,Ca原子的利用率________。
查看答案和解析>>
科目: 來源: 題型:
【題目】已知:①H2 (g) + Se (g) ![]() H2Se (g) +87.48kJ ②Se (g) → Se (s) +102.17kJ; 下列選項正確的是
H2Se (g) +87.48kJ ②Se (g) → Se (s) +102.17kJ; 下列選項正確的是
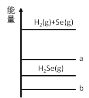
A.H2 (g) + Se (s)的總能量對應圖中線段 b
B.相同物質的量的 Se,Se(s)的能量高于 Se(g)
C.1mol Se (g)中通入 1mol H2(g),反應放熱 87.48kJ
D.H2 (g) + S (g) ![]() H2S (g) +QkJ ,Q< 87.48kJ
H2S (g) +QkJ ,Q< 87.48kJ
查看答案和解析>>
科目: 來源: 題型:
【題目】下圖為某城市某日空氣質量報告,下列敘述與報告內容不相符的是

A. 該日空氣首要污染物是PM10
B. 該日空氣質量等級屬于中度污染
C. 污染物NO2、CO可能主要來源于機動車尾氣
D. PM2.5、PM10指的是懸浮顆粒物,會影響人體健康
查看答案和解析>>
科目: 來源: 題型:
【題目】a、b、c、d 四種短周期元素在周期表中的位置如圖所示,a 和 b 分別位于周期表的第 2 列和第 13 列, 下列敘述正確的

A.離子半徑 b>d
B.b 可以和強堿溶液發生反應
C.c 的氫化物空間結構為三角錐形
D.a 的最高價氧化物對應水化物是強堿
查看答案和解析>>
科目: 來源: 題型:
【題目】著名化學家徐光憲在稀土領域貢獻突出,被譽為“稀土界的袁隆平”。釔是稀土元素之一,我國蘊藏著豐富的釔礦石![]() ,工業上通過如下工藝流程制取氧化釔,并獲得副產物鈹。
,工業上通過如下工藝流程制取氧化釔,并獲得副產物鈹。
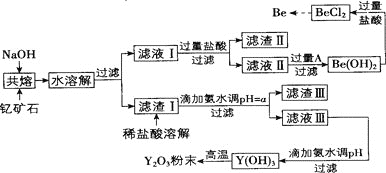
已知:
![]() 釔
釔![]() 的常見化合價為
的常見化合價為![]() 價;
價;
![]() 鈹和鋁處于元素周期表的對角線位置,化學性質相似;
鈹和鋁處于元素周期表的對角線位置,化學性質相似;
![]() 、
、![]() 形成氫氧化物沉淀時的pH如下表:
形成氫氧化物沉淀時的pH如下表:
離子 | 開始沉淀時的pH | 完全沉淀時的pH |
Fe3+ | 2:1 | 3:1 |
Y3+ | 6.0 | 8.3 |
![]() 將釔礦石與NaOH共熔的反應方程式補充完整:
將釔礦石與NaOH共熔的反應方程式補充完整:
_____![]() _____
_____![]() _____
_____![]() _____
_____![]() _____
_____![]() _____
_____![]() _____
_____![]() _____
_____![]()
![]() 濾渣Ⅱ的主要成分是_________。
濾渣Ⅱ的主要成分是_________。
![]() 試劑A可以是_________
試劑A可以是_________![]() 填序號
填序號![]() 。
。
A NaOH溶液 ![]() 氨水
氨水 ![]()
![]()
![]() 用氨水調節
用氨水調節![]() 時,a的取值范圍是_____________。
時,a的取值范圍是_____________。
![]() 計算常溫下
計算常溫下![]() 的平衡常數
的平衡常數![]() ____________。
____________。![]() 常溫下
常溫下![]()
![]() 濾液Ⅲ加入氨水產生沉淀的離子方程式為___________。
濾液Ⅲ加入氨水產生沉淀的離子方程式為___________。
![]() 從
從![]() 溶液中得到
溶液中得到![]() 固體的操作是_______。
固體的操作是_______。
查看答案和解析>>
科目: 來源: 題型:
【題目】有機化合物A的分子式是C13H20O8(相對分子質量為304),1molA在酸性條件下與4mol![]() 反應得到4molCH2COOH和1molB.下列說法錯誤的是
反應得到4molCH2COOH和1molB.下列說法錯誤的是
A. A和B的相對分子質量之差為168
B. B一定不能發生加成反應
C. 有機物B與CH3CH2OH互為同系物
D. 分子式為C5H1002且與CH2COOH屬于同類物質的有機物只有4種
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com