
【題目】將一定量的Cu和濃硫酸反應(裝置中的夾持、加熱儀器省略),反應后,圓底燒瓶內的混合液倒入水中,得到藍色溶液與少量黑色不溶物。
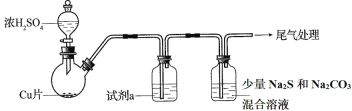
(1)反應后藍色溶液呈酸性的原因有①______________,②______________。
(2)為檢驗反應產生氣體的還原性,試劑 a 是______________。
(3)已知酸性:H2SO3>H2CO3>H2S。反應后測得 Na2S 和 Na2CO3 混合溶液中有新氣體生成。該氣體中 ______________ (填“含或不含”) H2S,理由是______________;
(4)少量黑色不溶物不可能是 CuO 的理由是______________。
查閱資料后發現該黑色固體可能是 CuS 或 Cu2S 中的一種或兩種,且 CuS 和 Cu2S 在空氣中煅燒易轉 化成 Cu2O 和 SO2。稱取 2.000g 黑色固體,灼燒、冷卻、……最后稱得固體 1.680g。
(5) 灼燒該固體除用到酒精燈、坩堝、坩堝鉗、三腳架等儀器,還需要______________。 確定黑色固體灼燒充分的依據是______________,黑色不溶物其成分化學式為______________。
【答案】反應后期濃硫酸變稀,而銅和稀硫酸不發生反應,硫酸有剩余 硫酸銅溶液水解呈酸性 溴水或酸性高錳酸鉀 不含 硫化氫和二氧化硫反應 氧化銅能與稀硫酸反應 玻璃棒;泥三角 充分灼燒的依據是再次灼燒,冷卻,稱量,兩次的質量差不能超過0.001g; CuS 和Cu2S
【解析】
(1)銅和濃硫酸反應,隨著反應的進行,濃硫酸會變成稀硫酸,稀硫酸與銅不反應,生成的硫酸銅水解顯酸性;
(2)檢驗二氧化硫的還原性,可以用具有氧化性的物質,且反應現象明顯;
(3)依據硫化氫和二氧化硫反應進行分析;
(4)氧化銅可以和稀硫酸反應;
(5)依據現象進行分析;
(1)隨著反應的進行濃硫酸會變成稀硫酸,稀硫酸與銅不反應,使溶液顯酸性,生成的硫酸銅水解使溶液顯酸性,
故答案為:反應后期濃硫酸變稀,而銅和稀硫酸不發生反應,硫酸有剩余;硫酸銅溶液水解呈酸性;
(2)二氧化硫有還原性,所以可以用溴水或者酸性高錳酸鉀溶液檢驗,
故答案為,溴水或酸性高錳酸鉀;
(3)Na2S 和 Na2CO3 混合溶液中通入二氧化硫,不會生成硫化氫,因為硫化氫和二氧化硫發生反應,
故答案為:不含;硫化氫和二氧化硫反應;
(4)少量黑色不溶物不可能是 CuO,因為氧化銅可以和稀硫酸反應,
故答案為:氧化銅能與稀硫酸反應;
(5)灼燒固體時除了需要酒精燈、坩堝、坩堝鉗、三腳架等儀器外,還需要玻璃棒,泥三角,充分灼燒的依據是再次灼燒,冷卻,稱量,兩次的質量差不能超過0.001g, 設CuSxmol,Cu2Symol,96x+160y=2;(x+y)80=1.68,解得,x=0.02,y=0.005,故兩者都有,
故答案為:玻璃棒;泥三角;充分灼燒的依據是再次灼燒,冷卻,稱量,兩次的質量差不能超過0.001g; CuS 和Cu2S。


 期末沖刺100分創新金卷完全試卷系列答案
期末沖刺100分創新金卷完全試卷系列答案科目:高中化學 來源: 題型:
【題目】下列圖示與對應的敘述相符的是
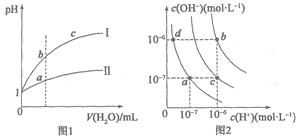
A.圖1表示相同溫度下pH=1的鹽酸和醋酸溶液分別加水稀釋時pH的變化曲線,其中曲線II為鹽酸,且b點溶液的導電性比a點強
B.圖1中,中和等體積的兩種酸,消耗等濃度的NaOH溶液體積V(I)>V(II)
C.圖2中純水僅升高溫度,就可以從a點變到c點
D.圖2中在b點對應溫度下,將pH=2的H2SO4與pH=10的NaOH溶液等體積混合后,溶液顯中性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知有機物F和高分子N的合成路線如圖所示:
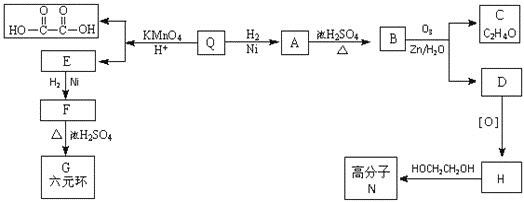
已知:RCH=CHR'![]() RCOOH+R'COOH,RCH=CHR'
RCOOH+R'COOH,RCH=CHR'![]() RCHO+R'CHO
RCHO+R'CHO
![]() 只含碳、氫、氧三種元素,且其碳、氫、氧元素質量比為
只含碳、氫、氧三種元素,且其碳、氫、氧元素質量比為![]() ,經測定Q的相對分子質量是128。
,經測定Q的相對分子質量是128。![]() 可與
可與![]() 加成,并能與
加成,并能與![]() 恰好完全反應,且分子中無支鏈。Q的分子式是 ______________。
恰好完全反應,且分子中無支鏈。Q的分子式是 ______________。
![]() 所含官能團的名稱是 ___________、 _____________;
所含官能團的名稱是 ___________、 _____________;![]() 的反應類型是 ________________;
的反應類型是 ________________;
![]() 寫出C與銀氨溶液反應的化學方程式: _______________;
寫出C與銀氨溶液反應的化學方程式: _______________;
![]() 的結構簡式是 _______________;Q的反式結構簡式是 ____________。
的結構簡式是 _______________;Q的反式結構簡式是 ____________。
![]() 下列說法正確的是 _________________。
下列說法正確的是 _________________。
A. C能與苯酚在一定條件下生成高分子化合物
B. D催化加氫的產物與F互為同分異構體
C. F能發生氧化反應、取代反應、加成反應
D. 高分子N的每條分子鏈中含有![]() 個酯基
個酯基
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常見有機物間的轉化關系如圖所示(以下變化中,某些反應條件及產物未標明)。A是天然有機高分子化合物,D是一種重要的化工原料。在相同條件下,G蒸氣密度是氫氣的44倍。
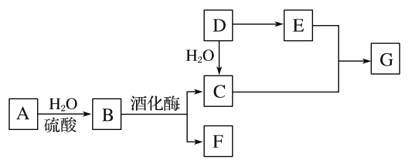
(1)D中官能團的名稱:______________________________________。
(2)C和E反應的化學方程式:________________________。
(3)檢驗A轉化過程中有B生成,先中和水解液,再需要加入的試劑是________________________________。
(4)某烴X的相對分子質量是D、F之和,分子中碳與氫的質量之比是5∶1。下列說法正確的是________(填字母)。
A.X 不溶于水,與甲烷互為同系物
B.X性質穩定,高溫下不會分解
C.X不存在含有3個甲基的同分異構體
D.X可能和溴水發生加成反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】a、b、c、d 四種短周期元素在周期表中的位置如圖所示,a 和 b 分別位于周期表的第 2 列和第 13 列, 下列敘述正確的

A.離子半徑 b>d
B.b 可以和強堿溶液發生反應
C.c 的氫化物空間結構為三角錐形
D.a 的最高價氧化物對應水化物是強堿
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CO2催化加氫制取甲醇、乙醇等低碳醇的研究,對于環境問題和能源問題都具有非常重要的意義。已知一定條件下的如下反應:
CO2(g) + 3H2(g) ![]() CH3OH(g) + H2O(g) H =-49.0 kJ· mol-1
CH3OH(g) + H2O(g) H =-49.0 kJ· mol-1
2CO2(g) + 6H2(g) ![]() CH3CH2OH(g) + 3H2O(g) H=-173.6 kJ· mol-1
CH3CH2OH(g) + 3H2O(g) H=-173.6 kJ· mol-1
下列說法不正確的是
A.CH3OH(g) + CO2(g) + 3H2(g) ![]() CH3CH2OH(g) + 2H2O(g) H<0
CH3CH2OH(g) + 2H2O(g) H<0
B.增大壓強,有利于反應向生成低碳醇的方向移動,平衡常數增大
C.升高溫度,可以加快生成低碳醇的速率,但反應限度降低
D.增大氫氣濃度可以提高二氧化碳的轉化率
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】綠色化學又稱環境友好化學,它的主要特點之一是提高原子的利用率,使原料中所有的原子全部 轉化到產品中,實現“零排放”。下列反應符合綠色化學這一特點的是
A. 工業冶煉 Fe2O3+3CO ![]() 2Fe+3CO2
2Fe+3CO2
B. 用生石灰制熟石灰 CaO+H2O=Ca(OH)2
C. 實驗室制取二氧化碳 CaCO3+2HCl=CaCl2+H2O+CO2↑
D. 實驗室制取氫氣 Zn+H2SO4=ZnSO4+H2↑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CoCl2可用于電鍍,是一種性能優越的電池前驅材料,由含鈷礦(Co元素主要以Co2O3、CoO存在,還含有Fe、Si、Cu、Zn、Mn、Ni、Mg、Ca元素)制取氯化鈷晶體的一種工藝流程如下:
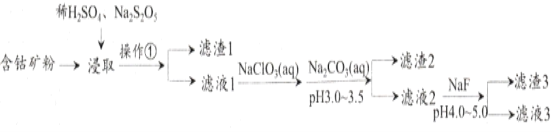
已知:①焦亞硫酸鈉Na2S2O5,常做食品抗氧化劑。CaF2、MgF2難溶于水。
②CoCl2·6H2O熔點86℃,易溶于水、乙醚等;常溫下穩定無毒,加熱至110—120℃時,失去結晶水變成有毒的無水氯化鈷。
③部分金屬離子形成氫氧化物的pH見下表:
Co3+ | Fe3+ | Cu2+ | Co2+ | Fe2+ | Zn2+ | Mn2+ | Mg2+ | |
開始沉淀pH | 0.3 | 2.7 | 5.5 | 7.2 | 7.6 | 7.6 | 8.3 | 9.6 |
完全沉淀pH | 1.1 | 3.2 | 6.6 | 9.2 | 9.6 | 9.2 | 9.3 | 11.1 |
回答下列問題:
(1)操作①的名稱為_________,NaClO3具有氧化性,其名稱為__________________。
(2)浸取中加入Na2S2O5的作用是___________________________。
(3)濾液1中加入NaClO3/span>的作用是_______________________________________,相關的離子方程式為__________________________________________。
(4)加入Na2CO3溶液生成濾渣2的主要離子方程式為___________________________。
(5)濾渣3主要成分為________________________(寫化學式)。
濾液3經過多次萃取與反萃取制備CoCl2晶體
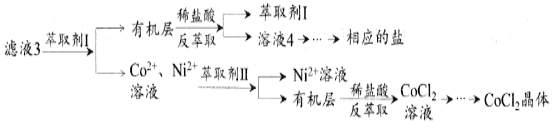
(6)濾液3中加入萃取劑I,然后用稀鹽酸反萃取的目的是_______________________。
(7)制備晶體CoCl2·6H2O,需在減壓環境下烘干的原因是_________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】馬日夫鹽[Mn(H2PO4)2·2H2O]主要用作磷化劑;以軟錳礦(主要成分為MnO2及少量的FeO、Al2O3和SiO2)為原料制備馬日夫鹽的主要工藝流程如圖:
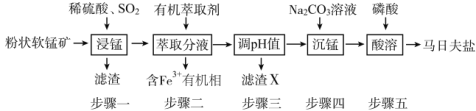
(1)按照無機物命名規律,馬日夫鹽[Mn(H2PO4)2·2H2O的化學名稱為___。
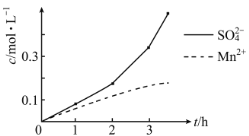
(2)步驟一中,MnO2被SO2和___還原。若SO2氣體中混有空氣,測得反應液中Mn2+、SO42-的濃度隨反應時間t變化如圖,科研人員認為Mn2+對O2與H2SO3反應起催化作用,其理由是__。
(3)濾渣X主要成分為___;步驟三調節pH時,最適宜加入的物質是__。
A.過量稀鹽酸 B.適量Na2CO3溶液
C.適量磷酸溶液 D.過量CaCO3
(4)在沉錳過程中,應將Na2CO3溶液逐量加入錳鹽溶液中,如果顛倒試劑混合順序會有Mn(OH)2生成,其原因是Na2CO3溶液具有較強__性;步驟五產生馬日夫鹽晶體的化學反應方程式為__。
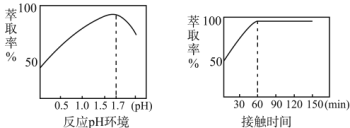
(5)Fe3+的萃取率與溶液的pH和接觸時間之間的關系如圖,據此分析,萃取的最佳條件為____。
(6)馬日夫鹽作防銹磷化劑的原因是利用其較強的酸性以及在防銹處理過程中生成了具有保護作用的FeHPO4,馬日夫鹽顯酸性的主要原因是__(用相關化學用語回答)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com