
科目: 來源: 題型:
【題目】次氯酸溶液是常用的消毒劑和漂白劑。某學習小組根據需要欲制備濃度不小于0.8mol/L的次氯酸溶液。
資料1:常溫常壓下,Cl2O為棕黃色氣體,沸點為3.8℃,42 ℃以上會分解生成Cl2和O2,Cl2O易溶于水并與水立即反應生成 HClO。
資料2:將氯氣和空氣(不參與反應)按體積比1∶3混合通入潮濕的碳酸鈉中發生反應2Cl2+2Na2CO3+H2O=Cl2O+2NaCl+2NaHCO3,用水吸收Cl2O(不含Cl2)制得次氯酸溶液。(裝置及實驗)用以下裝置制備次氯酸溶液。
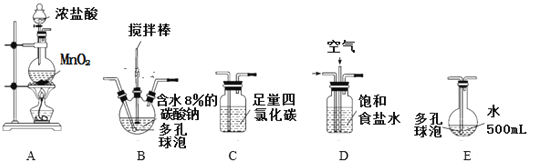
回答下列問題:
(1)各裝置的連接順序為_____→_____→_____→____→E。
(2)反應過程中,裝置B需放在冷水中,其目的是_________________________。
(3)裝置C的主要作用是______________________。
(4)若裝置B中生成的Cl2O氣體有20%滯留在E前各裝置中,其余均溶于裝置E的水中,裝置E所得500mL次氯酸溶液濃度為0.8mol/L,則至少需要含水8%的碳酸鈉的質量為_________g。
(5)已知次氯酸可被H2O2、FeCl2等物質還原成Cl-。測定E中次氯酸溶液的物質的量濃度的實驗方案為:用________________準確量取20.00 mL次氯酸溶液,加入足量的________溶液,再加入足量的________溶液,過濾,洗滌,真空干燥,稱量沉淀的質量。(可選用的試劑:H2O2溶液、FeCl2溶液、AgNO3溶液。)
查看答案和解析>>
科目: 來源: 題型:
【題目】由Al、CuO、Fe2O3組成的混合物共10.0g,放入500mL某濃度的鹽酸中,混合物完全溶解,當再加入250mL 2.00mol/L的NaOH溶液時,得到沉淀最多。上述鹽酸的濃度為( )
A. 1.00 mol/LB. 0.500 mol/L
C. 2.00 mol/LD. 3.00 mol/L
查看答案和解析>>
科目: 來源: 題型:
【題目】下列實驗方案中,能達到相應實驗目的的是
實驗方案 |
|
|
|
|
目的 | A.比較乙醇分子中羥基氫原子和水分子中氫原子的活潑性 | B.除去乙烯中的二氧化硫 | C.制銀氨溶液 | D.證明碳酸酸性強于苯酚 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 來源: 題型:
【題目】在高溫下, Al與Fe2O3發生鋁熱反應后得到的固體混合物中主要含有Al2O3、Fe,還含有少量Fe2O3。從該樣品中固體混合物分離出Al2O3,并回收Fe和Fe2O3的流程如下:

已知:NaAlO2 + CO2 + 2H2O = Al(OH)3↓ + NaHCO3
回答下列問題:
(1)固體①的成分是__________。溶液②的溶質是____________。
(2)加入過量NaOH溶液時,發生反應的離子方程式是__________。
(3)白色固體②與NaOH溶液反應的離子方程式是__________。
查看答案和解析>>
科目: 來源: 題型:
【題目】蒽(![]() )與苯炔(
)與苯炔(![]() )反應生成化合物X(立體對稱圖形),如圖所示:
)反應生成化合物X(立體對稱圖形),如圖所示:
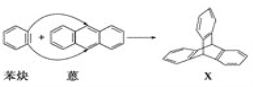
(1)蒽與X都屬于___(填字母)。
a.飽和烴 b.不飽和烴
(2)苯炔的分子式為___,苯炔不具有的性質是___(填字母)。
a.能溶于水 b.能發生氧化反應 c.能發生加成反應 d.常溫常壓下為氣體
(3)下列屬于苯的同系物的是___(填字母,下同)。
A.![]() B.
B.![]()
C.![]() D.
D.![]()
(4)下列物質中,能發生加成反應,也能發生取代反應,同時能使溴水因加成反應而褪色,還能使酸性高錳酸鉀溶液褪色的是___。
A.![]() B.C6H14 C.
B.C6H14 C.![]() D.
D.![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】滿足下列條件的有機物的種類數正確的是
選項 | 有機物 | 條件 | 種類數 |
A | C5H10O2 | 在酸性條件下會水解生成甲和乙,且甲、乙的相對分子質量相等 | 4 |
B | C6H12O2 | 能與 NaHCO3溶液反應 | 3 |
C | C5H12O | 含有2個甲基的醇 | 5 |
D |
| 該有機物的一氯代物 | 4 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 來源: 題型:
【題目】下列實驗裝置能達到實驗目的是(夾持儀器未畫出)
A. 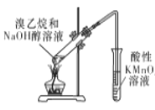 用于檢驗溴乙烷消去生成的乙烯
用于檢驗溴乙烷消去生成的乙烯
B. 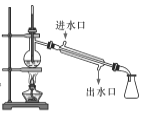 用于石油的分餾
用于石油的分餾
C. 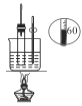 用于實驗室制硝基苯
用于實驗室制硝基苯
D. 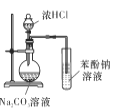 可證明酸性:鹽酸>碳酸>苯酚
可證明酸性:鹽酸>碳酸>苯酚
查看答案和解析>>
科目: 來源: 題型:
【題目】盆烯是近年合成的一種有機物,它的分子結構可簡化表示為![]() (其中C、H原子已略去),下列關于盆烯的說法中錯誤的是( )
(其中C、H原子已略去),下列關于盆烯的說法中錯誤的是( )
A. 盆烯是苯的一種同分異構體
B. 盆烯分子中所有的碳原子不可能在同一平面上
C. 盆烯是乙烯的一種同系物
D. 盆烯在一定條件下可以發生加成反應
查看答案和解析>>
科目: 來源: 題型:
【題目】已知X、Y、Z、W是短周期元素中的四種非金屬元素,它們的原子序數依次增大。X元素的原子形成的離子就是一個質子,Z、W在元素周期表中處于相鄰的位置,它們的單質在常溫下均為無色氣體,Y原子的最外層電子數是內層電子數的2倍。
(1)請寫出元素符號:Y__Z____W____。
(2)在一定條件下,由X單質與Z單質反應生成E,E在催化劑存在的條件下,可用于還原汽車尾氣中的____,以減少對大氣的污染。
(3)由X、Y、Z、W四種元素可組成酸式鹽,該化合物的水溶液與足量NaOH溶液在加熱條件下反應的離子方程式為____。
(4)工業上用E檢驗輸送氯氣的管道是否漏氣,可觀察到大量白煙,同時有單質Z生成,寫出化學方程式____。該反應中被氧化的E與參與反應的E的質量之比___。
查看答案和解析>>
科目: 來源: 題型:
【題目】燃料電池是目前電池研究的熱點之一,現有某課外小組自制的氫氧燃料電池,如圖所示,a、b均為惰性電極。下列敘述正確的是
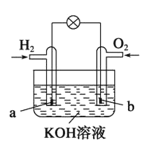
A.總反應方程式為2H2+O2![]() 2H2O
2H2O
B.a極反應是H2-2e-=2H+
C.使用過程中電解質溶液的pH逐漸減小
D.b電極是正極,該電極上發生氧化反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com