
科目: 來源: 題型:
【題目】(1)現有![]() 某氣體(由雙原子分子構成),其摩爾質量為
某氣體(由雙原子分子構成),其摩爾質量為![]() ,阿伏加德羅常數用
,阿伏加德羅常數用![]() 表示,試求
表示,試求
①該氣體在標準狀況下的體積為____![]() 。
。
②該氣體所含原子數為____。
(2)用雙線橋表示銅與濃硫酸反應的電子轉移方向和數目:__________________

當有![]() 被還原時,轉移電子的物質的量為____
被還原時,轉移電子的物質的量為____![]() ,生成標準狀況下
,生成標準狀況下![]() 的體積為___
的體積為___![]() 。
。
查看答案和解析>>
科目: 來源: 題型:
【題目】某研究性學習小組同學對由NaHCO3和KHCO3組成的某均勻混合物進行實驗,測得如下數據(鹽酸的物質的量濃度相等):
50mL鹽酸 | 50mL鹽酸 | 50mL鹽酸 | |
m(混合物) | 9.2g | 15.7g | 27.6g |
標準狀況下,V(CO2) | 2.24L | 3.36L | 3.36L |
(1)鹽酸的物質的量濃度為_________。
(2)混合物中,n(NaHCO3):n(KHCO3)=_________。
查看答案和解析>>
科目: 來源: 題型:
【題目】某純堿樣品含有少量![]() 雜質,某興趣小組用如圖所示裝置測定純堿樣品中
雜質,某興趣小組用如圖所示裝置測定純堿樣品中![]() 的質量分數(鐵架臺、鐵夾等均已略去)。
的質量分數(鐵架臺、鐵夾等均已略去)。
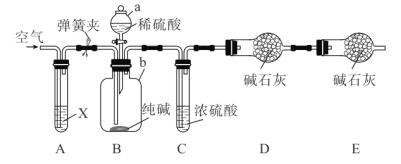
實驗步驟如下:
Ⅰ.按圖連接裝置,并檢查氣密性;
Ⅱ.準確稱量盛有堿石灰的干燥管![]() 的質量為
的質量為![]() ;
;
Ⅲ.準確稱量![]() 純堿樣品放入容器
純堿樣品放入容器![]() 中;
中;
Ⅳ.打開分液漏斗![]() 的旋塞,緩緩滴入稀硫酸,至不再產生氣泡為止;
的旋塞,緩緩滴入稀硫酸,至不再產生氣泡為止;
Ⅴ.打開彈簧夾,往試管![]() 中緩緩鼓入空氣數分鐘,最后稱得干燥管
中緩緩鼓入空氣數分鐘,最后稱得干燥管![]() 的質量為
的質量為![]() 。
。
請回答下列問題:
(1)檢查裝置![]() 氣密性的方法為____________。
氣密性的方法為____________。
(2)裝置![]() 中試劑
中試劑![]() 應選擇_____,目的是________。
應選擇_____,目的是________。
(3)裝置![]() 的作用是____,步驟
的作用是____,步驟![]() 中“緩緩鼓入空氣數分鐘”的目的是____________。
中“緩緩鼓入空氣數分鐘”的目的是____________。
(4)根據實驗中測得的有關數據,計算純堿樣品![]() 的質量分數為___(保留三位有效數字),若沒有裝置
的質量分數為___(保留三位有效數字),若沒有裝置![]() ,會導致測量結果____(填“偏大”“偏小”或“無影響”)。
,會導致測量結果____(填“偏大”“偏小”或“無影響”)。
查看答案和解析>>
科目: 來源: 題型:
【題目】分離提純時常用的儀器如圖所示,請回答下列問題:
A.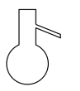 B.
B.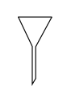 C.
C.![]() D.
D.![]() E.
E.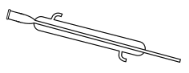
(1)儀器![]() 的名稱分別為____、____。
的名稱分別為____、____。
(2)分離以下混合物應主要選用上述哪種儀器(填字母符號)
a.除去澄清石灰水中懸浮的![]() 顆粒____;
顆粒____;
b.提取食鹽水中的![]() 固體____;
固體____;
c.除去油水中的水:_____。
查看答案和解析>>
科目: 來源: 題型:
【題目】某同學設計了一種電解法制取Fe(OH)2的實驗裝置(如圖),分別用鐵棒和碳棒作電極,通電后,溶液中產生大量的白色沉淀,且較長時間不變色。下列說法中錯誤的是
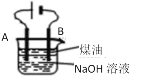
A.NaOH溶液加熱煮沸以除去其中溶解氧
B.A電極用碳棒,B電極用鐵棒
C.B電極發生的反應是:2H2O+2e- = H2↑+ 2OH-
D.電解池中的電解液也可以用NaCl溶液
查看答案和解析>>
科目: 來源: 題型:
【題目】環戊二烯可用于制備二茂鐵(Fe(C5H5)2,結構簡式為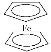 ),后者廣泛應用于航天、化工等領域中。二茂鐵的電化學制備原理如圖所示,其中電解液為溶解有溴化鈉(電解質)和環戊二烯的DMF溶液(DMF為惰性有機溶劑)。下列說法錯誤的是( )
),后者廣泛應用于航天、化工等領域中。二茂鐵的電化學制備原理如圖所示,其中電解液為溶解有溴化鈉(電解質)和環戊二烯的DMF溶液(DMF為惰性有機溶劑)。下列說法錯誤的是( )
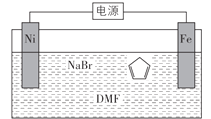
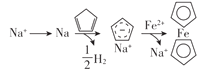
A.制備二茂鐵總反應為:Fe+2![]() =
=![]() +H2↑
+H2↑
B.電解制備需要在無水條件下進行
C.Ni電極與電源負極連接
D.陽極電極反應為:2Br--2e-=Br2
查看答案和解析>>
科目: 來源: 題型:
【題目】某化學興趣小組同學用下圖裝置測定氧化鐵樣品(含![]() 和
和![]() )中
)中![]() 的質量分數,下列說法正確的是( )
的質量分數,下列說法正確的是( )
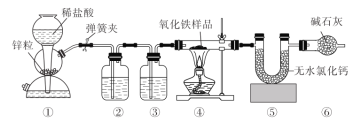
A.實驗室用![]() 和濃鹽酸制備
和濃鹽酸制備![]() 時也可用裝置①
時也可用裝置①
B.實驗開始時先點燃④處酒精燈,再打開彈簧夾
C.裝置⑥的作用是吸收④中生成的水蒸氣
D.裝置②③盛裝的試劑分別為![]() 溶液和濃硫酸
溶液和濃硫酸
查看答案和解析>>
科目: 來源: 題型:
【題目】X、Y、Z、W為原子序數依次增大的四種短周期元素,其中Z為金屬元素,X、W為同一主族元素。X、Z、W形成的最高價氧化物分別為甲、乙、丙。x、y2、z、w分別為X、Y、Z、W的單質,丁是化合物。其轉化關系如圖所示,下列判斷正確的是( )

A.反應①、②屬于氧化還原反應,③屬于非氧化還原反應
B.Y的離子半徑比Z的離子半徑小
C.反應③可以證明X的非金屬性強于W
D.一定條件下,x與甲反應生成丁
查看答案和解析>>
科目: 來源: 題型:
【題目】根據如圖所示的反應判斷,下列說法中錯誤的是
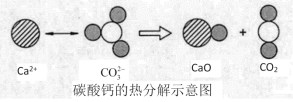
A.該反應的△H大于0
B.CO2(g)和CaO(s)的總能量大于CaCO3(s)的總能量
C.化學鍵斷裂吸收能量,化學鍵形成放出能量
D.由該反應可推知:凡是需要加熱才能發生的反應均為吸熱反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com