
科目: 來源: 題型:
【題目】第二代半導體材料——(Ⅲ-V)A族化合物的特殊性能使之成為科學家的研究熱點之一。
(1) 基態鎵原子的價電子軌道表示式為_____________。
(2) N、P、As位于同一主族,基態氮原子的核外共有________種不同運動狀態的電子,N2O的空間構型為_________,NH4NO3中N的雜化方式為_________________,與PO43-互為等電子體的分子有________________(填一種即可)。
(3)已知NH3分子的鍵角約為107°,而PH3分子的鍵角約為94°,試用價層電子對互斥理論解釋NH3的鍵角比PH¥的鍵角大的原因__________________________。
(4)第三周期主族元素中,按第一電離能大小排序,第一電離能在磷和鋁之間的元素有________________。
(5)氮化硼、氮化鋁、氮化鎵的結構類似于金剛石,熔點如表中所示:
物質 | BN | AIN | GaN |
熔點/℃ | 3000 | 2200 | 1700 |
試從結構的角度分析它們熔點不同的原因_____________________。
(6)磷化鋁晶胞如圖所示,A1原子的配位數為________,若兩個鋁原子之間的最近距離為d pm,NA代表阿伏加德羅常數的值, 則磷化鋁晶體的密度ρ=_________g/cm3。

查看答案和解析>>
科目: 來源: 題型:
【題目】現有金屬單質A、B、C和氣體甲、乙、丙以及物質D、E、F、G、H,它們之間的相互轉化關系如圖所示(圖中有些反應的生成物和反應的條件沒有標出)。
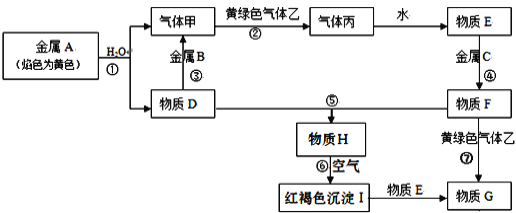
請回答下列問題:
(1)反應③的離子方程式___。
(2)反應⑥化學方程式____。
(3)反應⑦的離子方程式____;物質H在空氣中的現象____。
(4)D溶液中加入B的氧化物固體的離子反應方程式為___,向反應后的溶液中通入過量CO2的離子反應方程式為___。
查看答案和解析>>
科目: 來源: 題型:
【題目】草酸亞鐵晶體(FeC2O4·2H2O,相對分子質量為180)呈淡黃色,可用作照相顯影劑。某實驗小組對其進行了一系列探究。
I.純凈草酸亞鐵晶體熱分解產物的探究。
(1)氣體產物成分的探究。小組成員采用如圖裝置(可重復選用)進行實驗:
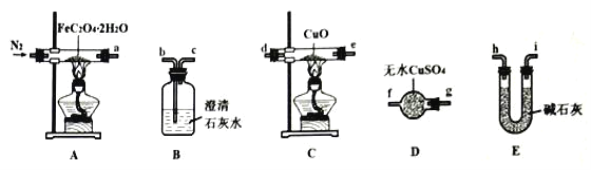
①裝置D的名稱為____。
②按照氣流從左到右的方向,上述裝置的連接順序為____→尾氣處理裝置(填圖中各儀器接口的字母編號)。
③實驗前先通入一段時間N2,其目的為____。
④實驗證明了氣體產物中含有CO,依據的實驗現象為_____。
(2)固體產物成分的探究。充分反應后,A處反應管中殘留黑色固體。小組成員設計實驗證明了其成分只有FeO,其實驗操作及現象為:___。
(3)依據(1)和(2)結論,可知A處反應管中發生反應的化學方程式為:___。
Ⅱ.草酸亞鐵晶體樣品純度的測定
工業制得的草酸亞鐵晶體中常含有FeSO4雜質,測定其純度的步驟如下(雜質不參與反應):
步驟1:稱取2g草酸亞鐵晶體樣品并溶于稀H2SO4中,配成250mL溶液。
步驟2:取上述溶液25.00mL,向其中加入0.01mol·L1KMnO4溶液,恰好完全反應時消耗 KMnO4溶液30mL。
[已知:FeC2O4+KMnO4+H2SO4→Fe2(SO4)3+CO2↑+MnSO4+K2SO4+H2O(未配平)]
(4)草酸亞鐵晶體樣品的純度為____;若步驟1配制溶液時部分Fe2+被氧化,則測定結果將____(填“偏高”、“偏低”或“不變”)。
查看答案和解析>>
科目: 來源: 題型:
【題目】有下列幾組物質,請將序號填入下列空格內:
A.C60和石墨
B.126C和136C
C.冰醋酸和乙酸
D.CH3CHO 與![]()
E.甲烷和十二烷
F.乙醇和乙二醇
①互為同系物的是_________________;
②互為同分異構體的是_____________;
③互為同位素的是________________;
查看答案和解析>>
科目: 來源: 題型:
【題目】實驗室需要480mL1mol·L-1NaOH溶液,根據溶液配制情況回答下列問題:
(1)實驗中除了托盤天平(砝碼)、藥匙、量筒、燒杯、玻璃棒外還需要的其他儀器有___。
(2)如圖是某同學在實驗室配制該NaOH溶液的過程示意圖,其中有錯誤的是___(填操作序號)。
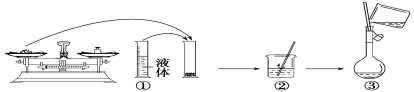
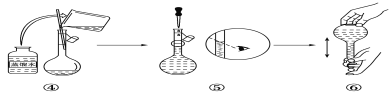
(3)下列操作會導致所配溶液的物質的量濃度偏高的是___。
A.配制NaOH溶液時,NaOH固體中含有Na2O雜質
B.用蒸餾水溶解NaOH固體后,立即轉入容量瓶中定容
C.定容后發現液面高于刻線,可用膠頭滴管將多余的水吸出
D.定容時仰視刻度線
E.用托盤天平稱量 NaOH 固體時,砝碼生銹
F.配制前容量瓶中有少量蒸餾水
(4)若某同學用密度為1.2g/cm3,質量分數為36.5%的濃鹽酸配制100mL3mol/L的稀鹽酸,需要用量筒量取濃鹽酸的體積為___mL。
查看答案和解析>>
科目: 來源: 題型:
【題目】2015年8月12號接近午夜時分,天津濱海新區一處集裝箱碼頭發生爆炸。發生爆炸的是集裝箱內的易燃易爆物品,爆炸火光震天,并產生巨大蘑菇云。根據掌握的信息分析,裝箱區的危險化學品可能有鉀、鈉、氯酸鈉、硝酸鉀、燒堿,硫化堿、硅化鈣、三氯乙烯、氯碘酸等。運抵區的危險化學品可能有環己胺、二甲基二硫、甲酸、硝酸銨、氰化鈉、4,6-二硝基苯-鄰仲丁基苯酚等。
回答下列問題:
(1)在組成NH4NO3、NaCN兩種物質的元素中第一電離能最大的是__________(填元素符號),解釋原因_____________________________________________
(2)二甲基二硫和甲酸中,在水中溶解度較大的是 (填名稱),原因是_______;燒堿所屬的晶體類型為______;硫化堿(Na2S)的S2-的基態電子排布式是____________。
(3)硝酸銨中,NO3-的立體構型為 ,中心原子的雜化軌道類型為__________
(4)1mol化合物NaCN中CN-所含的π鍵數為______,與CN-互為等電子體的分子有 。(CN)2又稱為擬鹵素,實驗室可以用氰化鈉、二氧化錳和濃硫酸在加熱條件下制得,寫成該制備的化學方程式___________。
(5)鈉鉀合金屬于金屬晶體,其某種合金的晶胞結構如圖所示。合金的化學式為____________;晶胞中K 原子的配位數為 ;已知金屬原子半徑r(Na)=186pm、r(K)=227pm,計算晶體的空間利用率 ________(列出計算式,不需要計算出結果)。

查看答案和解析>>
科目: 來源: 題型:
【題目】400K、101.3Kpa時,1.5L某烴蒸氣能在aL氧氣中完全燃燒,體積增大至(a+3)L(相同條件下),若a=8時,該烴可能的分子式( )
A.CH4B.C2H6C.C3H8D.C4H8
查看答案和解析>>
科目: 來源: 題型:
【題目】現有下列十種物質:①HCl;②NaHCO3;③K2SO4溶液;④SiO2;⑤蔗糖晶體;⑥NaOH;⑦氫氧化鐵膠體;⑧NH3·H2O;⑨空氣;⑩Al2(SO4)3
(1)上述物質中屬于電解質的有____(填序號),向⑦中逐滴滴入過量的①的水溶液,出現的實驗現象是___。
(2)用④與⑥焙燒制備硅酸鈉,可采用圖中的裝置為____(填選項編號)。
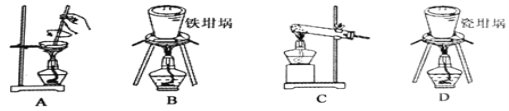
查看答案和解析>>
科目: 來源: 題型:
【題目】某有機物的結構簡式如圖所示,關于該有機物的說法不正確的是
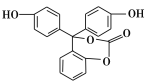
A.該有機物的化學式為C20H14O5
B.該有機物可發生加成、取代、氧化、消去等反應
C.該有機物分子中的三個苯環不可能共平面
D.1 mol該有機物與足量NaOH溶液充分反應,消耗NaOH的物質的量為5 mol
查看答案和解析>>
科目: 來源: 題型:
【題目】某無色溶液100mL,其中可能含Fe3+、Al3+、Na+、Mg2+、Cu2+、NH4+、K+、CO32-、SO42-等離子中的幾種,為分析其成分,取此溶液分別進行了四個實驗,其操作和有關現象如圖所示。
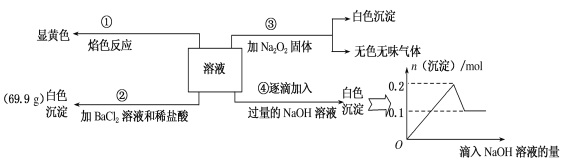
請回答下列問題:
(1)焰色反應是___(填“物理”或“化學”)變化;實驗③中產生的無色無味氣體是___(填化學式)。
(2)原溶液中一定存在的離子有___,一定不存在的離子有____。
(3)若溶液中K+物質的量為0.04mol,則c(Na+)=___mol/L。
(4)將一定量Fe2O3和Al2O3混合物溶于100mL稀硫酸中,向反應后的溶液中緩慢加入NaOH溶液,加入NaOH溶液的體積與生成沉淀的質量關系如圖所示,試回答:
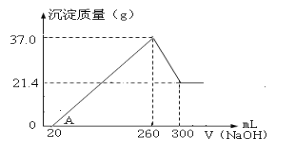
①混合物中含Fe2O3的質量為___g;
②所用硫酸溶液物質的量濃度為___mol/L。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com