
科目: 來源: 題型:
【題目】一瓶無色澄清的溶液,其中可能含有H+、![]() 、Na+、Al3+、Fe3+、I-、
、Na+、Al3+、Fe3+、I-、![]() 、
、![]() 、
、![]() 、
、![]() 。取該溶液進行以下實驗:
。取該溶液進行以下實驗:
①用pH試紙檢驗,溶液呈強酸性 ②取溶液適量,加入少量CCl4和數滴新制氯水,振蕩,CCl4層呈紫紅色 ③該溶液的焰色反應沒有黃色;根據以上實驗結果,下列推斷正確的是( )
A.向該溶液中加入BaCl2不一定能觀察到白色沉淀
B.可以確定沒有Na+、Fe3+、![]() 、
、![]() ,不能確定是否有
,不能確定是否有![]()
C.該溶液可能是NH4NO3與HI的混合
D.一定沒有Al3+、![]() 和
和![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】某企業以輝銅礦為原料生產堿式碳酸銅,工藝流程如下所示:
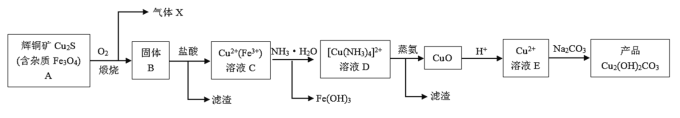
已知:Cu(OH)2溶于氨水形成[Cu(NH3)4]2+
根據以上工藝流程,下列說法不正確的是( )
A.為實現溶液C到溶液D的轉化,加入過量的NH3H2O后過濾即可
B.溶液E和碳酸鈉混合方式不同對產品的成分沒有影響
C.在制備產品時,溶液D中不直接加入Na2CO3溶液的原因可能是游離的Cu2+濃度太低
D.蒸氨過程發生總反應的化學方程式為:
查看答案和解析>>
科目: 來源: 題型:
【題目】紅礬鈉(重鉻酸鈉:![]() )是重要的基本化工原料,應用十分廣泛。工業制備紅礬鈉的流程如下:
)是重要的基本化工原料,應用十分廣泛。工業制備紅礬鈉的流程如下:
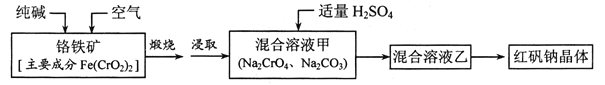
請回答下列問題:
(1)![]() 的基態電子排布式為____________。
的基態電子排布式為____________。
(2)鍛燒鉻鐵礦發生反應:____________Fe(CrO2)2+Na2CO3+O2![]() Fe2O3+Na2CrO4+CO2 配平上述化學反應方程式。
Fe2O3+Na2CrO4+CO2 配平上述化學反應方程式。
(3)溶液甲中加入H2SO4時,可以觀察到溶液由黃色變為橙色,并放出無色氣體,有關反應的離子方程式為____________。
(4)制備紅礬鈉的廢水必須進行處理。首先酸化廢水,將含+6價鉻的酸性廢液放入電解槽內,用鐵作陽極進行電解,陰極析出H2,陽極產物被![]() 氧化然后轉化為Cr(OH)3、 Fe(0H)3 沉淀。
氧化然后轉化為Cr(OH)3、 Fe(0H)3 沉淀。
①陽極的電極反應式為(不考慮后續反應):____________。
②溶液中金屬離子在陰極區可沉淀完全,從水的電離平衡角度解釋其原因:______。
③已知某含![]() 的酸性廢水中Cr元素的含量是52.5mg/L,處理后Cr元素最高允許 排量為0.5 mg/L。要處理100 m3廢水達到排放標準,至少消耗鐵_____kg。
的酸性廢水中Cr元素的含量是52.5mg/L,處理后Cr元素最高允許 排量為0.5 mg/L。要處理100 m3廢水達到排放標準,至少消耗鐵_____kg。
查看答案和解析>>
科目: 來源: 題型:
【題目】下列判斷中一定正確的是( )
A. NaCl及Na2O2固體中陰、陽離子數之比均為1:1
B. 等質量的O2與O3中,氧原子的個數比為3:2
C. 分別用H2O2、KMnO4分解制O2,當制得等質量O2時,轉移電子數之比為1:2
D. 10 mL 0.3 mol·L-1 NaCl溶液與30 mL 0.1 mol·L-1 AlCl3溶液中Cl -物質的量濃度比為1:3
查看答案和解析>>
科目: 來源: 題型:
【題目】25℃時,相同體積和pH的NaX、NaY、NaZ三種鹽溶液,分別加水稀釋,溶液pH的變化與所加水的體積關系如下圖所示。下列說法正確是( )

A.由圖可知三種酸的酸性為:HX<HY<HZ
B.在等物質的量濃度的NaX和HX混合溶液中存在:c(H+)-c(OH-)=c(X-)-c(HX)
C.濃度均為0.1mol/L的NaX、NaY、NaZ的混合溶液中:![]()
D.在pH相等NaX和NaY的溶液中存在:c(HX)+c(X-)=c(HY)+c(Y-)
查看答案和解析>>
科目: 來源: 題型:
【題目】銅是重要金屬,Cu及其化合物在科學研究和工業生產中具有許多用途。請回答以下問題:
(1)CuSO4可由金屬銅與稀硫酸并通入氧氣反應制備,該反應的化學方程式為_______;
(2)無水CuSO4粉末常用來檢驗一些有機物中的微量水分,現象是________________;
(3)![]() 的立體構型是________,其中S原子的雜化軌道類型是_______;
的立體構型是________,其中S原子的雜化軌道類型是_______;
(4)元素金(Au)處于周期表中的第六周期,與Cu同族,Au原子最外層電子排布式為______;一種銅合金晶體具有面心立方最密堆積的結構,在晶胞中Cu原子處于面心,Au原子處于頂點位置,該合金中每一層均為__________(填“密置層”、“非密置層”),金原子的配位數為__________;該晶體中,原子之間的作用力是________;
(5)上述晶體具有儲氫功能,氫原子可進入到由Cu原子與Au原子構成的四面體空隙中。若將Cu原子與Au原子等同看待,該晶體儲氫后的晶胞結構與CaF2的晶胞結構結構相似,該晶體儲氫后的化學式應為___________。若Cu原子與Au原子的距離為a cm,則該晶體儲氫后的密度為_________。(含a的表達式)
查看答案和解析>>
科目: 來源: 題型:
【題目】X、Y、Z、W是四種短周期元素,X原子M層上的電子數是原子核外電子層數的2倍;Y原子最外層電子數是次外層電子數的2倍;Z元素的單質為雙原子分子,Z的氫化物水溶液呈堿性;W元素最高正價是+7價。回答下列問題:
(1)元素X原子結構示意圖為________。
(2)元素Y的最高價氧化物的結構式為__________,其中一種同位素可測定文物年代,這種同位素的符號是________。
(3)元素Z能與氫元素形成-1價陰離子為_________,該陰離子的電子總數是________。
(4)元素W的單質與元素X的低價氧化物在水溶液中反應的離子方程式為___________。
(5)ZW3常溫下呈液態,可與水反應生成一種具有漂白性的酸和一種堿性氣體,反應的化學方程式為_______。
(6)探尋物質的性質差異性是學習的重要方法之一。X、Y、Z、W四種元素的最高價氧化物的水化物中化學性質明顯不同于其他三種酸的是_______(用酸的分子式表示)。
查看答案和解析>>
科目: 來源: 題型:
【題目】下表是元素周期表中的一部分。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | A | |||||||
2 | E | F | H | J | ||||
3 | B | C | D | G | I |
根據A~J在周期表中的位置,用元素符號或化學式回答下列問題:
(1)化學性質最不活潑的元素是________,氧化性最強的單質是________,還原性最強的單質是________。
(2)最高價氧化物對應的水化物中,堿性最強的是________,酸性最強的是________,呈兩性的是________。
(3)A分別與E、F、G、H、I形成的簡單氣態化合物中,最穩定的是________。
(4)在B、C、D、G、I中,原子半徑最大的是________。
(5)元素C與I形成的化合物的電子式是________。
查看答案和解析>>
科目: 來源: 題型:
【題目】瘦肉精是一種廉價藥品,學名鹽酸克倫特羅,它有減少脂肪增加瘦肉的效果,但也存在副作用,輕則導致心律不齊,重則導致心臟病。已知其結構簡式如下圖,下列有關說法正確的是( )

A.該有機物中有8種不同化學環境的氫原子
B.該有機物不能繼續和鹽酸反應
C.1mol該有機物在一定條件下最多可以消耗3molNaOH
D.該有機物能發生加成反應、消去反應、取代反應、氧化反應和酯化反應
查看答案和解析>>
科目: 來源: 題型:
【題目】A、B、C、D、E五種短周期主族元素,原子序數依次增大,其中C、D、E同周期,A、C同主族,B、E同主族,B元素的原子最外層電子數是次外層電子數的三倍,又知A單質是密度最小的氣體。
請回答下列問題:
(1)元素C在周期表中的位置______________________________。
(2)A、C、E以原子個數比1∶1∶1形成化合物X,其電子式為_________________。
(3)B、E對應簡單氫化物穩定性的大小順序是(用分子式表示) ________________。
(4)若D是非金屬元素,其單質在電子工業中有重要應用,請寫出其氧化物溶于強堿溶液的離子方程式:___________________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com