
科目: 來源: 題型:
【題目】常溫下,向25 mL 0.1 mol·L-1NaOH溶液中逐滴滴加0.2 mol·L-1的HN3(疊氮酸)溶液,pH的變化曲線如圖所示(溶液混合時體積的變化忽略不計,疊氮酸的Ka=10-4.7)。下列說法正確的是
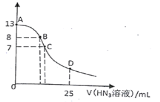
A. 0.1 mol·L-1 NaN3溶液pH約為8.85
B. 在B點,離子濃度大小為c(OH-)>c(H+)>c (Na+)>c(N3-)
C. 在C點,滴加的V(HN3)<12.5 mL
D. 在D點,c(Na+)=2c(HN3)+2 c(N3-)
查看答案和解析>>
科目: 來源: 題型:
【題目】要“打贏藍天保衛戰”,意味著對污染防治比過去要求更高。某種利用垃圾滲透液實現發電、環保二位一體相結合的裝置示意圖如圖,當該裝置工作時,下列說法正確的是( )
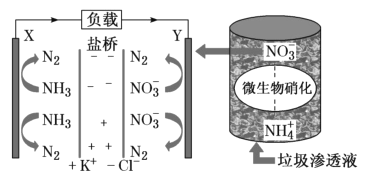
A.鹽橋中K+向X極移動
B.電路中流過7.5mol電子時,共產生標準狀況下N2的體積為44.8L
C.該裝置實現了將電能轉化為化學能
D.Y極發生的反應為2NO3--10e-+6H2O=N2↑+12OH-,周圍pH增大
查看答案和解析>>
科目: 來源: 題型:
【題目】最近,中國科學院大連化物所“CO2催化轉化為CO的研究”獲得新進展。如圖是使用不同催化劑(NiPc和CoPc)時轉化過程中的能量變化,下列說法不合理的是( )
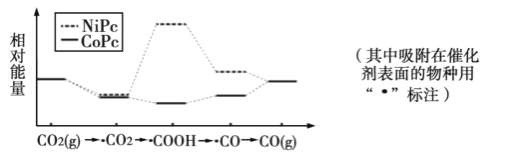
A.CO2經還原反應得到COOH
B.該研究成果將有利于緩解溫室效應,并解決能源轉化問題
C.相同基團的物種分別吸附在NiPc和CoPc表面,其能量可能不同
D.催化劑可以改變CO2轉化為CO反應的焓變
查看答案和解析>>
科目: 來源: 題型:
【題目】某小組同學用圖所示裝置制取氨,并探究其性質。
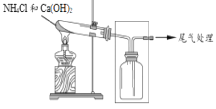
(1)制取氨氣的化學方程式是______。
(2)采用圖示的方法收集氨氣,是因為氨氣的密度比空氣 ______(填“大”或“小”)。
(3)將蘸有濃鹽酸的棉球放在玻璃片上,用集滿NH3的集氣瓶扣住棉球,可觀察到的現象是______。
(4)甲同學設計了下圖所示的裝置進行尾氣處理,乙同學認為該設計不合理,請畫出正確的尾氣吸收圖______。
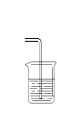
查看答案和解析>>
科目: 來源: 題型:
【題目】化合物M(![]() )、N(
)、N(![]() )、P(
)、P(![]() )都是重要的有機物。下列有關M、N、P的說法正確的是( )
)都是重要的有機物。下列有關M、N、P的說法正確的是( )
A.M與HBr發生加成反應的產物只有一種
B.P中所有碳原子一定共平面
C.M、N、P互為同分異構體
D.M能使酸性高錳酸鉀溶液褪色
查看答案和解析>>
科目: 來源: 題型:
【題目】氮化鋇(Ba3N2)是一種重要的化學試劑。高溫下,向氫化鋇(BaH2)中通入氮氣反應生成氮化鋇。可用如圖裝置制備氮化鋇。已知:Ba3N2遇水反應;BaH2在潮濕空氣中能自燃,遇水反應。下列說法不正確的是( )
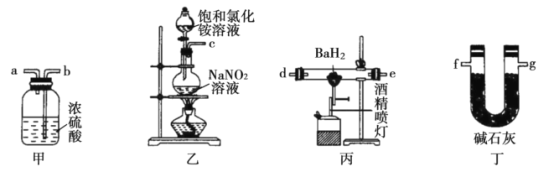
A.在實驗室中可以用裝置乙制備氯氣
B.實驗時,先點燃裝置丙中的酒精噴燈,后點燃裝置乙中的酒精燈
C.氣流從左向右的字母連接順序為c→b→a→d→e→g→f
D.裝置甲中的濃硫酸和裝置丁中的堿石灰作用相同,均可防止水蒸氣進入裝置丙中
查看答案和解析>>
科目: 來源: 題型:
【題目】物質中的化學能在一定條件下可轉化為電能。
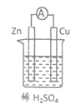
(1)將鋅片放入盛有稀硫酸的燒杯中,反應的離子方程式是_______。
(2)將鋅片、銅片按照圖所示裝置連接,能證明化學能轉化為電能的實驗現象是:銅片上有氣泡產生、_______。
(3)稀硫酸在圖所示裝置中的作用是:傳導離子、_______。
(4)下列反應通過原電池裝置,可實現化學能直接轉化為電能的是_______(填序號)。
① 2H2 + O2 =2 H2O
② SO3+ H2O = H2SO4
③ Cu + 2Fe3+ =Cu2++ 2Fe2+
查看答案和解析>>
科目: 來源: 題型:
【題目】鎘鎳可充電電池的充、放電反應按下式進行:Cd+2NiO(OH)+2H2O![]() Cd(OH)2+2Ni(OH)2,由此判斷,下列說法錯誤的是
Cd(OH)2+2Ni(OH)2,由此判斷,下列說法錯誤的是
A. 放電時,NiO(OH)作正極
B. 放電時,Cd發生還原反應
C. 電解質溶液為堿性溶液
D. 充電時,陽極反應為Ni(OH)2+OH--e-== NiO(OH)+H2O
查看答案和解析>>
科目: 來源: 題型:
【題目】研究煤的合理利用及 CO2的綜合應用有著重要的意義。請回答以下問題:
I.煤的氣化
已知煤的氣化過程涉及的基本化學反應有:
①C(s)+H2O(g) ![]() CO(g)+H2(g) △H=+131kJ·mol-1
CO(g)+H2(g) △H=+131kJ·mol-1
②CO(g)+3H2(g) ![]() CH4(g) +H2O(g) △H=akJ·mol-1
CH4(g) +H2O(g) △H=akJ·mol-1
查閱資料反應②中相關化學鍵能數據如下表:
化學鍵 | C≡O | H—H | H—C | H—O |
E(kJ·mol-1) | 1072 | 436 | 414 | 465 |
(1)則反應②中 a =_____________。
(2)煤直接甲烷化反應 C(s) + 2 H2 (g) ![]() CH4(g) 的△H=為 _____kJ mol-1, 該反應在_____________(填“高溫”或“低溫 ”)下自發進行。
CH4(g) 的△H=為 _____kJ mol-1, 該反應在_____________(填“高溫”或“低溫 ”)下自發進行。
II.合成低碳烯烴
在體積為1 L 的 密閉容器中,充入 1mol CO2和 2 .5 mol H2, 發生 反應: 2CO2 ( g) + 6 H2(g)![]() C2H4(g)+4 H2O(g) △H=-128kJ·mol-1,測得溫度對催化劑催化效率和CO2 平衡轉化率的影響如右圖 所 示 :
C2H4(g)+4 H2O(g) △H=-128kJ·mol-1,測得溫度對催化劑催化效率和CO2 平衡轉化率的影響如右圖 所 示 :
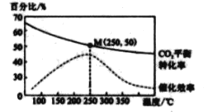
(3) 圖中低溫時, 隨著溫度升高催化劑的催化效率提高, 但 CO2的平衡轉化率卻反而降低 ,其原因是_______________.
(4) 250℃時,該反應的平衡常數K 值為____________。
III.合成甲醇
在恒溫 2 L 容積不變的密閉容器中,充入 1molCO2 和 3 molH2, 發生反應:. CO2(g)+3H2(g) ![]() CH3OH(g)+ H2O(g),測得不同時刻反應前后容器內壓強變化(p后/p前)如下表:
CH3OH(g)+ H2O(g),測得不同時刻反應前后容器內壓強變化(p后/p前)如下表:
時間/h | 1 | 2 | 3 | 4 | 5 | 6 |
p后/p前 | 0.90 | 0.85 | 0.82 | 0.81 | 0.80 | 0.80 |
(5) 反應前 1 小時內的平均反應速率 v(H2)為_______molL-1h-1 , 該溫度下CO2的平衡轉化率為_____________。
查看答案和解析>>
科目: 來源: 題型:
【題目】通過傳感器可以監測空氣中甲醛的含量。一種燃料電池型甲醛氣體傳感器的原理如圖所示,下列說法錯誤的是

A. a為電池的正極,發生還原反應
B. b極的電極反應為HCHO+H2O-4e-==CO2+4H+
C. 傳感器工作過程中,電解質溶液中硫酸的濃度減小
D. 當電路中轉移2×10-4 mol電子時,傳感器內參加反應的HCHO為3.0 mg
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com