
科目: 來源: 題型:
【題目】2005年法拉利公司發布的敞篷車(法拉利Superamerica),其玻璃車頂采用了先進的電致變色技術,即在原來玻璃材料基礎上增加了有電致變色系統組成的五層膜材料(如圖所示)。其工作原理是:在外接電源(外加電場)下,通過在膜材料內部發生氧化還原反應,實現對器件的光透過率進行多級可逆性調節。下列有關說法中不正確的是( )
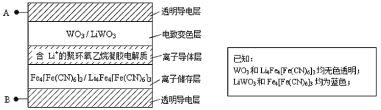
A.當A外接電源正極時,Li+脫離離子儲存層
B.當A外接電源負極時,電致變色層發生反應為:WO3+Li++e-=LiWO3
C.當B外接電源正極時,膜的透過率降低,可以有效阻擋陽光
D.該電致變色系統在較長時間的使用過程中,離子導體層中Li+的量可保持基本不變
查看答案和解析>>
科目: 來源: 題型:
【題目】[選修3——物質結構與性質] 元素X位于第四周期,其基態原子的內層軌道全部排滿電子,且最外層電子數為2。元素Y基態原子的3p軌道上有4個電子。元素Z的原子最外層電子數是其內層的3倍。
(1)在Y的最高價氧化物分子中,Y原子軌道的雜化類型是_______________。
(2)Z的氫化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是_______________________;Z的氫化物在固態時的密度比在液態時還小,其原因是_________
(3)Y與Z可形成YZ42-。
①YZ42-的空間構型為________________(用文字描述)。
②寫出一種與YZ42-互為等電子體的分子的化學式:_________________。
(4)X的氯化物與氨水反應可形成配合物[X(NH3)4]Cl2,1 mol該配合物中含有σ鍵的
數目為_______。
(5)X與Y所形成化合物晶體的晶胞如圖所:
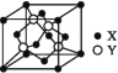
①在該晶體中,X離子的配位數為__________,與Y距離最近且距離相等的Y原子的數目為________。
②該晶胞的邊長為a cm,該晶體的密度為__________________ g·cm-3。
查看答案和解析>>
科目: 來源: 題型:
【題目】X、Y、Z三種短周期元素在周期表中的位置如圖所示。若X的最高正價與負價的代數和為2,則下列說法不正確是( )
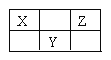
A.最簡單氣態氫化物穩定性Z>X
B.Z無氧酸溶液能在玻璃容器上刻標記
C.X的氫化物可用作制冷劑
D.原子半徑由大到小為Y>Z>X
查看答案和解析>>
科目: 來源: 題型:
【題目】NA表示阿伏加德羅常數,則下列說法不正確的是( )
A.常溫常壓下,18g18O2所含的質子數為8NA
B.1mol氫氧根離子中含有的電子數為NA
C.氫氧燃料電池中轉移1mol電子消耗0.5molH2
D.鈉在空氣中燃燒可生成多種氧化物,23g鈉充分燃燒時轉移電子數為NA
查看答案和解析>>
科目: 來源: 題型:
【題目】下列說法中正確的是( )
A.向0.1molL-1的氨水中加入少量硫酸銨固體,溶液中![]() 增大
增大
B.廚房小實驗:將雞蛋殼浸泡在食醋中,有氣泡產生,說明CH3COOH是弱電解質
C.有甲、乙兩種醋酸溶液,測得甲的pH=a、乙的pH=a+1,若用于中和等物質的量濃度等體積的NaOH溶液,需消耗甲、乙兩酸的體積V(乙)>10V(甲)
D.體積相同、濃度均為0.1molL-1的NaOH溶液、氨水,分別稀釋m、n倍,使溶液的pH都變為9,則m<n
查看答案和解析>>
科目: 來源: 題型:
【題目】利用有機物X在一定條件下可合成植物生長所需的“平衡因子”Y(部分產物未寫出)。已知含有“手性碳原子”的分子可形成對映異構體。下列有關說法中正確的是( )
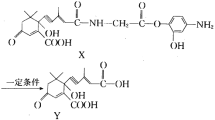
A.X,Y分子都不存在對映異構體
B.X分子中所有碳原子可能都在同一平面
C.Y分子可以發生取代、酯化、消去、加成、氧化等反應
D.未寫出的產物可能有2種,且都具有兩性化合物的特性
查看答案和解析>>
科目: 來源: 題型:
【題目】已知五種元素的原子序數大小順序為C>A>B>D>E,A、C同周期,B、C同主族。A與B形成的離子化合物A2B中所有離子的電子數相等,其電子總數為30;D和E可形成4核10個電子的分子。
試回答下列問題:
(1)寫出這五種元素的名稱:A___,B____,C___,D__,E___。
(2)用電子式表示離子化合物A2B的形成過程___。
(3)按要求表示下列化合物的原子構成關系:
①D元素形成單質的電子式___;
②E與B形成化合物的電子式___;
③A、B、E形成化合物的電子式___;
④D與E兩元素按原子數目比為1∶3和2∶4構成分子M和N,M的電子式___,N的結構式___。
查看答案和解析>>
科目: 來源: 題型:
【題目】甲醇是一種可再生能源,具有開發和應用的廣闊前景,研究甲醇具有重要意義。有人模擬用CO和H2合成甲醇,其反應為:CO(g) + 2H2(g) CH3OH(g) △H<0
(1)在容積固定為1L的密閉容器內充入2 mol CO和4 mol H2發生上述反應,20min時用壓力計監測容器內壓強的變化如下:
反應時間/min | 0 | 5 | 10 | 15 | 20 | 25 |
壓強/MPa | 12.4 | 10.2 | 8.4 | 7.0 | 6.2 | 6.2 |
則反應從開始到20min時,以CO濃度變化表示的平均反應速率v(CO)=_________mol/(L·min),該溫度下平衡常數K=___________,若平衡后增大壓強,則K值_________(填“增大”、“減小”或“不變”)。
(2)在恒溫恒容的密閉容器中,不能判定CO(g)+2H2(g) CH3OH(g) △H<0,反應達到平衡的是___________;
A、壓強保持不變 B、氣體的密度保持不變
C、氣體平均摩爾質量保持不變 D、速率v(H2):v(CH3OH)=2:1
(3)如圖是甲醇燃料電池結構示意圖,C是________(填“正”或“負”)極,寫出此電極的電極反應式__________________________________________。

(4)若以該電池為電源,用石墨做電極電解100mL CuSO4溶液,電解一段時間后,兩極均收集到11.2L的氣體(標準狀況下),則原CuSO4溶液的物質的量濃度為________mol/L。
查看答案和解析>>
科目: 來源: 題型:
【題目】非金屬單質A經如圖所示的過程轉化為含氧酸D,已知D為強酸,請回答下列問題:
A![]() B
B![]() C
C![]() D
D
(1)若A在常溫下為固體,B是能使品紅溶液褪色的有刺激性氣味的無色氣體。
①D的化學式是___。
②在工業生產中B氣體的大量排放被雨水吸收后形成了___而污染了環境。
(2)若A在常溫下為無色無味氣體,C是紅棕色的氣體
①A、C的化學式分別是:A___;C___。
②D的濃溶液在常溫下可與銅反應并生成C氣體,請寫出該反應的化學方程式:___。該反應___(填“屬于”或“不屬于”)氧化還原反應。
查看答案和解析>>
科目: 來源: 題型:
【題目】下列對化學用語的理解中正確的是( )
A.原子結構示意圖:![]() 可以表示35Cl,也可以表示37Cl
可以表示35Cl,也可以表示37Cl
B.電子式:![]() 可以表示羥基,也可以表示氫氧根離子
可以表示羥基,也可以表示氫氧根離子
C.比例模型![]() :可以表示甲烷分子,也可以表示四氯化碳分子
:可以表示甲烷分子,也可以表示四氯化碳分子
D.結構簡式(CH3)2CHOH:可以表示1-丙醇,也可以表示2-丙醇
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com