
科目: 來源: 題型:
【題目】實驗室用下圖所示裝置制備AlC13溶液,并用AlC13溶液溶解一定量的CaCO3形成溶液,再用氨水沉淀,然后鍛燒沉淀制備新型的超導材料和發光材料七鋁十二鈣 (12CaO·7Al2O3)。已知A1C13易水解,易升華。
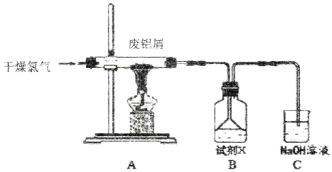
(1)①實驗室用氯酸鉀和濃鹽酸制備氯氣,其離子方程式為____________;
②C裝置的作用____________;
(2)氯氣與廢鋁屑反應生成的AlC13蒸氣溶解在B中,B中盛放的試劑X是____________;為了防止AlC13蒸氣凝華堵塞導管,實驗中可采取的措施是____________(寫出一點)。
(3)B裝置中的AlC13溶液溶解CaCO3時,AlC13溶液和碳酸鈣粉末的混合方式為____________;
(4)實驗要控制碳酸鈣和AlC13的量,要求n(CaCO3): n(A1C13)> 12:14,其原因是____________;
(5)以工業碳酸鈣(含有少量A12O3、Fe2O3雜質)生產二水合氯化鈣(CaC12·2H2O)的方法為:將工業碳酸鈣溶于鹽酸,____________。
已知:幾種離子生成氫氧化物沉淀pH(開始沉淀的pH按金屬離子濃度為1.0mol/L計算)

(實驗中需用到的試劑和儀器有:鹽酸,氫氧化鈣,冰水,pH計)。
查看答案和解析>>
科目: 來源: 題型:
【題目】

①用量筒量取50 mL 0.25 mol/L硫酸倒入小燒杯中,測出硫酸溫度;
②用另一量筒量取50 mL 0.55 mol/L NaOH溶液,并用另一溫度計測出其溫度;
③將NaOH溶液倒入小燒杯中,設法使之混合均勻,測出混合液最高溫度。
回答下列問題:
(1)寫出稀硫酸和稀氫氧化鈉溶液反應表示中和熱的熱化學方程式(中和熱數值為57.3 kJ/mol):_____。
(2)倒入NaOH溶液的正確操作是________(從下列選出)。
A.沿玻璃棒緩慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)使硫酸與NaOH溶液混合均勻的正確操作是________(從下列選出)。
A.用溫度計小心攪拌 B.揭開硬紙片用玻璃棒攪拌
C.輕輕地振蕩燒杯 D.用套在溫度計上的環形玻璃棒輕輕地攪動
(4)若用50mL0.55mol/LHCl與50 mL 0.55 mol/L NaOH溶液反應測定中和熱,則測出的中和熱,
(填偏大 偏小 不變)
查看答案和解析>>
科目: 來源: 題型:
【題目】【物質結構與性質】純銅在工業上主要用來制造導線、電器元件等,銅能形成多種-1和+2價態的化合物且其化合物常帶有顏色。
(1)寫出基態Cu+的核外電子排布式____________;
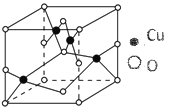
(2)如圖結構是銅的某氧化物的晶體結構的最小重復單元,則該氧化物的化學式為____________;
(3)向硫酸銅溶液中滴加氨水會生成藍色沉淀,在滴加氨水至沉淀剛好全部溶解時可得到藍色溶液,繼續向其中加入極性較小的乙醇可以生成深藍色的[Cu(NH3)4]SO4H2O沉淀。
①該沉淀中S原子的雜化類型為____________;
②寫出一種與NH3分子互為等電子體的陽離子的化學式____________。
(4)NH3的沸點高于PH3,原因是____________
(5)CuO的熔點比CuCl的熔點____________(填“高”或“低”),其原因是____________。
查看答案和解析>>
科目: 來源: 題型:
【題目】在一密閉容器中充入NO2,在一定條件下進行反應:2NO2![]() 2NO+O2。達到平衡狀態的標志是
2NO+O2。達到平衡狀態的標志是
A.NO2的消耗速率與NO的生成速率相等
B.容器內NO2的物質的量與NO的物質的量相等
C.NO2和O2的消耗速率之比為2∶1
D.單位時間內生成2n mol NO。同時生成n mol O2
查看答案和解析>>
科目: 來源: 題型:
【題目】(1)有下列幾種物質
A.金剛石和石墨
B.C2H6和C5H12
C.C2H4和C2H6
D.CH3CH2CH2CH3和CH3CH(CH3)2
E.35Cl和37Cl
屬于同分異構體的是________;屬于同素異形體的是________;屬于同系物的是________;屬于同位素的是________。
(2)請寫出下列反應的化學方程式,并判斷其反應類型。
①由甲烷制取CH3Cl:____________________________,屬于________反應。
②由苯制取溴苯:________________________________,屬于________反應。
③由乙烯制取一氯乙烷____________________________,屬于________反應。
④由CH2=CH-Cl制取聚氯乙烯: 屬于________反應。
(3)寫出結構中含有四個甲基的己烷的結構簡式: :寫出丙烯(CH2=CH-CH3)與HCl一定條件下加成的產物的結構簡式: ;寫出異丁烷的一氯取代物的結構簡式: 。
查看答案和解析>>
科目: 來源: 題型:
【題目】D、E為中學化學常見的金屬單質且D常呈紅棕色,F是一種黑色晶體。E與C的濃溶液在常溫作用呈鈍化現象,加熱時則有大量無色氣體產生,同時生成H。在一定條件下C、D間能發生反應。各物質轉化關系如下圖:

(1)已知1g E在B中燃燒放出的熱量為Q kJ,試寫出表示E燃燒熱的熱化學方程式____。
(2)檢驗H和G的混合溶液中含有G的陽離子的試劑可以是:_____________。
A.氯水和KSCN溶液 B.氫氧化鈉溶液 C.酸性KMnO4溶液
(3)用惰性電極電解一定濃度的A的水溶液,陽極反應式為_____________________,通電一段時間后,向所得溶液中加入8.0g D的氧化物后恰好恢復到電解前的濃度,則電解過程中收集到標準狀況下的氣體體積為多少升?
查看答案和解析>>
科目: 來源: 題型:
【題目】乙二醛(OHC-CHO)是一種重要的精細化工產品。
Ⅰ.工業生產乙二醛
(1)乙醛(CH3CHO)液相硝酸氧化法
在Cu(NO3)2催化下,用稀硝酸氧化乙醛制取乙二醛,反應的化學方程式為 。該法具有原料易得、反應條件溫和等優點,但也存在比較明顯的缺點是 。
(2)乙二醇(HOCH2CH2OH)氣相氧化法
① 已知:OHC-CHO(g)+2H2(g)![]() HOCH2CH2OH(g) ΔH=-78 kJ·mol-1 K1
HOCH2CH2OH(g) ΔH=-78 kJ·mol-1 K1
2H2(g)+O2(g)![]() 2H2O(g) ΔH=-484 kJ·mol-1 K2
2H2O(g) ΔH=-484 kJ·mol-1 K2
乙二醇氣相氧化反應HOCH2CH2OH(g)+O2(g)![]() OHC—CHO(g)+2H2O(g)的ΔH= kJ·mol-1。相同溫度下,該反應的化學平衡常數K= (用含K1、K2的代數式表示)。
OHC—CHO(g)+2H2O(g)的ΔH= kJ·mol-1。相同溫度下,該反應的化學平衡常數K= (用含K1、K2的代數式表示)。

② 當原料氣中氧醇比為1.35時,乙二醛和副產物CO2的產率與反應溫度的關系如下圖所示。反應溫度在450~495℃之間和超過495℃時,乙二醛產率降低的主要原因分別是 、
Ⅱ.乙二醛電解氧化制備乙醛酸(OHC—COOH)的生產裝置如下圖所示,通電后,陽極產生的Cl2 與乙二醛溶液反應生成乙醛酸。

(3)陰極電極式為
(4)陽極液中鹽酸的作用,除了產生氯氣外,還有
(5)保持電流強度為a A,電解t min,制得乙醛酸m g,列式表示該裝置在本次電解中的電流效率η=
(設:法拉第常數為f C·mol-1;η=![]() )
)
查看答案和解析>>
科目: 來源: 題型:
【題目】在一定溫度下,固定體積的密閉容器內,反應2HI(g)![]() H2 (g)+ I2 (g)達到平衡狀態的標志是:
H2 (g)+ I2 (g)達到平衡狀態的標志是:
①I2的體積分數不再變化;
②生成1 mol H2同時消耗1 molI2;
③容器內壓強不再變化;
④生成2 mol HI同時消耗1molH2;
⑤氣體的密度不再變化;
⑥混合氣體的平均分子質量不再變化
A.①②③④⑤⑥ B.①②③⑤⑥ C.①②⑤⑥ D.①②
查看答案和解析>>
科目: 來源: 題型:
【題目】已知:2NO2(g)![]() N2O4(g) △ H<0。在恒溫恒容條件下,將一定量NO2和N2O4的混合氣體通入容積為2L的密閉容器中,反應過程中各物質的物質的量濃度c隨時間t的變化關系如下圖所示。
N2O4(g) △ H<0。在恒溫恒容條件下,將一定量NO2和N2O4的混合氣體通入容積為2L的密閉容器中,反應過程中各物質的物質的量濃度c隨時間t的變化關系如下圖所示。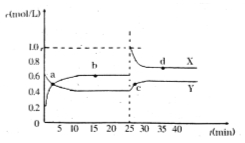
(1)a、b、c、d四個點中,化學反應處于平衡狀態的是 點。
(2)b點平衡常數的表達式為 。
(3)b、d兩點所表示的反應體系中,氣體顏色由深的是 (填字母)。
查看答案和解析>>
科目: 來源: 題型:
【題目】化學反應原理研究氮、氧等單質及其化合物的反應有重要意義。
(1)合成氨反應N2(g)+3H2(g)![]() 2NH3(g),若在恒溫、恒壓條件下向平衡體系中通入氬氣,平衡 移動(填“向左”、“向右”、或“不”)。
2NH3(g),若在恒溫、恒壓條件下向平衡體系中通入氬氣,平衡 移動(填“向左”、“向右”、或“不”)。
(2)O2 (g)=O+2(g)+e- ![]() H1=+ 1175.7 kJ·mol-1
H1=+ 1175.7 kJ·mol-1
PtF6(g)+ e- ![]() PtF6-(g)
PtF6-(g) ![]() H2= - 771.1 kJ·mol-1
H2= - 771.1 kJ·mol-1
O2+PtF6-(s)=O2+(g)+PtF6- ![]() H3=+482.2 kJ·mol-1
H3=+482.2 kJ·mol-1
則反應O2(g)+ PtF6 (g)=O2++PtF6- (s)的![]() H=_____________ kJ·mol-1。
H=_____________ kJ·mol-1。
(3)在25℃下,向濃度均為0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成___沉淀(填化學式),生成該沉淀的離子方程式為_________。(已知25℃時,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20)
(4)在25℃下,將a mol·L-1的氨水與0.01 mol·L-1的鹽酸等體積混合,反應平衡時溶液中c(NH4+)=c(Cl-),則溶液顯_____________性(填“酸”、“堿”、或“中”);用含a的代數式表示NH3·H2O的電離常數Kb=__________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com