
科目: 來源:2016-2017學年黑龍江省高一下學期開學考試化學試卷(解析版) 題型:選擇題
已知在堿性溶液中可發生如下反應:Fe(OH)3+ClO-+OH-→FeO42-+Cl-+H2O(未配平)。則有關敘述不正確的是( )
A. FeO42-中Fe的化合價是+6價
B. 每產生1molCl-,轉移2mol電子
C. 反應中氧化劑與還原劑的物質的量之比為2:3
D. FeO42-具有強氧化性,一般其還原產物為Fe3+,可用作新型自來水消毒劑和凈水劑
查看答案和解析>>
科目: 來源:2016-2017學年黑龍江省高一下學期開學考試化學試卷(解析版) 題型:選擇題
現有CuO和Fe3O4的混合物7.2g,向其中加入1mol·L-1的H2SO4溶液150mL恰好完全反應,若將14.4 g該混合物用足量CO還原,充分反應后剩余固體質量為( )
A. 3.2g B. 4.8g C. 6g D. 9.6g
查看答案和解析>>
科目: 來源:2016-2017學年黑龍江省高一下學期開學考試化學試卷(解析版) 題型:選擇題
向含Na2CO3、NaAlO2的混合溶液中逐滴加入150mL 1mol•L-1的HCl溶液,測得溶液中的某幾種離子物質的量的變化如圖所示,則下列說法不正確的是( )
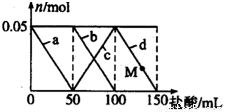
A. a曲線表示的離子方程式為:AlO2-+H++H2O=Al(OH)3
B. b和c曲線表示的離子反應是相同的
C. M點時Al(OH)3的質量小于3.9g
D. 原混合溶液中的CO32-與AlO2-的物質的量之比為2:1
查看答案和解析>>
科目: 來源:2016-2017學年黑龍江省高一下學期開學考試化學試卷(解析版) 題型:實驗題
Ⅰ.實驗室需要配制0.1 mol·L-1NaOH溶液500mL。
(1)根據計算用托盤天平稱取的質量為__________g。在下圖所示儀器中,配制上述溶液肯定不需要的是_________(填序號),除圖中已有儀器外,配制上述溶液還需要的玻璃儀器是 _____________。
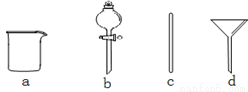
(2)配制時,其正確的操作順序是(用字母表示,每個操作只用一次)__________。
A.用少量水洗滌燒杯2次~3次,洗滌液均注入容量瓶,振蕩
B.在盛有NaOH固體的燒杯中加入適量水溶解
C.將燒杯中已冷卻的溶液沿玻璃棒注入容量瓶中
D.將容量瓶蓋緊,反復上下顛倒,搖勻
E.改用膠頭滴管加水,使溶液凹液面恰好與刻度相切
F.繼續往容量瓶內小心加水,直到液面接近刻度1 cm~2 cm處
(3)下面操作造成所配NaOH溶液濃度偏高的是(_____)
A.溶解后溶液沒有冷卻到室溫就轉移
B.轉移時沒有洗滌燒杯、玻璃棒
C.向容量瓶加水定容時眼睛俯視液面
D.搖勻后發現液面低于刻度線,又加蒸餾水至刻度線.
II.向濃度相等、體積均為100 mL 的 A、B 兩份NaOH 溶液中,分別通入一定量的 CO2 后,再向所得溶液中滴加0.1 mol/L 鹽酸 , 產生 CO2 的體積(標準狀況)與所加鹽酸的體積關系如圖所示。
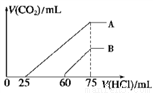
(4)①A 曲線表明,原溶液通入CO2后,所得溶質與鹽酸反應產生CO2 的最大體積是_________mL(標準狀況)。
②B 曲線表明,原溶液通入CO2后,所得溶液中溶質的化學式為______________。
III.某學生用 Na2CO3和 NaHCO3 組成的某混合物進行實驗,測得如下數據(鹽酸的物質的量濃度相等且不考慮HCl的揮發)
實驗序號 | ① | ② | ③ |
鹽酸體積/mL | 50 | 50 | 50 |
固體質量/g | 4.11 | 8.22 | 16.44 |
生成氣體體積/L(標況) | 1.008 | 2.016 | 2.016 |
(5)原混合物樣品中 n(Na2CO3)∶n(NaHCO3)=____________ , 鹽酸的物質的量濃度為________mol/L ,實驗③反應后,至少需繼續加入_____mL的該鹽酸溶液才能把混合物全部反應。
查看答案和解析>>
科目: 來源:2016-2017學年黑龍江省高一下學期開學考試化學試卷(解析版) 題型:填空題
鐵和鋁是日常生活中用途廣泛的金屬。
I.(1)向NaAlO2溶液中滴加AlCl3溶液,生成白色膠狀沉淀,則發生反應的離子方程式為_________________________。
(2)實驗室常用還原性 Fe 粉與水蒸氣反應的實驗來研究 Fe 的還原性,則該反應的化學方程式為_________________________。
(3)電子工業用FeCl3溶液腐蝕敷在絕緣板上的銅制造印刷電路板,請寫出FeCl3溶液與銅反應的離子方程式:__________________________。
II.已知合金A由兩種常見金屬組成。為測定其組成,某同學的實驗流程如圖所示:
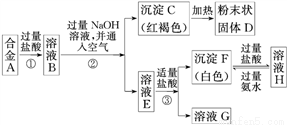
請回答:
(4)溶液E中所含的溶質是_________________(寫化學式)
(5)合金A中的一種金屬可以與粉末狀固體D在高溫下反應生成合金A中的另一種金屬,請寫出該反應的化學方程式_____________________________。
查看答案和解析>>
科目: 來源:2016-2017學年黑龍江省高一下學期開學考試化學試卷(解析版) 題型:填空題
I.明礬石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O,還含有少量Fe2O3雜質,可利用明礬石制備氫氧化鋁。
(1)已知明礬石脫水后要硫化,化學方程式為2Al2(SO4)3+3S 2Al2O3+9SO2,該反應的氧化劑與還原劑的物質的量之比是___________;若生成1 mol Al2O3,則轉移的電子數為________。
2Al2O3+9SO2,該反應的氧化劑與還原劑的物質的量之比是___________;若生成1 mol Al2O3,則轉移的電子數為________。
(2)證明廢渣中含有Fe2O3 的化學方法:_____________________。
II.鎂鋁合金(Mg17Al12 )是一種潛在的貯氫材料,可在氬氣保護下,將一定化學計量比的Mg、Al 單質在一定溫度下熔煉獲得。該合金在一定條件下完全吸氫的反應方程式為:Mg17Al12 + 17H2=17MgH2 + 12Al ,得到的混合物Y(17MgH2 +12Al)在一定條件下可釋放出氫氣。
(3)熔煉制備鎂鋁合金(Mg17Al12)時通入氬氣的目的是_____________________
(4)在6.0 mol·L-1 HCl 溶液中,混合物Y 能完全釋放出H2。1 mol Mg17Al12 完全吸氫后得到的混合物Y 與上述鹽酸完全反應,釋放出H2的物質的量為_______mol。(已知:MgH2 + 2HCl = MgCl2 + 2H2↑)
查看答案和解析>>
科目: 來源:2017屆浙江省高三3月選考化學試卷(解析版) 題型:選擇題
下列反應中,氧元素被還原的是
A. 2Na+O2 Na2O2 B. Na2O+H2O=2NaOH
Na2O2 B. Na2O+H2O=2NaOH
C. 2F2+ 2H2O=4HF+ O2 D. 2C+SiO2 2CO↑+Si
2CO↑+Si
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com