
科目: 來源: 題型:填空題

| 氫氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 開始沉淀pH | 1.5 | 3.3 | 9.4 |
查看答案和解析>>
科目: 來源: 題型:解答題
 +Na2Cr2O7+H2SO4$\stackrel{55℃~60℃}{→}$
+Na2Cr2O7+H2SO4$\stackrel{55℃~60℃}{→}$ +H2O
+H2O| 物質 | 沸點(℃) | 密度(g•cm-3,20℃) | 溶解性 |
| 環己醇 | 161.1(97.8)* | 0.9624 | 能溶于水和醚 |
| 環己酮 | 155.6(95)* | 0.9478 | 微溶于水,能溶于醚 |
| 水 | 100.0 | 0.9982 |

 .
.查看答案和解析>>
科目: 來源: 題型:解答題
 醇與氫鹵酸反應是制備鹵代烴的重要方法.實驗室制備溴乙烷的裝置如圖所示,試管d中裝有少量蒸餾水.已知溴乙烷的沸點為38.4℃,密度為1.43g/mL;可能存在的副反應有:加熱反應過程中反應混合物會呈現黃色甚至紅棕色;醇在濃硫酸的存在下脫水生成烯和醚等.實驗步驟中:在圓底燒瓶中加入10g乙醇、足量濃硫酸,然后加入研細的20.6g溴化鈉和幾粒碎瓷片.
醇與氫鹵酸反應是制備鹵代烴的重要方法.實驗室制備溴乙烷的裝置如圖所示,試管d中裝有少量蒸餾水.已知溴乙烷的沸點為38.4℃,密度為1.43g/mL;可能存在的副反應有:加熱反應過程中反應混合物會呈現黃色甚至紅棕色;醇在濃硫酸的存在下脫水生成烯和醚等.實驗步驟中:在圓底燒瓶中加入10g乙醇、足量濃硫酸,然后加入研細的20.6g溴化鈉和幾粒碎瓷片.查看答案和解析>>
科目: 來源: 題型:解答題


| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 開始沉淀時 | 3.4 | 6.3 | 1.5 |
| 完全沉淀時 | 4.7 | 8.3 | 2.8 |
查看答案和解析>>
科目: 來源: 題型:解答題
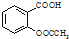 )是世界上應用最廣泛的解熱、鎮痛和抗炎藥.乙酰水楊酸受熱易分解,分解溫度為128~135℃.某學習小組在實驗室以水楊酸(鄰羥基苯甲酸)與醋酸酐[(CH3CO)2O]為主要原料合成阿司匹林,制備基本操作流程如下:
)是世界上應用最廣泛的解熱、鎮痛和抗炎藥.乙酰水楊酸受熱易分解,分解溫度為128~135℃.某學習小組在實驗室以水楊酸(鄰羥基苯甲酸)與醋酸酐[(CH3CO)2O]為主要原料合成阿司匹林,制備基本操作流程如下:
| 名稱 | 相對分子質量 | 熔點或沸點 (℃) | 水 |
| 水楊酸 | 138 | 158(熔點) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸點) | 反應 |
| 乙烯水楊酸 | 180 | 135(熔點) | 微溶 |


查看答案和解析>>
科目: 來源: 題型:解答題
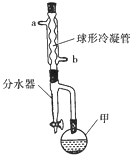 乙酸異戊酯常作為配制香蕉、梨、蘋果等多種口味食品的香料.實驗室合成乙酸異戊酯的原料是乙酸和異戊醇[(CH3)2CHCH2CH2OH],其裝置如圖所示.
乙酸異戊酯常作為配制香蕉、梨、蘋果等多種口味食品的香料.實驗室合成乙酸異戊酯的原料是乙酸和異戊醇[(CH3)2CHCH2CH2OH],其裝置如圖所示.| 甘油 | 環已烷 | 乙酸 | 異戊醇 | |
| 沸點/℃ | 290 | 80.7 | 117.9 | 132.5 |
| 密度/g•cm-3 | 1.26 | 0.78 | 1.05 | 0.81 |
查看答案和解析>>
科目: 來源: 題型:填空題

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 開始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |

查看答案和解析>>
科目: 來源: 題型:填空題

| 編號 | 氮化鋁樣品質量 | 量氣管第一次讀數 | 量氣管第二次讀數 |
| ① | 1.0g | 350.0mL | 13.7mL |
| ② | 1.0g | 350.0mL | 25.0mL |
| ③ | 1.0g | 350.0mL | 14.3mL |
查看答案和解析>>
科目: 來源: 題型:解答題


查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com