
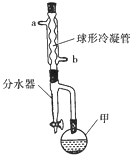
 乙酸異戊酯常作為配制香蕉、梨、蘋果等多種口味食品的香料.實驗室合成乙酸異戊酯的原料是乙酸和異戊醇[(CH3)2CHCH2CH2OH],其裝置如圖所示.
乙酸異戊酯常作為配制香蕉、梨、蘋果等多種口味食品的香料.實驗室合成乙酸異戊酯的原料是乙酸和異戊醇[(CH3)2CHCH2CH2OH],其裝置如圖所示.| 甘油 | 環已烷 | 乙酸 | 異戊醇 | |
| 沸點/℃ | 290 | 80.7 | 117.9 | 132.5 |
| 密度/g•cm-3 | 1.26 | 0.78 | 1.05 | 0.81 |
分析 (1)CH3COOH與(CH3)2CHCH2CH2OH反應生成CH3COOCH2CH2CH(CH3)2和H2O;
(2)根據儀器形狀確定名稱;
(3)降低生成物的濃度平衡向正反應方向移動,冷凝水下進上出;
(4)甘油浴加熱便于控制反應溫度;
(5)當不再生成水,反應達到平衡;
(6)Na2CO3溶液能與乙酸反應;
(7)無水硫酸鎂具有吸水性;
(8)先計算出乙酸和異戊醇的物質的量,然后判斷過量情況,根據不足量計算出理論上生成乙酸異戊酯的物質的量,最后根據實際上制取的乙酸異戊酯計算出產率.
解答 解:(1)CH3COOH與(CH3)2CHCH2CH2OH反應生成CH3COOCH2CH2CH(CH3)2和H2O,化學方程式為CH3COOH+(CH3)2CHCH2CH2O$?_{△}^{濃硫酸}$CH3COOCH2CH2CH(CH3)2+H2O,故答案為:CH3COOH+(CH3)2CHCH2CH2O$?_{△}^{濃硫酸}$CH3COOCH2CH2CH(CH3)2+H2O;
(2)儀器甲為圓底燒瓶,故答案為:圓底燒瓶;
(3)降低生成物的濃度平衡向正反應方向移動,可提高反應物的轉化率或生成物的產率,冷凝水下進上出,從b口進水,故答案為:提高反應物的轉化率或生成物的產率;b;
(4)甘油浴加熱便于控制反應溫度、使圓底燒瓶受熱均勻,故答案為:便于控制反應溫度;使圓底燒瓶受熱均勻;
(5)當不再生成水,反應達到平衡,停止加熱,故答案為:水層高度(或水的體積、液面對應刻度)不再變化;
(6)乙酸異戊酯在飽和碳酸鈉中的溶解度比在水中的小,Na2CO3溶液能與乙酸反應,故答案為:ad;
(7)無水硫酸鎂具有吸水性,能作干燥劑,所以無水硫酸鎂的作用是作干燥劑,故答案為:作干燥劑;
(8)乙酸的物質的量為:n=$\frac{100g}{60g/mol}$=1.67mol,異戊醇的物質的量為:n=$\frac{20g}{88g/mol}$=0.227mol,由于乙酸和異戊醇是按照1:1進行反應,所以乙酸過量,生成乙酸異戊酯的量要按照異戊醇的物質的量計算,即理論上生成0.227mol乙酸異戊酯;實際上生成的乙酸異戊酯的物質的量為:$\frac{13g}{130g/mol}$=0.1mol,所以實驗中乙酸異戊酯的產率為:$\frac{0.1mol}{0.227mol}$×100%=44%,故答案為:44%.
點評 本題考查制備實驗方案設計,涉及物質的制備、物質產率的計算等知識,試題涉及的題量較大,知識點較多,充分培養了學生的分析、理解能力及靈活應用所學知識的能力,題目難度中等.


 輕松奪冠全能掌控卷系列答案
輕松奪冠全能掌控卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | Na+、Ba2+、Cl?、SO42- | B. | Ca2+、HCO3?、C1?、K+ | ||
| C. | HCO3?、K+、I?、H+ | D. | H+、Cl?、Na+、CO32 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 小于0.5 mol•L-1 | B. | 等于0.5 mol•L-1 | C. | 大于0.5 mol•L-1 | D. | 無法確定 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 正反應為放熱反應 | |
| B. | 加入催化劑,該化學反應的反應熱不變 | |
| C. | 反應物總能量高于生成物總能量 | |
| D. | 升高溫度可增大正反應速率,降低逆反應速率 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題


查看答案和解析>>
科目:高中化學 來源: 題型:填空題

| 氫氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 開始沉淀pH | 1.5 | 3.3 | 9.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | AlCl3 和NaOH | B. | H2SO4和BaCl2 | C. | NaHCO3和HCl | D. | NaCl和AgNO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NaOH | B. | NaCl | C. | Na2CO3 | D. | NaBr |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com